-
Medical journals
- Career
Nové obzory ve farmakoterapii obezity
Authors: V. Hainer; R. Taxová Braunerová; P. Kalousková; M. Kunešová
Authors‘ workplace: Endokrinologický ústav Centrum pro diagnostiku a léčbu obezity Ředitelka: doc. RNDr. Běla Bendlová, CSc.
Published in: Prakt. Lék. 2023; 103(4): 163-169
Category: Reviews
Overview
Nevelký nebo dočasný hmotnostní úbytek, kterého se dosahovalo s většinou antiobezitik, která byla v minulosti k dispozici, nesplnil očekávání jak pacientů, tak lékařů. Kombinované léky a analoga gastrointestinálních hormonů představují nový, účinnější a bezpečnější přístup k léčbě obezity a s ní spojených zdravotních rizik. Analoga intestinálních hormonů, jako je např. analog glucagon like peptidu-1 (GLP-1) liraglutid, byla zprvu úspěšně použita v léčbě diabetu 2. typu a až později v léčbě obezity. Článek informuje o klinických studiích 3. fáze s novými analogy intestinálních hormonů, o agonistovi GLP-1 semaglutidu a o duálním agonistovi intestinálních hormonů tirzepatidu; jeho jedna molekula cílí na receptory dvou střevních hormonů GLP-1 a GIP (glucose-dependent insulinotropic polypeptide). Jak semaglutid, tak tirzepatid se aplikují podkožně jednou týdně. Hmotnostní redukce docílená s těmito léky, zvláště s tirzepatidem, je srovnatelná s tou, kterou pozorujeme po méně invazivních bariatrických výkonech a je provázena významným zlepšením kardiometabolických rizik a příznivým bezpečnostním profilem. Gastrointestinální nežádoucí účinky po těchto lécích jsou obvykle přechodného charakteru a jsou mírné až střední závažnosti. Semaglutid byl již schválen k dlouhodobé léčbě obezity Evropskou lékovou agenturou (EMA), zatímco schválení tirzepatidu se očekává. Klinické studie s orálním semaglutidem, trojitým inkretinovým agonistou retatrutidem, nepeptidickým orálním agonistou GLP-1 orforglipronem a kombinací cagrilintidu se semaglutidem přinesla rovněž nadějné výsledky v redukčním režimu. Na druhé straně setmelanotid je lék, který působí na melanokortinový receptor 4 a je vyhrazen pro léčbu velmi vzácných monogenních onemocnění, která se projevují těžkou obezitou manifestující se v raném dětství, např. při deficitu proopiomelanokortinu nebo leptinového receptoru. Individualizovaná léčba antiobezitiky by měla být integrální součástí komplexní léčby obezity zahrnující dietu, pohybovou aktivitu a kognitivně behaviorální intervenci. Řádně vyškolení lékaři by měli být garantem úspěšnosti léčby antiobezitiky. Navíc, ministerstvo zdravotnictví a zdravotní pojišťovny by měly vzít v úvahu, že cena nových antiobezitik zabraňuje této účinné léčbě u většiny indikovaných pacientů, a proto by měla být přijata opatření k zajištění patřičné dostupnosti těchto léků.
Klíčová slova:
antiobezitika – redukce hmotnosti – semaglutid – tirzepatid – setmelanotid – analoga inkretinů – kardiometabolická rizika
ÚVOD
Obezita je chronické onemocnění, které nabylo charakteru globální epidemie. Podle Světové zdravotnické organizace v posledních čtyřech dekádách došlo u dospělých k trojnásobnému vzestupu počtu dospělých jedinců s obezitou. V Evropě včetně České republiky převyšuje počet dospělých s nadváhou a obezitou 50 %, přičemž ⅕ až ¼ dospělé populace je obézní. Narůstající prevalence nadváhy a obezity s sebou přináší závažné zdravotní a socioekonomické následky. S obezitou se pojí vyšší výskyt diabetu 2. typu, kardiovaskulárních onemocnění, degenerativních onemocnění pohybového aparátu a některých nádorů. Obezita ovlivňuje nejen nemocnost a invaliditu, ale i kvalitu a délku života (25). Léčba obezity navozením negativní energetické bilance cílí jak na redukci celkového tělesného tuku, tak zejména na redukci útrobního tuku a kardiometabolických rizik. Omezení energetického příjmu pomocí nízkoenergetické diety a zvýšení energetického výdeje zvýšenou pohybovou aktivitou bývá i při aplikaci běžné kognitivně behaviorální intervence dlouhodobě málo účinné. Prognózu dlouhodobého redukčního režimu zlepšuje intenzivní, avšak časově náročná modifikace životního stylu spojená s větší frekvencí kontrol či skupinových setkání (40).
Účinnost komplexní intervence životního stylu lze podpořit léky, antiobezitiky. Ta přispívají k normalizaci regulačních a/nebo metabolických poruch, které se podílejí na patogenezi obezity a na rozvoji s obezitou spojených kardiometabolických rizik. Antiobezitika tak přispívají u pacientů s obezitou nejen k větší redukci hmotnosti, ale i k větší redukci kardiometabolických rizik oproti jedincům, jimž bylo při stejné behaviorální intervenci životního stylu podáváno placebo (10, 11, 13, 22). Hmotnostní redukce docílená farmakoterapií obezity v minulosti většinou neuspokojila očekávání nejen pacientů, ale i lékařů. Antiobezitika se obvykle podávala jen po omezenou dobu buď v důsledku jejich malé účinnosti a výši finanční úhrady pacientem anebo vzhledem k časovému omezení preskripce s cílem omezit nežádoucí účinky. Stažení několika antiobezitik z trhu (např. dexfenfuraminu, sibutraminu, rimonabantu, lorkaserinu) či ukončení jejich klinického zkoušení (např. ecopipamu, některých stimulátorů beta-3-adre-nergních receptorů) vzhledem k výskytu nežádoucích účinků podpořilo skeptický pohled odborné veřejnosti na farmakoterapii obezity (11). Nový přístup v léčbě obezity představují kombinované přípravky a analoga hormonů gastrointestinálního traktu (GIT), které splňují požadavky lékových agentur jak na účinnost, tak na bezpečnost. Z těchto léků jsou u nás k dispozici kombinace naltrexonu s bupropionem (Mysimba®) a analog glukagonu podobného peptidu 1 (glucagon-like peptide-1 – GLP-1) liraglutid (Saxenda®). O klinických studiích s těmito přípravky bylo referováno v přehledné kapitole (11). Podobně jako u liraglutidu probíhaly klinické studie s dalšími analogy GLP-1 nejdříve u pacientů s diabetes mellitus 2. typu (DM2), u nichž se osvědčila jako účinná a bezpečná antidiabetika.
V tomto sdělení podáváme informaci o nových antiobezitikách, z nichž některá jsou již k dispozici pro léčbu indikovaných pacientů, a u jiných se předpokládá uvedení na trh v nejbližší době. Věnujeme se analogu GLP-1 semaglutidu a agonistovi melanokortinového receptoru 4 (MC4R) setmelanotidu, které již byly schváleny k léčbě indikovaných pacientů Evropskou lékovou agenturou (European Medicines Agency, EMA). Další antiobezitika, o nichž referujeme (tirzepatid, retatrutid, orforglipron), úspěšně prošla různými fázemi klinického zkoušení.
SEMAGLUTID
Semaglutid jako analog GLP-1 je z 94 % identický s tímto endogenním hormonem a již se osvědčil v léčbě DM2 (Ozempic®). Semaglutid při vysoké glykemii stimuluje sekreci inzulinu a potlačuje sekreci glukagonu, přičemž při nízké glykemii naopak tlumí sekreci inzulinu, aniž ovlivňuje sekreci glukagonu. Snižuje příjem potravy jednak působením v centrálním nervovém systému, jednak i tím, že zpomaluje vyprazdňování žaludku.
Semaglutid v léčbě DM2. Semaglutid podávaný v podkožní injekci jednou týdně byl zkoumán v léčbě DM 2. typu ve studiích SUSTAIN 1-10 (1, 2, 4, 21, 32, 33, 38). Eliaschewitz et al. (7) shrnuli výsledky studií PIONEER 1-10, v nichž byl semaglutid pacientům s DM 2. typu podáván perorálně. Semaglutid u pacientů s DM2 a vysokým kardiovaskulárním rizikem snižuje výskyt akutních kardiovaskulárních příhod (29). O použití semaglutidu v léčbě pacientů s DM 2. typu u nás referoval Haluzík (14).
Později proběhly klinické studie s uplatněním semaglutidu v léčbě obezity a s ní spojených kardiometabolických rizik (studie STEP 1-5) (26, 37). Výhodou semaglutidu oproti liraglutidu (Saxenda®) je podávání pouze jednou týdně v podkožní injekci a docílená větší redukce hmotnosti oproti placebu (14,9 % vs. 2,9 %). Podávaný podkožně jednou týdně zlepšuje kompenzaci DM 2. typu a navozuje významný pokles tělesné hmotnosti. Ve studiích u diabetiků byl semaglutid při podkožní aplikaci podáván v dávce 0,5 a 1 mg, ve studiích, v nichž byl podáván pacientům s obezitou, bylo použito podobně jako u liraglutidu vyšší dávky, a to 1,0 a 2,4 mg (37).
Semaglutidu jako antiobezitiku se věnovalo pět studií STEP (6, 9, 34, 41, 44). Wilding et al. (44) srovnávali ve skupině 1961 pacientů s nadváhou či obezitou vliv podávání semaglutidu v dávce 2,4 mg s.c. jednou týdně a placeba po dobu 68 týdnů. Po semaglutidu došlo k redukci tělesné hmotnosti o 14,9 % (15,3 kg), zatímco při aplikaci placeba o 2,4 % (2,6 kg). Redukce hmotnosti o 10 % a více docílilo 69,1 % pacientů léčených semaglutidem a pouze 12 % těch, kteří dostávali placebo. Pacienti léčení semaglutidem vykazovali signifikantně větší zlepšení kardiometabolických rizik oproti jedincům, kteří dostávali placebo. Obdobná randomizovaná a dvojitě zaslepená studie Waddena et al. (41) poukázala na význam léčby obezity a nadváhy semaglutidem (2,4 mg s.c. jednou týdně) v kombinaci s definovanou nízkoenergetickou dietou podávanou v prvních 8 týdnech a s intenzivní behaviorální terapií aplikovanou po dobu 68 týdnů. Iniciálně bylo do intervenované skupiny zařazeno 407 pacientů a do placebové skupiny 204 pacientů. Pacienti léčení semaglutidem zredukovali svou výchozí hmotnost o 16 %, zatímco jedinci v placebové skupině o 5,7 %. Více jedinců v intervenované oproti placebové skupině zredukovalo hmotnost jak o ≥ 5 % (86,6 % vs. 47,6 %, p < 0,001), tak o ≥ 10 % (75,3 % vs. 27,0 %, p < 0,001) a o ≥ 15 % (55,8 % vs. 13,2 %, p < 0,001).
Semaglutid se rovněž příznivě uplatnil při ovlivnění relapsu hmotnostního vzestupu po chirurgické léčbě obezity (30). Hmotnostní redukce u těchto pacientů byla větší při léčbě semaglutidem než liraglutidem.
Weghuber et al. (42) referovali o léčbě semaglutidem u adolescentů s obezitou ve věku 12–18 let. Semaglutid podávaný v dávce 2,4 mg jednou týdně po dobu 68 týdnů navodil redukci indexu tělesné hmotnosti (Body Mass Index – BMI) o 16,1 %, zatímco po placebu se BMI snížil pouze o 0,6 %. Semaglutid oproti placebu rovněž příznivěji ovlivnil kardiometabolická rizika (obvod pasu, glykovaný hemoglobin a lipidy). Výskyt nežádoucích gastrointestinálních účinků byl častější u adolescentů léčených semaglutidem než u těch, kteří dostávali placebo, nicméně jen vzácně vedl k ukončení léčby. V průběhu podávání semaglutidu nebylo pozorováno ovlivnění růstu či pubertálního vývoje.
Indikační kritéria, výskyt nežádoucích účinků a kontraindikace podávání semaglutidu shrnula nedávno publikovaná studie z Pennsylvánské univerzity (17). V prvních dnech podávání semaglutidu se nejčastěji vyskytují nežádoucí gastrointestinální účinky lehčího charakteru (nauzea, zvracení, průjmy či zácpa), které většinou v průběhu další léčby ustupují. Prokázalo se, že tyto nežádoucí účinky vedou k přerušení léčby jen u 4,3 % pacientů. Po podávání agonistů GLP-1 receptorů se při rychlejším hmotnostním poklesu zvyšuje riziko vzniku cholelitiázy. Po jejich podávání rovněž dochází k nevelkému zvýšení tepové frekvence. Probíhající klinická studie hodnotí podávání semaglutidu u pacientů s obezitou a srdečním selháváním při zachovalé ejekční frakci. V současnosti probíhá rovněž studie hodnotící vliv podávání semaglutidu na výskyt závažných kardiovaskulárních příhod u pacientů s obezitou a nadváhou (35). Kontraindikace podávání semaglutidu jsou obdobné jako u liraglutidu: medulární karcinom štítné žlázy či syndrom mnohočetné endokrinní neoplazie 2. typu (MEN 2), hypersenzitivita na přípravek, těhotenství a akutní pankreatitida v anamnéze.
Bezpochyby je povzbudivé, že semaglutid (Wegovy®) byl v roce 2022 schválen Evropskou lékovou agenturou (EMA) k léčbě obezity u indikovaných pacientů. Využití semaglutidu jako antiobezitika může významně omezovat podobně jako u liraglutidu jeho vysoká cena. Perspektivou v léčbě diabetu i obezity je perorální forma semaglutidu s podáváním jednou za den. Klinické studie umožnily schválení perorálního semaglutidu (Rybelsus®) v léčbě DM2 Evropskou lékovou agenturou již v dubnu 2020. Výsledky klinické studie 3. fáze s léčbou perorálním semaglutidem u pacientů s obezitou nebo nadváhou (OASIS 1), kteří neměli DM2, byly publikovány v červnu 2023 (24). Pacienti dostávali po dobu 68 týdnů buď semaglutid v dávce 50 mg/den, nebo placebo. Po podávání semaglutidu došlo ke klinicky významné redukci hmotnosti oproti placebu (–15,1 % vs. 2,4 %). Vesměs lehké nežádoucí gastrointestinální účinky, které časem ustupovaly, byly častější po podávání semaglutidu než po podávání placeba (80 % vs. 46 %).
TIRZEPATID
Tirzepatid představuje nový přístup v léčbě obezity a DM2, kdy se kombinací agonistů receptorů více hormonů gastrointestinálního traktu docílí větší účinnosti i bezpečnosti přípravku (18, 31). U tirzepatidu se jedná o kombinaci analoga GLP-1 s analogem inzulinotropního peptidu závislého na glukóze (glucose-dependent insulinotropic peptide – GIP). Tirzepatid tlumí chuť k jídlu a snižuje příjem potravy jak působením v CNS, tak tím, že zpomaluje vyprazdňování žaludku. Mimo to zvyšuje syntézu a sekreci inzulinu, indukuje delší přežívání beta-buněk pankreatu a zvyšuje lipolýzu.
Významné je i kardioprotektivní působení tirzepatidu. O mechanismu působení tirzepatidu a jeho klinickém využití v léčbě obezity a diabetu jsme zevrubněji referovali v souhrnném sdělení (12).
Metaanalýza sedmi studií srovnávala účinnost a bezpečnost tirzerpatidu při léčbě DM2 v dávce 5, 10 a 15 mg s placebem, s inzulinem glarginem, inzulinem degludec a s agonisty GLP-1 semaglutidem a dulaglutidem (23). Léčba tirzepatidem navodila významný pokles koncentrace glykovaného hemoglobinu, a to o 17,7 mmol/l po dávce 5 mg, o 20,2 mmol/l po dávce 10 mg a 22,3 mmol/l po dávce 15 mg. Tento pokles HbA1c byl signifikantně vyšší jak ve srovnání s placebem, tak s podávanými agonisty GLP1 receptorů.
Podáváním tirzepatidu se docílilo u diabetiků rovněž významné redukce tělesné hmotnosti, a to o 6,3 kg po dávce 5 mg, o 8,4 kg po dávce 10 mg a o 9,3 kg po dávce 15 mg. Jak pokles HbA1c, tak pokles tělesné hmotnosti po tirzepatidu byl signifikantně vyšší jak ve srovnání s placebem, tak s podávanými agonisty GLP-1. Tirzepatid u diabetiků příznivě ovlivňuje lipidové spektrum, zejména významně snižuje sérové triglyceridy a rovněž redukuje koncentrace zánětlivých cytokinů. S úpravou inzulinové rezistence a lipidového spektra dochází i ke zlepšení ukazatelů nealkoholové steatózy jater. Tirzepatid (Mounjaro®) byl v květnu 2022 schválen americkou Federální lékovou agenturou (Federal Drug Administration – FDA) k léčbě pacientů s DM2 při současně aplikované dietní a pohybové intervenci životního stylu (36).
Úloze tirzepatidu v léčbě obezity a nadváhy (s BMI ≥ 27 kg/m2) se věnovala studie SURMOUNT-1 (19). Do randomizované dvojitě zaslepené studie bylo zařazeno 2539 pacientů s alespoň jednou zdravotní komplikací obezity, avšak s výjimkou DM2. Nicméně u 1032 (40,6 %) pacientů byl diagnostikován před započetím studie prediabetes. Pacienti dostávali podkožní injekcí jednou týdně buď tirzepatid (5 mg, 10 mg, 15 mg), nebo placebo. Po 72 týdnech došlo v intervenovaných skupinách oproti placebu k významné (p < 0,001) redukci jak tělesné hmotnosti, tak k poklesu délky obvodu pasu (tab. 1). Hmotnostní redukce docílená podáváním tirzepatidu byla významně vyšší než po jiných doposud používaných antiobezitikách a byla srovnatelná s redukcí hmotnosti po některých méně invazivních bariatrických výkonech.
U intervenovaných skupin došlo ve srovnání s placebem k významně většímu zlepšení kardiometabolických rizik včetně délky obvodu pasu, systolického a diastolického krevního tlaku, lipidového profilu, inzulinu na lačno a aktivity aspartát aminotransferázy. Téměř všichni pacienti (> 95 %), jimž byl v intervenovaných skupinách iniciálně diagnostikován prediabetes, docílili po léčbě normoglykemie. Nežádoucí účinky po podávání tirzepatidu podobně jako po agonistech GLP-1 mají gastrointestinální charakter (nauzea, průjem, zácpa), bývají obvykle mírné a mají přechodný charakter. Nicméně se po tirzepatidu vyskytují méně často než při monoterapii analogy GLP-1, a to zřejmě díky přítomnosti GIP v molekule tirzepatidu.
RETATRUTID
Retatrutid je agonistou receptorů tří gastrointestinálních hormonů: GLP-1, GIP a glukagonu. Nedávno byla publikována zpráva o 2. fázi klinického zkoušení tohoto preparátu v léčbě nadváhy a obezity (20). Retatrutid byl podáván podkožně jednou týdně po dobu 48 týdnů. Po všech dávkách preparátu došlo k významnému poklesu tělesné hmotnosti: po 1 mg o 8,7 %, po 4 mg o 17,1 %, po 8 mg o 22,8 % a po 12 mg o 24,2 %, zatímco v placebové skupině poklesla hmotnost pouze o 2,1 %. Nežádoucí účinky po retatrutidu byly obvykle méně závažné a měly charakter gastrointestinálních potíží. Bylo pozorováno nevelké zvýšení tepové frekvence, která však po 24 týdnech podávání klesala.
ORFORGLIPRON
Orforglipron je agonistou GLP-1 receptorů, který nemá peptidický charakter, což umožňuje jeho perorální podávání. Ve 2. fázi klinického zkoušení byl podáván po dobu 36 týdnů v dávkách 12, 24, 36 a 45 mg jednou denně (43). Redukce hmotnosti po orforglipronu dosahovala v 36. týdnu v závislosti na dávce 9,4–14,7 %, přičemž po placebu klesla hmotnost o 2,3 %. Po podávání orforglipronu došlo k významné redukci kardiometabolických rizik. Podobně jako po jiných agonistech GLP-1 převažovaly po podávání tohoto preparátu nežádoucí gastrointestinální příznaky lehkého a nevýrazného charakteru. Bezpochyby výhodou tohoto antiobezitika by mohla být vedle perorálního podávání i jeho předpokládaná nižší cena na trhu ve srovnání s přípravky peptidického charakteru.
V přehledném sdělení bylo nedávno referováno o kombinaci analog hormonů GIT v 1. fázích klinického zkoušení (22). Sem patří např. přípravek CagriSema, který je kombinací agonisty amylinového receptoru cagrilintidu se semaglutidem, či duální agonista receptoru GLP-1 a glukagonu.
SETMELANOTID V LÉČBĚ VZÁCNÝCH MONOGENNÍCH OBEZIT
Monogenní obezity jsou vzácná onemocnění vznikající v důsledku mutace genů kódujících hormony, resp. neuropeptidy a jejich receptory, které jsou zapojeny do systému regulace příjmu potravy v CNS prostřednictvím leptin melanokortinové signalizační osy. Podílí se pouze 3–4 % na všech případech těžké obezity vzniklé v raném dětství. Vesměs se jedná o mutace genu pro melanokortinový receptor 4 (MC4R). Ostatní mutace jsou velmi vzácné. Prevalence mutace leptinového genu je u homozygotů 1 : 4 400 000. Predikovaná prevalence mutace genu leptinového receptoru je 1,34 na milion obyvatel. Mendelovsky děděné syndromy spojené s obezitou jsou rovněž vzácná onemocnění spojená často s mentální retardací, dysmorfií a orgánově specifickými vývojovými vadami. Prevalence Bardetova-Biedlova syndromu se udává jeden případ na 100 000 obyvatel. Fenotypy monogenních obezit a syndromů spojených s obezitou jsou popsány v nedávno publikované monografii o obezitě (3).
Úspěšná léčba mutace genu pro leptin syntetickým derivátem tohoto hormonu metreleptinem byla popsána již v roce 1999 (8) a od roku 2014 je k léčbě deficitu leptinu tento lék k dispozici. Příznivě ovlivňuje nejen metabolické, ale i neuroendokrinní a psychobehaviorální poruchy spojené s leptinovým deficitem. Úspěšnou léčbu dalších poruch melanokortinové signalizace otevřel agonista melanokortinového receptoru 4 (MC4R) setmelanotid. Clément et al. (5) a Kühnen et al. (27) referovali o úspěšné léčbě mutací genu leptinového receptoru (LEPR) a mutací genu proopiomelanokortinu (POMC) setmelanotidem.
Indikace podávání setmelanotidu. Americká léková agentura v listopadu 2020 a Evropská léková agentura v červenci 2021 schválily podávání setmelanotidu (Imcivree®) jako léku první volby při dlouhodobém redukčním režimu u pacientů ve věku nad 6 let se vzácnými formami obezity při mutacích, které mají za následek deficit anorexigenní signalizace prostřednictvím POMC, PCSK1 (proprotein konvertáza subtilisin/ kexin typu 1) a LEPR. Wabitsch et al. (39) popsali příznivé ovlivnění trajektorií tělesné hmotnosti a BMI u 17 pacientů s těmito mutacemi v průběhu léčby setmelanotidem po dobu 1 roku. U pacientů s deficitem POMC a LEPR bylo po léčbě setmelanotidem prokázáno významné zlepšení kvality života, které souviselo jak s příznivým ovlivněním hladu, tak s významnou redukcí hmotnosti (28).
Nadějné jsou výsledky s léčbou setmelanotidem u Bardetova-Biedlova syndromu (BBS), u nějž po ročním podávání významně pokleslo skóre hladu a tělesná hmotnost se snížila o 16,3 % (16). Příznivé ovlivnění tělesné hmotnosti setmelanotidem bylo potvrzeno i v nedávno publikované multicentrické, randomizované, dvojitě zaslepené a placebem kontrolované studii, do níž bylo zařazeno 32 pacientů s BBS (15). Méně přesvědčivé byly výsledky u šesti pacientů, u nichž byl diagnostikován Alströmův syndrom (15). Setmelanotid se podává formou každodenní podkožní injekce.
Mezi nejčastější nežádoucí účinky patří reakce v místě vpichu a kožní hyperpigmentace. Bariérou v léčbě setmelanotidem je bezpochyby velmi vysoká cena přípravku. Jelikož se jedná o léčbu velmi vzácných onemocnění (orphan diseases), bude třeba řešit indikaci a úhradu léčby individuálně. V České republice je třeba nejdříve zajistit včasnou detekci pacientů s těmito vzácnými těžkými hereditárními obezitami, které vznikají v raném dětství, a to obvykle v období do věku 5 let.
Table 1. Ovlivnění tělesné hmotnosti a obvodu pasu podáváním tirzepatidu v dávce 5, 10 a 15 mg jednou týdně vs. placeba po dobu 72 týdnů (podle Jastreboff AM et al. N Engl J Med 2022; 387(3): 205–216). 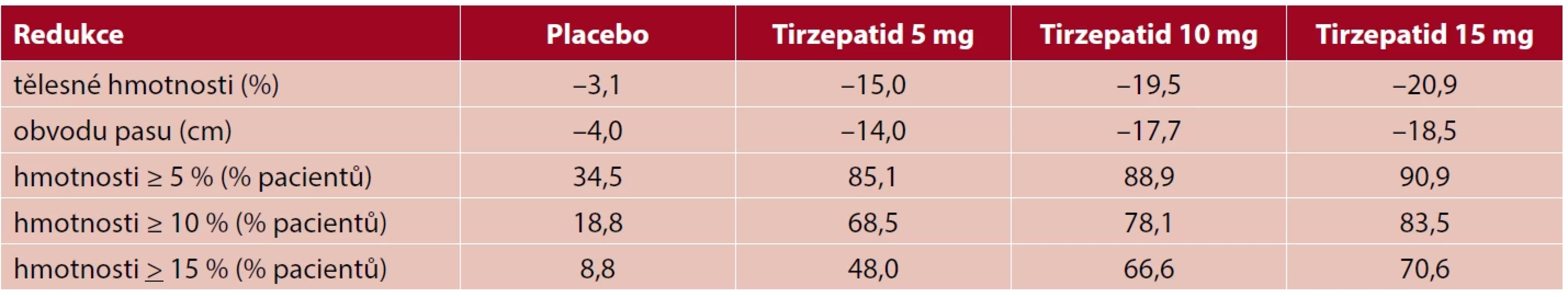
ZÁVĚR
Analoga gastrointestinálních hormonů podávaná jako monoterapie či v kombinaci představují jak z hlediska účinnosti, tak bezpečnosti novou generaci antiobezitik. Navozují významnou redukci tělesné hmotnosti a kardiometabolických rizik. Jimi docílená redukce hmotnosti je, zejména po kombinovaných preparátech, srovnatelná s účinností méně invazivních výkonů bariatrické chirurgie. Nežádoucí účinky se obvykle projevují lehčími gastrointestinálními příznaky, které obvykle během léčby ustupují. Nevýhodou je u většiny těchto nových preparátů nutnost injekční aplikace formou podkožní injekce, i když jen jednou za týden. Dostupnost těchto antiobezitik pro pacienty však výrazně limituje i jejich vysoká cena. Příslibem do budoucna by mohla být analoga hormonů GIT nepeptidického charakteru, která by umožňovala perorální aplikaci bez obav z ovlivnění vstřebávání současným příjmem potravy a tekutin, přičemž by zároveň představovala levnější výrobu a následně i cenu oproti peptidům.
Agonista melanokortinového receptoru 4 setmelanotid se uplatní jednak v léčbě některých velmi vzácných monogenních onemocnění, která jsou důsledkem poruchy melanokortinové signalizace a manifestují se těžkou obezitou v raném dětství, jednak v léčbě rovněž velmi vzácně se vyskytujícího Bardetova-Biedlova syndromu.
Předpokladem úspěšného uplatnění nových antiobezitik v klinické praxi je jejich adekvátní indikace respektující jak mechanismus působení léku a jeho nežádoucí účinky, tak specificitu jednotlivých pacientů s ohledem na věk, přítomnost komorbidit, léčebné preference a mnohdy geneticky determinovanou iniciální odpověď na léčbu. Garantem úspěšné farmakoterapie obezity by měli být adekvátně vyškolení lékaři.
Seznam použitých zkratek
BBS Bardet-Biedlův syndrom
BMI index tělesné hmotnosti (Body Mass Index) DM2 diabetes mellitus 2. typu
EMA European Medicines Agency FDA Federal Drug Administration
GIP inzulinotropní peptid závislý na glukóze (glucose-dependent insulinotropic peptide)
GIT gastrointestinální trakt
GLP-1 glukagonu podobný peptid-1 (glucagon-like peptide-1)
LEPR leptinový receptor
MC4R melanokortinový receptor 4
PCSK1 proprotein konvertáza subtilisin/kexin typu 1 POMC proopiomelanokortinKonflikt zájmů: žádný.
adresa pro korespondenci:
doc. MUDr. Vojtěch Hainer, CSc.
Endokrinologický ústav
Centrum pro diagnostiku a léčbu obezity
Národní 8, 110 00 Praha 1
e-mail: vhainer@endo.cz
Sources
- Ahmann AJ, Capehorn M, Charpentier G, et al. Efficacy and safety of once-weekly semaglutide versus exenatide ER in subjects with type 2 diabetes (SUSTAIN 3): a 56-week, open-label randomized clinical trial. Diabetes Care 2018; 41(2): 258–266.
- Ahrén B, Masmiquel L, Kumar H, et al. Efficacy and safety of once-weekly semaglutide versus once-daily sitagliptin as an add-on to metformin, thiazolidinediones, or both, in patients with type 2 diabetes (SUSTAIN 2): a 56-week, double blind, phase 3a trial. Lancet Diabetes Endocrinol. 2017; 5(5): 341–354.
- Aldhoon-Hainerová I. Obezita v dětství a dospívání. Geneticky podmíněná obezita. In: Hainer V, a kol. Základy klinické obezitologie. 3., zcela přepracované a doplněné vydání. Praha: Grada Publishing 2022; 432–435.
- Aroda VR, Bain SC, Cariou B, et al. Efficacy and safety of once-weekly semaglutide versus once-daily insulin glargine as add-on to metformin (with or without sulfonylureas) in insulin-naive patients with type 2 diabetes (SUSTAIN 4): a randomised, open-label, parallel-group, multicentre, multinational, phase 3a trial. Lancet Diabetes Endocrinol. 2017; 5(5): 355–366.
- Clément K, Biebermann H, Farooqi IS, et al. MC4R agonism promotes durable weight loss in patients with leptin receptor deficiency. Nat Med. 2018; 24 : 551–555.
- Davies M, Faerch L, Jeppesen OK. Semaglutide 2,4 mg once a week in adults with overweight or obesity, and type 2 diabetes (STEP 2): a randomised, double-blind, double-dummy, placebo-controlled, phase 3 trial. Lancet Diabetes Endocrinol. 2021; 397 : 971–984.
- Eliaschewitz FG, Canani LH. Advances in GLP-1 treatment: focus on oral semaglutide. Diabetol Metab Syndr 2021; 13(1): 99.
- Farooqi IS, Jebb SA, Langmack G, et al. Effects of recombinant leptin therapy in a child with congenital leptin deficiency. N Engl J Med. 1999; 341 : 879–894.
- Garvey WT, Batterham RL, Bhatta M, et al. Two-year effects of semaglutide in adults with overweight or obesity: the STEP 5 trial. Nat Med. 2022; 28 : 2083–2091.
- Hainer V. Comparative efficiency and safety of pharmacological approaches to the management of obesity. Diabetes Care. 2011; 34 (Suppl 2): S349–S354.
- Hainer V, Haluzík M. Farmakoterapie obezity. In: Hainer V, a kol. Základy klinické obeziotologie. 3., zcela přepracované a doplněné vydání. Praha: Grada Publishing 2022; 341–372.
- Hainer V, Kunešová M, Taxová Braunerová R, AldhoonHainerová I. Duální agonista inkretinových recptorů tirzepatid: nové antidiabetikum je nadějnou perspektivou v léčbě obezity. DMEV. 2022; 25 : 136–140.
- Haluzík M, Müllerová D, Sucharda P, a kol. Farmakoterapie obezity-update 2023. Čas. Lék. čes. 2023; 162 : 19–31.
- Haluzík M. Semaglutid. Remedia. 2019; 29 : 25–31.
- Haqq AM, Chung WK, Dolfuss H, et al. Efficacy and safety of setmelanotide, a melanocortin-4 receptor agonist, in patients with Bardet-Biedl syndrome and Alstrom syndrome: a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial with an open-label period. Lancet Diabetes Endocrinol. 2022; 10 : 859–868.
- Haws R, Brady S, Davis E, et al. Effect of setmelanotide, a melanocortin-4 receptor agonist, on obesity in Bardet-Biedl syndrome. Diabetes Obes Metab. 2020; 22 : 2133–2140.
- Chao AM, Tronieri JS, Amaro A, Wadden TA. Clinical insight on semaglutide for chronic weight management in adults: Patient selection and special consideration. Drug Design Develop Ther. 2022; 16 : 4449–4461.
- Chavda VP, Ajabiya J, Teli D, et al. Tirzepatide, a new era of dual-targeted treatment for diabetes and obesity: A mini-review. Molecules. 2022; 27 : 4315.
- Jastreboff AM, Aronne LJ, Ahmad NN, et al. Tirzepatide once weekly for the treatment of obesity. N Engl J Med. 2022; 387(3): 205–216.
- Jastreboff AM, Kaplan LM, Frías JP, et al. Triple-hormonereceptor agonist retatrutide for obesity – A phase 2 trial. N Engl J Med. 2023; 389(6): 514–526.
- Jendle J, Birkenfeld AL, Polonsky WH, et al. Improved treatment satisfaction in patients with type 2 diabetes treated with once-weekly semaglutide in the SUSTAIN trials. Diabetes Obes Metab. 2019; 21 : 2315–2326.
- Jeon E, Lee KY, Kim K-K. Approved anti-obesity medications in 2022 KSSO guidelines and promise of phase 3 clinical trials: Anti-obesity drugs in the sky and on the horizon. J Obes Metab Syndr. 2023; 32 : 106–120.
- Karagiannis T, Avgerinos I, Liakos A, et al. Management of type 2 diabetes with dual GIP/GLP-1 receptor agonist tirzepatide: a systematic review and meta-analysis. Diabetologia. 2022; 65 : 1251–1261.
- Knop FK, Aroda VR, de Vale RD, et al. Oral semaglutide 50 mg taken once per day in adults with overweight or obesity (OASIS 1): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2023; 402(10403): 705–719.
- Kunešová M, Müllerová D, Hainer V. Epidemiologie a zdravotní rizika obezity. In: Hainer V, a kol. Základy klinické obezitologie. 3., zcela přepracované a doplněné vydání. Praha: Grada Publishing 2022; 19–43.
- Kushner RF, Calanna S, Davies M, et al. Semaglutide 2,4 mg for the treatment of obesity: Key elements of the STEP trials 1 to 5. Obesity. 2020; 28 : 1050–1061.
- Kühnen P, Clément K, Wiegand S, et al. Proopiomelanocortin deficiency treated with a melanocortin-4 receptor agonist. N Eng J Med. 2016; 375 : 240–246.
- Kühnen P, Wabitsch M, von Schnurbein J, et al. Quality of life outcomes in two phase 3 trials of setmelanotide in patients with obesity due to LEPR or POMC deficiency. Orphanet J Rare Dis. 2022; 17(1): 38.
- Marso SP, Bain SC, Consoli A, et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med. 2016; 375 : 1834–1844.
- Murvelashvili N, Xie L, Schellinger JN, et al. Effectiveness of semaglutide versus liraglutide for treating post-metabolic and bariatric surgery weight recurrence. Obesity (Silver Spring). 2023; 31 : 1280–1289.
- Nauck MA, D´Alessio DA. Tirzepatide, a dual GIP/GLP-1 receptor co-agonist for the treatment of type 2 diabetes with unmatched effectiveness regarding glycaemic control and body weight reduction. Cardiovasc Diabetol. 2022; 21 : 169.
- Pratley RE, Aroda VR, Lingvay I, et al. Semaglutide versus dulaglutide once weekly in patients with type 2 diabetes (SUSTAIN 7): a randomised, open-label phase 3b trial. Lancet Diabetes Endocrinol. 2018; 6 : 275–286.
- Rodbard HW, Lingvay I, Reed J, et al. Semaglutide added to basal insulin in type 2 diabetes (SUSTAIN 5): a randomized, controlled trial. J Clin Endocrinol Metab. 2018; 103 : 2291–2301.
- Rubino D, Abrahamsson N, Davies M, et al. Effect of continued weekly subcutaneous semaglutide vs. placebo on weight loss maintenance in adults with overweight or obesity: The STEP 4 randomized clinical trial. JAMA. 2021; 325 : 1414–1425.
- Ryan DH, Lingvay I, Colhoun HM, et al. Semaglutide effects on cardiovascular outcomes in people with overweight or obesity (SELECT) rationale and design. Am Heart J. 2020; 229 : 61–69.
- Seyd YY. Tirzepatide: First approval. Drugs. 2022; 82 : 1213–1220.
- Singh G, Krauthamer M, Bjalme-Evans M. Wegovy (semaglutide): a new weight loss drug for chronic weight management. J Invest Med. 2022; 70 : 5–13.
- Sorli S, Harashima SI, Tsoukas GM, et al. Efficacy and safety of once-weekly semaglutide monotherpy versus placebo in patients with type 2 diabetes (SUSTAIN 1) a double-blind, randomised, multicentre phase 3a trial. Lancet Diabetes Endocrinol. 2017; 5 : 251–260.
- Wabitsch M, Farooqi S, Flück CE, et al. Natural history of obesity due to POMC, PCSK1, and LEPR deficiency and the impact of setmelanotide. J Endocr Soc. 2022; 6 : 1–9.
- Wadden TA, Tronieri JS, Butryn ML. Lifestyle modification approaches for the treatment of obesity. Am Psychol. 2020; 75 : 235–251.
- Wadden TA, Bailey TS, Billings LK, et al. Effect of subcutaneous semaglutide vs. placebo as an adjunct to intensive behavioral therapy on body weight in adults with overweight or obesity The STEP3 randomized clinical trial. JAMA. 2021; 325 : 1403–1413.
- Weghuber D, Barrett T, Barrientos-Pérez M, et al. Once-weekly semaglutide in adolescents with obesity. N Engl J Med. 2022; 387 : 2245–2257.
- Wharton S, Blevins T, Connery L, et al. Daily oral GLP-1 receptor agonist orforglipron for adults with obesity. N Engl J Med. 2023 Jun 23. doi: 10.1056/NEJMoa2302392 [Online ahead of print].
- Wilding JPH, Batterham RL, Calanna S, et al. Once-weekly semaglutide in adults with overweight or obesity. N Engl J Med. 2021; 384 : 989–1002.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2023 Issue 4-
All articles in this issue
- Nové obzory ve farmakoterapii obezity
- Složky potravin s předpokládaným ochranným účinkem proti nádorovým onemocněním
- Odhad glomerulární filtrace ze sérového kreatininu u dětí
- Armeo Spring zlepšuje kvalitu pohybu i života po iktu
- Životní styl dětí s onkologickým onemocněním v období remise a jejich zdravých vrstevníků
- Změny v prevalenci obezity českých adolescentů mezi lety 2018 a 2022 a její současné koreláty: HBSC studie
- Kvalita života u mladé pacientky po ischemické cévní mozkové příhodě: interpretativní fenomenologická analýza
- Alkohol a osteoporóza: důsledky pro praxi
- 65. Purkyňův den v Libochovicích
- Význam přesné diagnostiky a klasifikace cholangiokarcinomu (EURO-CHOLANGIO-NET konference, Sapienza University of Rome, 8. až 9. června 2023)
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nové obzory ve farmakoterapii obezity
- Odhad glomerulární filtrace ze sérového kreatininu u dětí
- Armeo Spring zlepšuje kvalitu pohybu i života po iktu
- Kvalita života u mladé pacientky po ischemické cévní mozkové příhodě: interpretativní fenomenologická analýza
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

