-
Medical journals
- Career
Aktuální výsledky screeningu kolorektálního karcinomu v České republice a potenciální význam kolonické kapslové endoskopie
Authors: O. Ngo 1,2; R. Chloupková 1,2; Suchánek Š. 3; Zavoral M. 3; Dušek L. 1,2; O. Májek 1,2
Authors‘ workplace: Ústav zdravotnických informací a statistiky ČR, Praha 1; Institut biostatistiky a analýz, LF MU, Brno 2; Interní klinika 1. LF UK a ÚVN – VFN Praha 3
Published in: Gastroent Hepatol 2019; 73(5): 387-391
Category: Gastrointestinal Oncology: Original Article
doi: https://doi.org/10.14735/amgh2019387Overview
Východiska: Česká republika patří v mezinárodním srovnání mezi zatíženější země v incidenci a mortalitě kolorektálního karcinomu. Důležitou součástí prevence je screeningový program, který je v ČR již dlouhodobě zaveden. Pro zajištění vysoké kvality je nutný průběžný monitoring celého screeningového procesu. Cílem sdělení je vyhodnotit výkonnostní charakteristiky screeningu ve vztahu k možnému přínosu kolonické kapslové endoskopie.
Materiál a metody: K hodnocení byla využita data zdravotních pojišťoven a klinická data o provedených preventivních koloskopiích do roku 2018. Hodnoceny byly indikátory výkonnosti související s cíli sdělení (pozitivita testu na okultní krvácení do stolice (TOKS), pozitivní prediktivní hodnota TOKS a čekací doba na koloskopii po pozitivním testu).
Výsledky: Od roku 2014 došlo díky adresnému zvaní k výraznému navýšení počtu provedených preventivních koloskopií. Pozitivita TOKS dosahuje v posledních letech okolo 6–7 % a vzhledem k relativně nízké pozitivní prediktivní hodnotě TOKS pro adenomy (přibližně 40 %) byl zaznamenán nezanedbatelný podíl falešně pozitivních výsledků, což může indikovat nadbytečné koloskopie a nadměrně zatěžovat screeningová centra. Současně došlo ke zřetelnému nárůstu čekací doby na následnou koloskopii po pozitivním výsledku testu.
Závěr: Při hodnocení výkonnostních charakteristik provedených TOKS a následných koloskopií je patrný problém v relativně nízké pozitivní prediktivní hodnotě TOKS. Potenciální příspěvek ke snížení zátěže center může představovat kolonická kapslová endoskopie, která by se mohla uplatňovat jako „filtrový“ test u jedinců s pozitivním TOKS.
Klíčová slova:
kolorektální karcinom – plošný screening – indikátory výkonnosti – koloskopie – kolonická kapslová endoskopie
Úvod
Zhoubný nádor tlustého střeva a konečníku (KRK – kolorektální karcinom) se řadí mezi vážná onkologická onemocnění a tuto skutečnost dokládají aktuálně dostupné statistiky Mezinárodní agentury pro výzkum rakoviny (IARC – International Agency for Research on Cancer), dle kterých je KRK světově jedna z nejčastěji diagnostikovaných malignit a současně jedna z nejčastějších příčin úmrtí mezi onkologickými onemocněními. ČR již není v mezinárodním srovnání na nejvyšších příčkách ve výskytu (incidenci) a úmrtnosti (mortalitě) KRK, ale přesto stále patří mezi zatíženější země tímto onemocněním [1]. Dle dostupných dat Národního onkologického registru ČR (NOR) byla sledována v roce 2017 incidence tohoto onemocnění 70,9 nových případů na 100 tisíc osob (okolo 8 tisíc nových případů ročně), téměř polovina počtu nemocných na tento zhoubný nádor (ZN) každoročně umírá (35,1 úmrtí na 100 tisíc osob – více než 3,5 tisíce úmrtí na dané onemocnění ročně) [2].
Klíčovou roli v prevenci KRK představuje screeningový program, který má za cíl detekovat prekancerózní léze a časná klinická stadia KRK, a v konečném důsledku tedy snižovat populační zátěž tohoto onemocnění [3,4]. Screening KRK patří mezi tři programy časného záchytu ZN, které jsou doporučeny Radou Evropské unie [5]. Tato doporučení byla akceptována v řadě evropských zemí, které zavádí Národní programy screeningu KKR. V roce 2015 byl ve 20 z 28 členských států Evropské unie zaveden populační screening a další tři země jej implementovaly v roce 2016 [6,7].
V ČR byl v roce 2000 oficiálně zahájen Národní program screeningu kolorektálního karcinomu pro osoby od 50 let věku. Těmto osobám je zpravidla nabízen test na okultní krvácení do stolice (TOKS) následovaný koloskopií v případě pozitivity testu a osoby od 55 let mají možnost volby, a to buď pokračovat ve vyšetřování TOKS, nebo si zvolit přímo screeningovou koloskopii [8]. Využívání TOKS je v souladu s běžnou praxí většiny zavedených screeningových programů v Evropě. Dle nejnovějších vědeckých důkazů je preferována kvantitativní imunochemická forma testů. Nespornou výhodou této formy testu oproti guajakovým TOKS je diagnostická přesnost [9,10], která má však dopad i na kapacitní zátěž (z důvodu zvýšeného podílu pozitivních výsledků) zapojených screeningových center, která provádí preventivní koloskopie. ČR disponuje komplexní sítí specializovaných pracovišť, která provádí preventivní koloskopie [11]. Předpokladem úspěšné organizace programu je vysoká úroveň zapojení občanů do screeningu [12]. Jedním z opatření ke zvýšení participace na screeningu bylo zavedení adresného zvaní osob ve věku 50–70 let formou dopisu počátkem roku 2014 [13,14].
Pro zajištění odpovídající výkonnosti screeningového programu je nezbytný průběžný monitoring celého screeningového procesu prostřednictvím tzv. sady indikátorů výkonnosti definovaných v evropských doporučeních vydaných Evropskou komisí ve spolupráci s IARC [15]. Cílem sdělení je prezentovat aktuální výsledky Národního programu screeningu kolorektálního karcinomu v ČR s ohledem na možný význam kolonické kapslové endoskopie a dále zejména diskutovat využití tohoto vyšetření jako „filtrového“ testu u osob s pozitivním TOKS.
Materiál a metody
V souladu s evropskými doporučeními je v ČR vybudován systém informační podpory, který má sbírat a uchovávat data a pravidelně monitorovat výkonnost onkologických screeningových programů prostřednictvím zmíněných indikátorů. Uvedený informační systém představuje zejména tři datové zdroje – data plátců zdravotní péče, Národní registr kolorektálního screeningu (klinická data provedených preventivních vyšetření ve screeningových centrech) a NOR. V souvislosti s cíli sdělení bude hodnocen vývoj pozitivity provedených TOKS (podíl pozitivních výsledků testu mezi všemi adekvátně testovanými osobami) z dat plátců zdravotní péče a následné koloskopie po pozitivním výsledku testu na podkladech klinických dat z registru (zejména počty vyšetření, detekční míra kolorektálních lézí u screeningové koloskopie a detekce lézí u koloskopie po pozitivním testu, resp. pozitivní prediktivní hodnota TOKS). Tyto údaje budou doplněny z klinických dat o indikátor monitorující průměrnou čekací dobu na navazující koloskopii po pozitivním testu. Zmíněné ukazatele byly hodnoceny do roku 2018 prostřednictvím metod deskriptivní statistiky a veškeré statistické výpočty byly provedeny v softwarovém nástroji IBM SPSS Statistics 25.
Výsledky
V ČR je v posledních letech prováděno u osob ve věku od 50 let okolo 650 tisíc screeningových TOKS ročně. Na grafu 1 je hodnocen vývoj pozitivity TOKS, která dosahovala v předchozím období více než 7 %. V posledních 2 letech došlo k jejímu poklesu.
Graph 1. Vývoj pozitivity TOKS v čase.
Graph 1. Development of faecal occult blood test positivity over time.
V tab. 1 jsou uvedeny počty provedených preventivních koloskopií v jednotlivých letech dle indikace (screeningová a následná koloskopie po pozitivním testu – TOKS + koloskopie) spolu s podíly nalezených kolorektálních lézí (adenom, pokročilý adenom, karcinom). Od roku 2014 lze sledovat výrazné navýšení počtu provedených preventivních koloskopií. U TOKS + koloskopií došlo ovšem v posledních 2 letech ke znatelnému poklesu počtu provedených vyšetření. Podíl nalezených kolorektální lézí je přirozeně vyšší u TOKS + koloskopií – zastoupení adenomů, resp. pokročilých adenomů v čase roste a v posledních letech dosahuje okolo 45, resp. 21 %. V rámci screeningových koloskopií, které spíše reflektují přirozenou incidenci kolorektálních lézí v populaci, mírně roste zastoupení adenomů, podíl karcinomů zůstává v čase neměnný. V souhrnu bylo provedeno od roku 2006 více než 300 tisíc preventivních koloskopií (z většiny TOKS + koloskopie) a přibližně v 36 % byl nalezen během koloskopie alespoň jeden adenom, v 16 % pokročilý adenom a ve 3 % karcinom.
Table 1. Detekce kolorektálních lézí u preventivních koloskopií dle indikace.
Tab. 1. Detection of colorectal lesions in preventive colonoscopy by indication.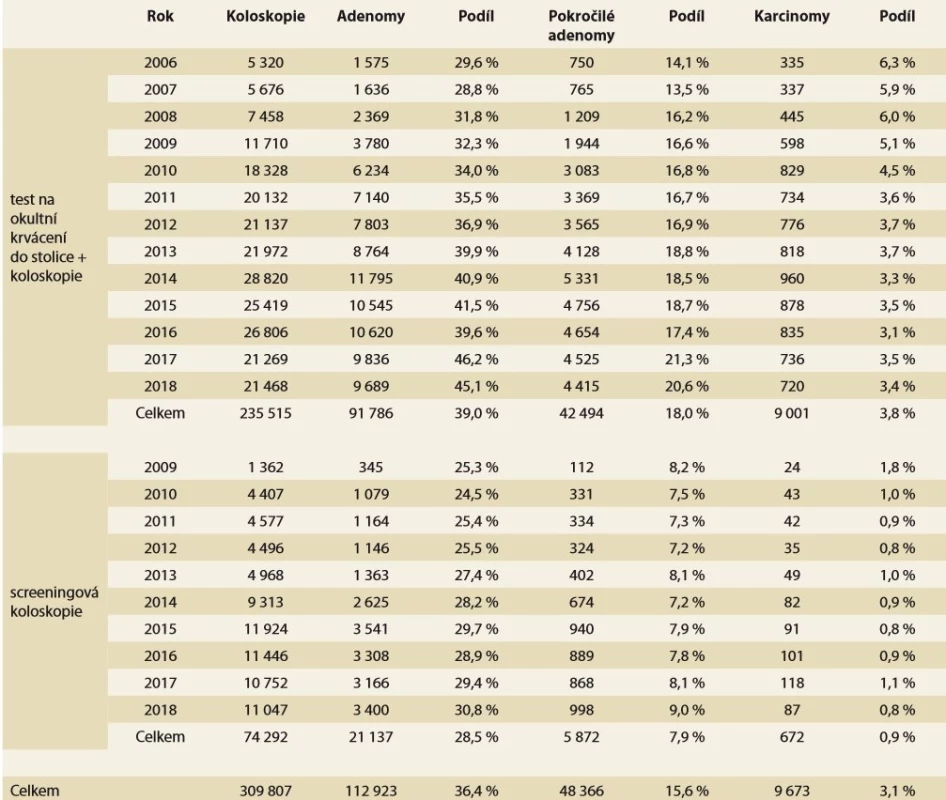
Z tab. 2 lze vidět průměrnou čekací dobu na koloskopii po pozitivním TOKS, která od roku 2006 mírně roste (výrazněji od roku 2014) a v posledních letech se stabilizovala a dosahuje okolo 1,6 měsíce.
Table 2. Průměrná čekací doba na koloskopie po pozitivním testu v čase.
Tab.2. Mean waiting time for colonoscopy after positive test over time.
*Je ukládáno pouze orientační datum (měsíc a rok) provedení TOKS. Čekací doba je tedy hodnocena v celých měsících: 0 (kolonoskopie ve stejném měsíci), 1 (kolonoskopie v následujícím měsíci), atd.
Do počtu TOKS + koloskopií byly zahrnuty pouze záznamy s čekací dobou kratší 18 měsíců.
TOKS - test na okultní krvácení do stoliceDiskuze
V ČR sledujeme z dat NOR díky preventivním opatřením v poslední době podstatné zlepšení vývoje populační zátěže KRK. Tento pozitivní vývoj byl také potvrzen v nezávislé mezinárodní studii OECD, kde byl v ČR sledován nejvyšší pokles mortality KRK v rámci všech evropských zemí [16]. Přesto je stále pozorovatelný vysoký podíl pokročilých nádorů (okolo 50 % pacientů v klinickém stadiu III a vyšším) [17]. Je tedy nezbytné stále zvyšovat informovanost a zájem cílové populace k účasti ve screeningovém programu [12]. Velmi podstatný je průběžný monitoring celého screeningového procesu prostřednictvím výše zmíněných indikátorů výkonnosti pro odhalení případných dílčích rezerv programu, a to nejen na straně primární péče a testování TOKS, ale rovněž z pohledu preventivních koloskopií, které zaujímají ve screeningovém procesu klíčovou roli nástroje pro definitivní stanovení diagnózy a případnou terapii kolorektální neoplazie.
Vzhledem k cílům příspěvku byly hodnoceny rezervy zejména v diagnostické přesnosti používaných TOKS v ČR ve vztahu k provedeným preventivním koloskopiím. Počty screeningových vyšetření obecně výrazně vzrostly od roku 2014 díky adresnému zvaní osob ke screeningu a v kombinaci s relativně vysokou pozitivitou TOKS bylo provedeno mnohem větší množství preventivních koloskopií. Navíc relativně nízká detekce adenomových polypů u TOKS + koloskopií svědčí (vedle potenciálních rezerv v senzitivitě koloskopických vyšetření) o nezanedbatelném podílu falešně pozitivních výsledků TOKS, které mohou mít za následek nadbytečné koloskopie a v důsledku toho nadměrně zatěžují screeningová centra a snižují jejich kapacitu pro vyšší pokrytí populace koloskopickým screeningem. V souvislosti se zvýšenými objemy vyšetření došlo od roku 2014 k výraznému nárůstu průměrné čekací doby na koloskopii po pozitivním TOKS. V posledních 2 letech lze ovšem sledovat snížení pozitivity TOKS, potenciálně v důsledku zavádění kvantitativních imunochemických forem testu s vyšší specificitou, což má za následek znatelné snížení počtu provedených TOKS + koloskopií (a lepší detekci adenomů) a do jisté míry i dopad na snížení a stabilizaci průměrné čekací doby. Přesto ale zůstává vysoký podíl vyšetřených osob s falešně pozitivním výsledkem TOKS, a tedy i prodloužená čekací doba na koloskopii.
Je tedy velmi žádoucí nacházet a také implementovat efektivní cesty pro nastavení optimální screeningové strategie [18]. Potenciální strategií pro optimalizaci zátěže screeningových center je provedení kolonické kapslové endoskopie po pozitivním výsledku testu pro předvýběr osob vhodných k návštěvě na navazující koloskopii. Dostupné studie ukazují, že se jedná o screeningovou metodu se slibnými diagnostickými charakteristikami [19–21]. V ČR již probíhá od roku 2016 prospektivní multicentrická studie, která hodnotí diagnostické ukazatele provedených kolonických kapslových endoskopií u osob po pozitivním imunochemickém testu. Tato studie také prokazuje velmi dobré výsledky v detekci kolorektálních lézí a zejména vysokou negativní prediktivní hodnotu (88 % pro polypy ≥ 6 mm a 93 % pro polypy ≥ 10 mm), a prokazuje tak potenciál kolonické kapsle stát se možným „filtrovým“ testem u osob s pozitivním fekálním imunochemickým testem a zamezit zbytečnému provádění následných koloskopií v případě falešně pozitivního výsledku TOKS. V rámci české studie je navíc srovnáno čtení lékaře a sestry a dle předběžných výsledků jsou zaškolené endoskopické sestry schopny adekvátně vyhodnotit provedené vyšetření [22].
Závěr
Dlouhodobě zavedená opatření pro sekundární prevenci KRK se příznivě projevují na populační úrovni. Přesto lze ve screeningovém procesu a jeho výsledcích identifikovat rezervy. Při hodnocení provedených TOKS a následných koloskopií je patrným problémem relativně nízká prediktivní hodnota TOKS (detekce adenomů u TOKS + koloskopie), která s sebou nese řadu falešně pozitivních výsledků, které v konečném důsledku zatěžují screeningová centra a způsobují prodlužující se čekací dobu na koloskopii po pozitivním výsledku testu. Řešením snížení zátěže center může být kolonická kapslová endoskopie, která je dobře akceptovatelnou metodou a má potenciál v uplatnění jako „filtrový“ test u jedinců s pozitivním TOKS.
Doručeno/Submitted: 7. 10. 2019
Přijato/Accepted: 14. 10. 2019
RNDr. Ondřej Májek, Ph.D.
Institut biostatistiky a analýz LF MU
Kamenice 126/3 625 00 Brno
Sources
1. Ferlay J, Ervik M, Lam F et al. Global cancer observatory: cancer today. [online]. Available from: https: //gco.iarc.fr/today.
2. Dušek L, Mužík J, Kubásek M et al. Epidemiologie zhoubných nádorů v České republice. [online]. Available from: http: //www.svod.cz.
3. Kim PJ, Plescia J, Clevers H et al. Survivin and molecular pathogenesis of colorectal cancer. Lancet 2003; 362 (9379): 205–209. doi: 10.1016/S0140-6736 (03) 13910-4.
4. Stewart BW, Wild C (eds). World Cancer report 2014. Lyon: International Agency for Research on Cancer 2014.
5. Official Journal of the European Union 2003. European Council. Council Recommendation of 2 December 2003 on cancer screening. [online]. Available from: http: //eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri= OJ: L: 2003 : 327 : 0034 : 0038: EN: PDF.
6. Zavoral M, Suchanek S, Zavada F et al. Colorectal cancer screening in Europe. World J Gastroenterol 2009; 15 (47): 5907–5915. 10.3748/ wjg.15.5907.
7. Ponti A, Anttila A, Ronco G. Cancer screening in the European Union (2017). Report of the implementation of the council Recommendation on cancer screening. Inernational Agency for Research on Cancer 2017. [online]. Available from: https: //screening.iarc.fr/EUreport.php.
8. Suchanek S, Majek O, Vojtechova G et al. Colorectal cancer prevention in the Czech Republic: time trends in performance indicators and current situation after 10 years of screening. Eur J Cancer Prev 2014; 23 (1): 18–26. doi: 10.1097/CEJ.0b013e328364f203.
9. van Rossum LG, van Rijn AF, Laheij RJ et al. Random comparison of guaiac and immunochemical fecal occult blood tests for colorectal cancer in a screening population. Gastroenterology 2008; 135 (1): 82–90. doi: 10.1053/j.gastro.2008.03.040.
10. Grega T, Májek O, Ngo O et al. Současné principy screeningu kolorektálního karcinomu – od oportunního k populačnímu screeningovému programu. Gastroent Hepatol 2016; 70 (5): 383–392. doi: 10.14735/amgh2016 383.
11. Zavoral M, Vojtěchová G, Májek O et al. Population colorectal cancer screening in the Czech Republic. Cas Lek Cesk 2016; 155 (1): 7–12.
12. Ngo O, Bučková B, Suchánek Š et al. Účast české populace na screeningu kolorektálního karcinomu – vývoj a aktuální stav. Gastroent Hepatol 2017; 71 (5): 377–383. doi: 10.14735/amgh2017377.
13. Dušek L, Májek O, Blaha M et al. Koncepce populačního screeningu v České republice, metodika a první výsledky adresného zvaní občanů do preventivních onkologických programů. Klin Onkol 2014; 27 (Suppl 2): 2S59–2S68. doi: 10.14735/amko20142S59.
14. Ngo O, Chloupková R, Ambrožová M et al. Evaluation of the personalized invitation of Czech citizens to screening programs. Časopis Lékařů Čes 2019; 158 (3–4): 147–150.
15. Segnan N, Patnick J, L von Karsa (eds). European guidelines for quality assurance in colorectal cancer screening and diagnosis. 1st ed. Luxembourg: Publications Office ot the European Union 2010.
16. OECD. Survival and mortality for colorectal cancer. In: Health at a Glance 2013. [online]. Available from: https: //www.oecd.org/els/health-systems/Health-at-a-Glance-2013.pdf.
17. Dušek L, Májek O, Mužík J et al. Epidemiologie a populační screening nádorů tlustého střeva a konečníku v ČR na podkladě nově dostupných dat. Gastroent Hepatol 2015; 69 (6): 509–517. doi: 10.14735/amgh2015 509.
18. Zavoral M, Suchanek S, Majek O et al. Colorectal cancer screening: 20 years of development and recent progress. World J Gastroenterol 2014; 20 (14): 3825–3834. doi: 10.3748/wjg.v20.i14.3825.
19. Kobaek-Larsen M, Kroijer R, Dyrvig AK et al. Back-to-back colon capsule endoscopy and optical colonoscopy in colorectal cancer screening individuals. Colorectal Dis 2018; 20 (6): 479–485. doi: 10.1111/codi.13965.
20. Holleran G, Leen R, O’Morain C et al. Colon capsule endoscopy as possible filter test for colonoscopy selection in a screening population with positive fecal immunology. Endoscopy 2014; 46 (6): 473–478. doi: 10.1055/s-0034-1365 402.
21. Rex DK, Adler SN, Aisenberg J et al. Accuracy of capsule colonoscopy in detecting colorectal polyps in a screening population. Gastroenterology 2015; 148 (5): 948–957. doi: 10.1053/j.gastro.2015.01.025.
22. Voška M, Grega T, Vojtěchová G et al. Porovnání účinnosti kolonické kapslové endoskopie a optické koloskopie u osob s pozitivním imunochemickým testem na okultní krvácení do stolice – multicentrická, prospektivní studie. Gastroenterol Hepatol 2018; 72 (4): 298–303. doi: 10.14735/amgh2018298.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery Clinical oncology
Article was published inGastroenterology and Hepatology
2019 Issue 5-
All articles in this issue
- Sekundární prevence kolorektálního karcinomu v České republice
- Gastrointestinální onkologie
- Doporučené postupy České gastroenterologické společnosti ČLS JEP pro kapslovou endoskopii
- Aktuální výsledky screeningu kolorektálního karcinomu v České republice a potenciální význam kolonické kapslové endoskopie
- Střevní příprava před koloskopií – existuje optimální příprava?
- Porovnání účinnosti kolonické kapslové endoskopie a optické koloskopie u osob s pozitivním imunochemickým testem na okultní krvácení do stolice – multicentrická, prospektivní studie
- Vliv současné léčby na populační data dlouhodobého přežívání nemocných s karcinomem pankreatu
- Divertikulární choroba tlustého střeva – nový pohled na klasifikaci a léčbu
- Mikrobiota v etiopatogenéze a liečbe symptomatickej divertikulovej choroby hrubého čreva
- Nutriční diety u gastroenterologických nemocných vyššího věku s chronickým onemocněním ledvin
- Díl V. – Příčiny úmrtí pacientů s idiopatickými střevními záněty a související časové trendy
- XXXIII. Hildebrandove bardejovské gastroenterologické dni
- Opustil nás profesor Meinhard Classen
- Výběr z mezinárodních časopisů
- Kvíz z klinické praxe
- Správná odpověď na kvíz
- Kreditovaný autodidaktický test: Gastrointestinální onkologie
- Asacol 1,6 g využívá nový technologický koncept OPTICORE™
- Papilárny adenokarcinóm žalúdka
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Střevní příprava před koloskopií – existuje optimální příprava?
- Divertikulární choroba tlustého střeva – nový pohled na klasifikaci a léčbu
- Doporučené postupy České gastroenterologické společnosti ČLS JEP pro kapslovou endoskopii
- Aktuální výsledky screeningu kolorektálního karcinomu v České republice a potenciální význam kolonické kapslové endoskopie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

