-
Medical journals
- Career
Porovnání nákladové efektivity okamžitě zahájené léčby oproti odložené terapii chronické hepatitidy C v České republice
Authors: J. Skoupá 1; P. Urbánek 2
Authors‘ workplace: Czechta Institute, o. p. s., Praha 1; Interní klinika 1. LF UK a ÚVN – VFN Praha 2
Published in: Gastroent Hepatol 2018; 72(1): 58-65
Category: Hepatology: Original Article
doi: https://doi.org/10.14735/amgh201858Overview
Východiska:
Přímo působící antivirotika (DAA – direct-acting antiviral agents) dramaticky zlepšila prognózu pacientů infikovaných virem hepatitidy C (HCV). Limitací jejich širokého použití jsou vysoké náklady. Cílem předložené analýzy je zhodnotit nákladovou efektivitu u dosud neléčených pacientů infikovaných HCV genotypem 1 (GT1), a to okamžitě bez ohledu na stav jaterní fibrózy nebo až při pokročilé jaterní fibróze.Materiál a metody:
Byl adaptován farmakoekonomický model s typickou strukturou pro HCV infekci. Do modelu vstupuje kohorta 10 000 pacientů, která je léčena kombinací ledipasvir/sofosbuvir buď okamžitě (hodnocená kohorta), anebo až při progresi do pokročilé fibrózy/cirhózy (komparativní kohorta). Věk a METAVIR rozložení odpovídá situaci v České republice. V analýze byly uvažovány náklady zdravotní, alternativně i sociální. Data o účinnosti, pravděpodobnosti progrese a kvalitě života byly převzaty z literatury. Výsledky jsou prezentovány jako inkrementální náklady (ICER) na QALY (Quality adjusted life-years). Pro limitaci nejistoty byly provedeny analýzy senzitivity.Výsledky:
V celoživotním časovém horizontu byla okamžitá léčba DAA dominantní (méně nákladná a účinnější) při srovnání s odloženou terapií. Dominance byla jak při úvaze zdravotních (ICER/QALY –4 414 Kč), tak i zdravotních a sociálních nákladů (ICER/QALY –214 948 Kč). Okamžitá léčba zabránila 619 příhodám, zejména hepatocelulárního karcinomu a předčasnému úmrtí. Provedené analýzy senzitivity potvrdily robustnost výsledků.Závěr:
Analýza nákladové efektivity prokázala, že okamžitá léčba nově diagnostikovaných pacientů s HCV GT1 je dominantní v porovnání s odloženou terapií v podmínkách České republiky, a to jak z pohledu zdravotních, tak i zdravotních a sociálních nákladů.Klíčová slova:
nákladová efektivita – infekce virem hepatitidy C – přímo působící antivirotikaÚvod
Léčba chronické infekce virem hepatitidy C (HCV) se v posledních letech dostává do centra zájmu lékařů, pacientů a zdravotních pojišťoven. S dostupností přímo působících antivirotik (DAA – direct-acting antivirals) dramaticky vzrostl podíl vyléčených pacientů. Kritériem vyléčení je trvalá eliminace viru, která brání rozvoji jaterních i mimojaterních komplikací HCV infekce. Eliminací viru je myšleno dosažení setrvalé virologické odpovědi (SVR – sustained virologic response), která je definována negativitou sérové HCV RNA ve 12. týdnu po skončení protivirové léčby [1]. Pro hodnocení jednotlivých stadií jaterní fibrózy se používá systém METAVIR, který byl vyvinut pro histologické hodnocení v dobách, kdy byla jaterní biopsie jedinou metodou umožňující právě hodnocení stadia postižení [2]. V současné době je jaterní biopsie v této indikaci téměř úplně nahrazena neinvazivními metodami hodnocení jaterní fibrózy. I tyto moderní přístupy jsou korelovány se systémem METAVIR, a proto se tato klasifikace používá i nadále a my se jí budeme v následujícím textu držet.
Problém léčby kombinacemi DAA spočívá v tom, že narostly náklady na terapii. Obvyklá cena jednoho léčebného režimu trvajícího 3 měsíce je přibližně 1–1,5 mil. Kč. Aktuální evropské doporučené postupy uvádí, že všichni pacienti s jaterní cirhózou musí být léčeni okamžitě, bez odkladu [3]. Stejně tak je okamžitá terapie vhodná u nemocných se signifikantní fibrózou (METAVIR F ≥ 2), u pacientů s extrahepatální manifestací (např. se symptomatickou vaskulitidou na základě kryoglobulinemie, s nefropatií, non-hodgkinským lymfomem B buněk) a u infikovaných s rizikem rychlé progrese fibrózy (např. po transplantaci jater (LTx – liver transplantation). Byť evropská doporučení jednoznačně uvádí potřebu terapie i u nemocných bez fibrózy (METAVIR F0–F1), nespecifikují její načasování (okamžité či odložené, tj. až při progresi jaterního onemocnění).
Rovněž české doporučené postupy uvádějí prakticky identické indikace k okamžité terapii a přesně nedefinují časovou urgenci zahájení léčby u nemocných bez fibrózy [1].
Publikovaná zahraniční literatura se v poslední době zabývá efektivitou a nákladovou efektivitou okamžité vs. oddálené terapie HCV [4–6].
V ČR bývá terapie u pacientů bez závažné fibrózy oddalována. Často se tak děje z ekonomických důvodů, což je dáno i fixními rozpočty pracovišť. Na základě limitovaných zdrojů jsou tak preferenčně léčeni nemocní s pokročilou jaterní chorobou (F3–F4).
Cíl studie
Cílem předložené studie je zhodnocení nákladové efektivity u pacientů infikovaných HCV genotypem 1 (HCV GT1), kteří dosud nebyli léčeni. Analýza je provedena s ohledem na okamžitou léčbu bez ohledu na METAVIR (F0–F4) vs. oddálenou terapii (F3 a F4), tedy při různém METAVIR skóre.
Materiál a metodika
Pro účely analýzy nákladové efektivity byl adaptován farmakoekonomický Markovův model přechodových stavů vytvořený společností MAPI. Model hodnotí náklady a přínosy léčených pacientů s HCV a fibrózou F0–F4 bez ohledu na pokročilost jaterní fibrózy a porovnává je s kohortou farmakologicky léčených pouze ve stadiu F3 a F4. Použitý model odpovídá svojí strukturou klasickému modelu podle Bennetta et al, který byl rovněž základem pro posuzování nákladové efektivity v ČR v rámci žádostí o stanovení ceny a úhrady (schéma 1) [7]. Do modelu vstupuje kohorta 10 000 pacientů s rozložením METAVIR skóre, které vychází z publikované literatury a přibližně odpovídá i rozložení v ČR (tab. 1) [4]. Kohorta je buď léčena okamžitě bez ohledu na METAVIR (hodnocená intervence), nebo je léčena až po progresi do F3/F4 (komparativní intervence). Pacienti s F0–F2, kteří po léčbě dosáhnou SVR, jsou považováni za vyléčené a jejich jaterní onemocnění již neprogreduje. U malé části nemocných s F3 a F4 je v souladu s literárními údaji uvažována progrese do pokročilejších stadií jaterního onemocnění např. dekompenzované cirhózy a hepatocelulárního karcinomu (HCC – hepatocellular carcinoma) [8]. U většiny ale k progresi nedochází. U nemocných bez léčby (F0–F2) v kontrolním rameni choroba postupně přechází do stadia F3 nebo F4, kdy je již farmakologicky léčena. Po terapii je další vývoj identický jako výše uvedeno, tedy po dosažení SVR u většiny pacientů choroba neprogreduje. Pokud SVR není dosaženo, dochází k rozvoji dekompenzované cirhózy, HCC, případně k LTx. Pravděpodobnosti přechodu mezi jednotlivými stavy (tab. 2) vychází z literatury a byly akceptovány i autoritami v ČR [8–11]. V modelu není předpokládána rekurence HCV (pojem zahrnující pozdní relapsy a reinfekce při nové expozici HCV). V obou ramenech modelu jsou pacienti léčeni fixní kombinací DAA ledipasvir/sofosbuvir, která je v ČR hrazena z veřejných prostředků. Parametry účinnosti léčby (tedy dosažení SVR) vycházejí z literatury, konkrétně ze studií fáze III, které hodnotily účinnost a bezpečnost fixní kombinace ledipasvir/sofosbuvir u dosud neléčených pacientů s HCV GT1 (tab. 1) [12,13]. Délka léčby je 8 týdnů (F0–F1), resp. 12 týdnů (F2–F4). Efekt terapie je vždy vztažen k délce léčby a k METAVIR skóre podle výsledků klinických studií [14].
Table 1. Vstupní parametry a efektivita léčby. Tab. 1. Input parameters and treatment efficiency. 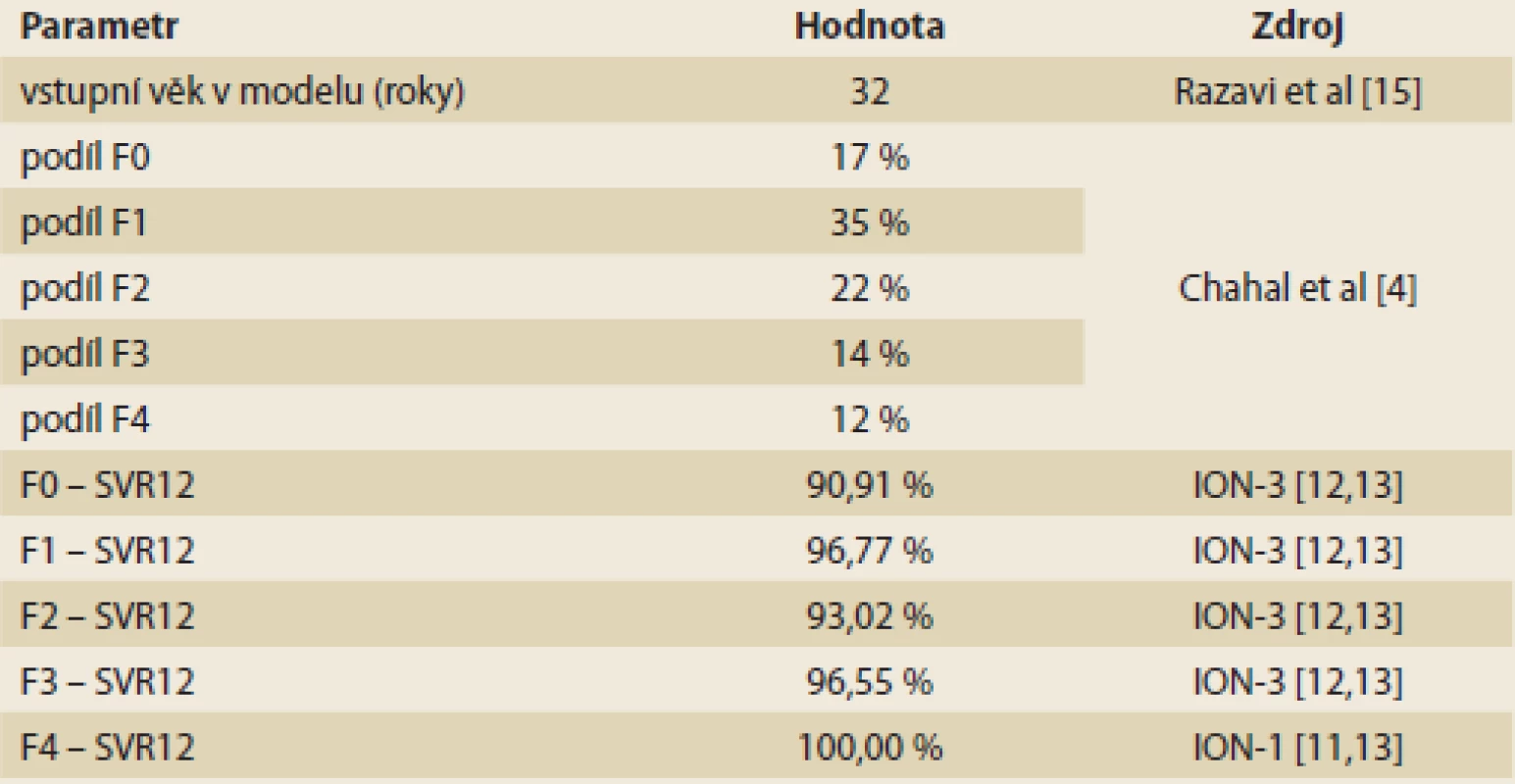
SVR – setrvalá virologická odpověď Table 2. Přechodové pravděpodobnosti v modelu. Tab. 2. Transition probabilities in the model. 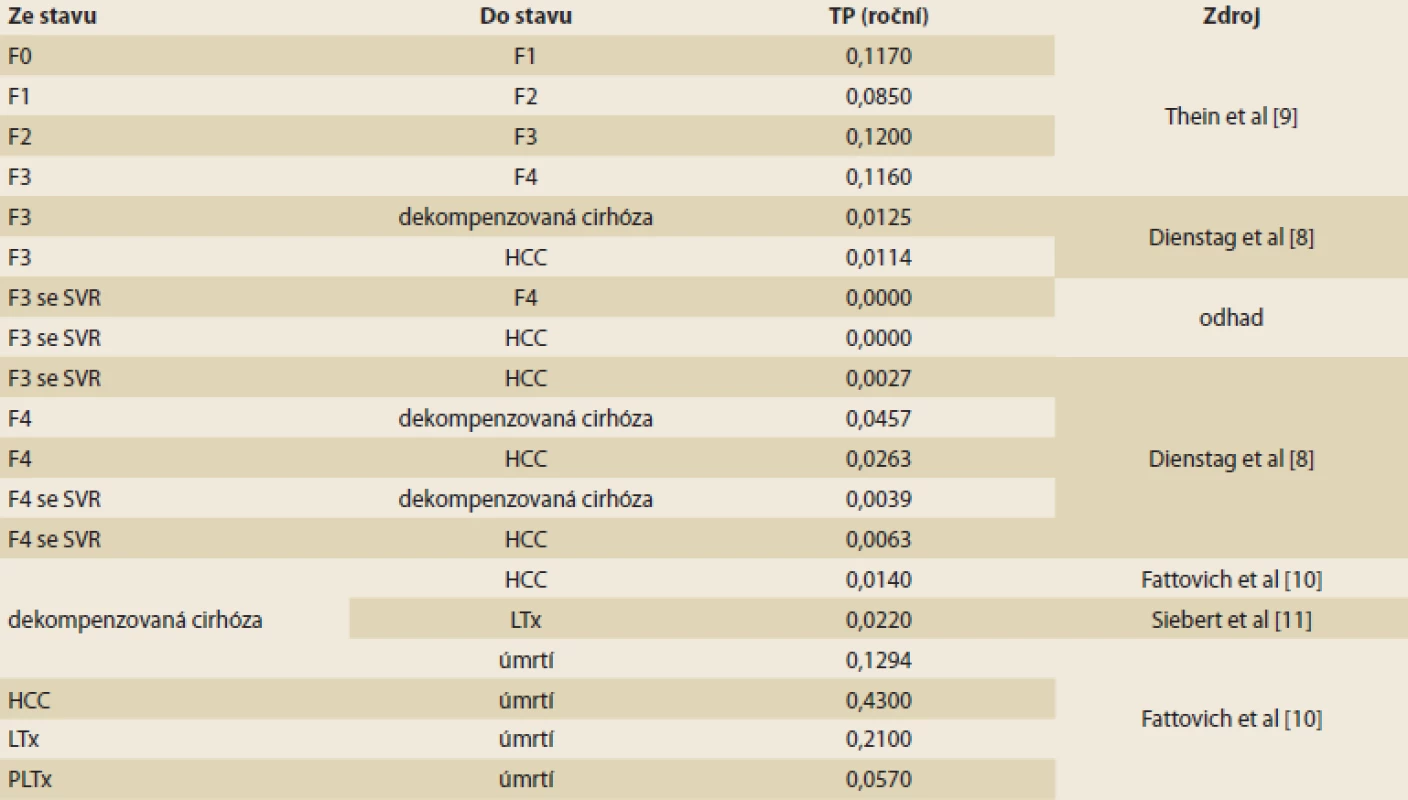
SVR – trvalá virologická odpověď, HCC – hepatocelulární karcinom, LTx – transplantace jater, PLTx – stav po transplantaci jater, TP – přechodové pravděpodobnosti Schéma 1. Markovova modelu. Scheme 1. Markov model scheme. 
HCC – hepatocelulární karcinom, LTx – transplantace jater, PLTx – stav po transplantaci jater Do modelu vstupují pacienti s chronickou HCV infekcí vyvolanou GT1 průměrného věku 32 let, což odpovídá průměrnému věku diagnózy a primoléčby v ČR [15]. S ohledem na charakter onemocnění je modelován celoživotní časový horizont (60 let). Stav nemocných je hodnocen každé 2 týdny (uvažovaná délka cyklu v modelu), tzn. že pacient každé 2 týdny buď setrvává v původním stavu zdraví, nebo přechází do jiného zdravotního stavu. Kohorta léčených osob v čase stárne a mortalita odpovídá pravděpodobnosti úmrtí podle věku na základě údajů Českého statistického úřadu [16]. Pro komplikace (dekompenzace cirhózy, rozvoj HCC) a stav po LTx byla zahrnuta specifická mortalita.
Analýza je typu cost-utility (tedy užitečnosti nákladů). Jedná se o preferovanou analýzu ve farmakoekonomice, ve které jsou parametrem přínosu tzv. QALY (Quality adjusted life-years), což představuje roky života v plné kvalitě zdraví. Parametr QALY je přínosem volby jak v ČR, tak i v dalších zemích Evropy. Kvalita života je různá u jednotlivých stadií fibrózy (METAVIR), u komplikací a po dosažení SVR. V ekonomických modelech má tedy pacient v jednotlivých cyklech modelu určitou kvalitu života (utilitu) v závislosti na stavu zdraví, ve kterém se právě nachází. Utility v jednotlivých cyklech jsou potom v horizontu analýzy sečteny a výsledkem jsou QALY (tedy roky života v plné kvalitě) pro hodnocenou a komparativní intervenci. K hodnocení kvality života je upřednostňován generický dotazník EQ-5D, který lze použít prakticky pro jakékoli onemocnění [17]. Hodnoty utilit pro jednotlivé stavy v modelu byly odvozeny z publikované literatury (tab. 3) [18].
Table 3. Hodnoty utilit v modelu. Tab. 3. Utility values in the model. 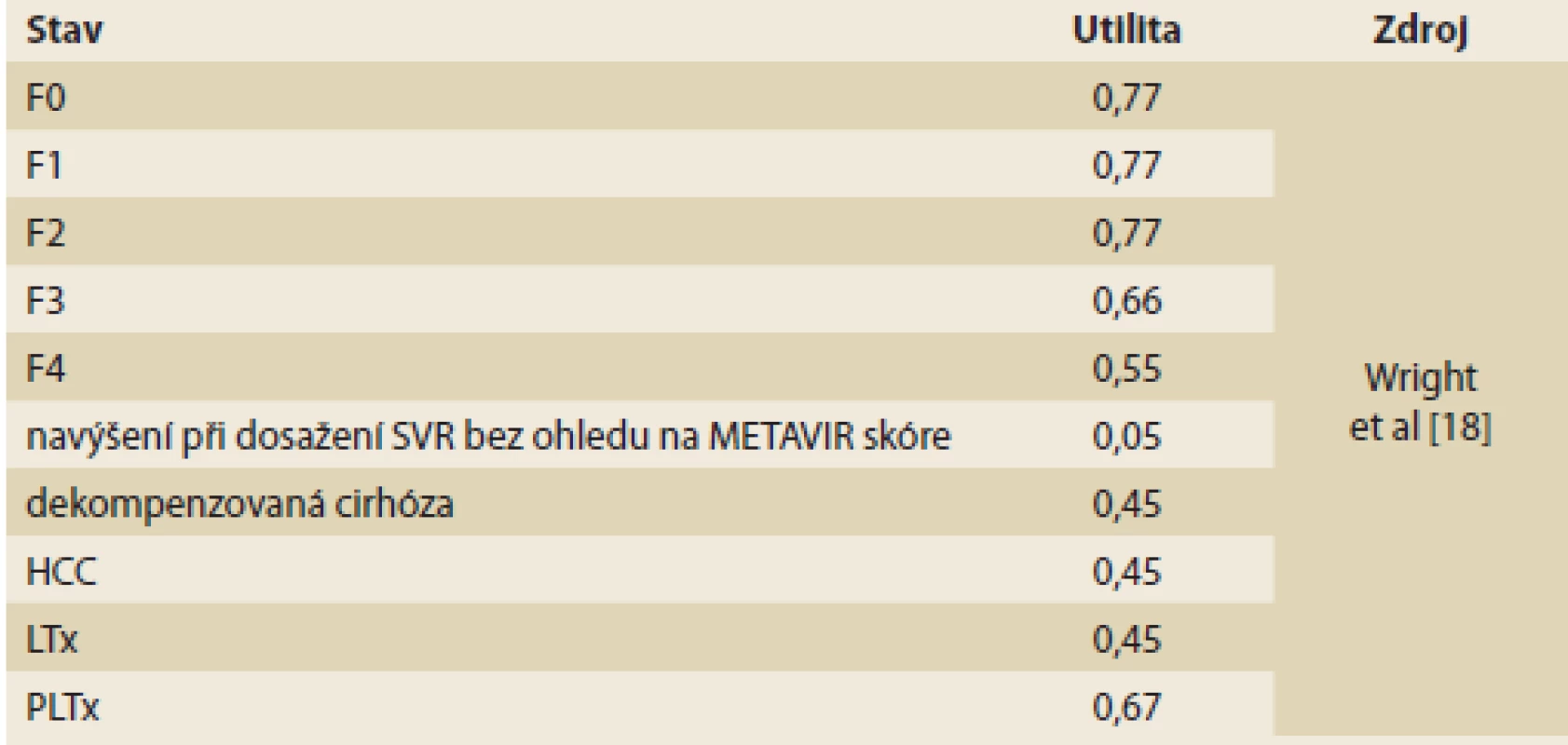
SVR – setrvalá virologická odpověď, HCC – hepatocelulární karcinom, LTx – transplantace jater, PLTx – stav po transplantaci jater Náklady v modelu jsou v základním scénáři přímé (zdravotní), v alternativním scénáři potom přímé i nepřímé (sociální). Pro stanovení cen a úhrad jsou v ČR akceptovány pouze zdravotní náklady, nicméně HCV infekce postihuje mladou populaci v produktivním věku. Při pracovní neschopnosti nebo trvalé invaliditě je tak sociální systém zatížen náklady, které nejsou zanedbatelné. Zdravotní náklady zahrnují medikaci, monitoring během terapie a náklady komplikací (dekompenzaci cirhózy, HCC) i transplantace. Nepřímé náklady vychází z průměrné mzdy v ČR ve druhém čtvrtletí 2017 [20]. Sumarizace nákladů je zobrazena v tab. 4.
Table 4. Náklady v modelu. Tab. 4. Model costs. 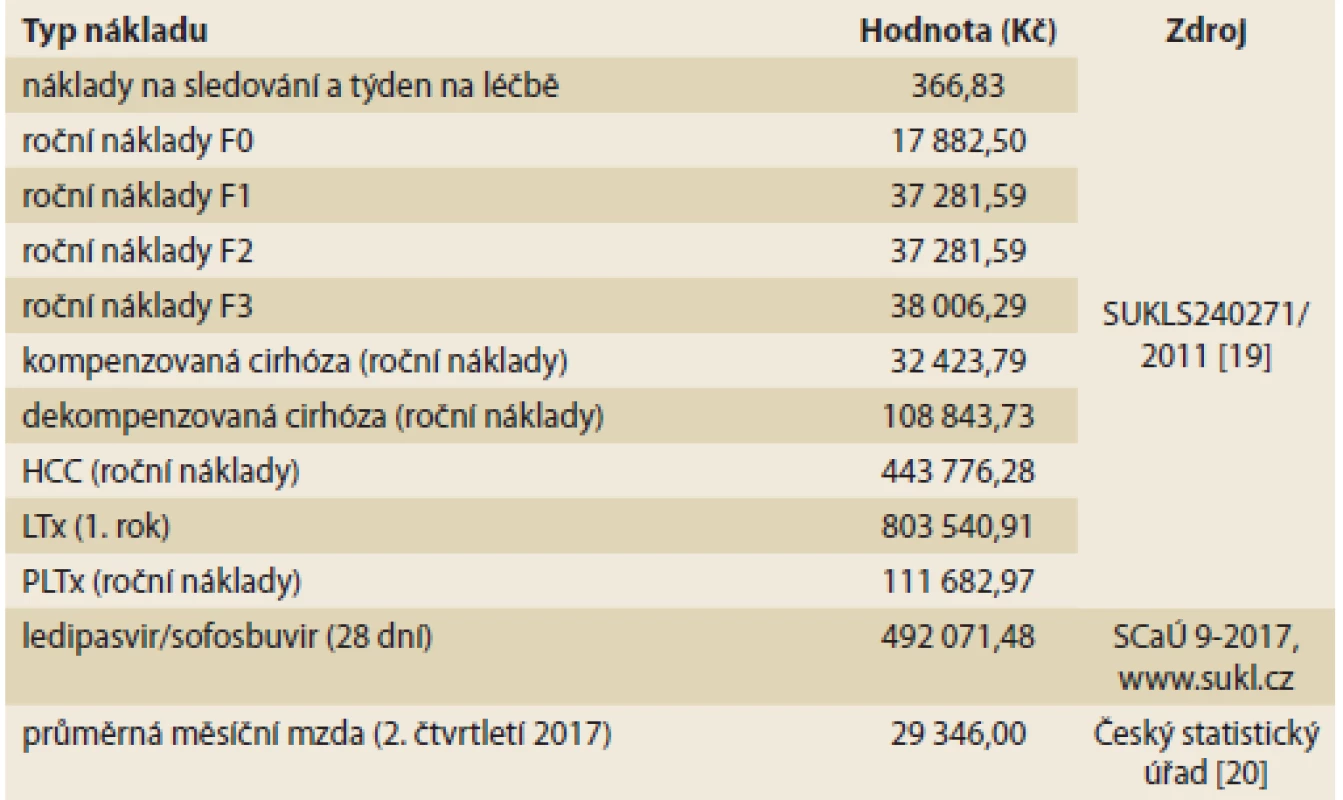
HCC – hepatocelulární karcinom, LTx – transplantace jater, PLTx – stav po transplantaci jater, SCaÚ – seznam cen a úhrad Náklady a výstupy (QALY) jsou diskontovány 3 % ročně, což odpovídá metodice Státního ústavu pro kontrolu léčiv [21].
Výsledek analýzy je prezentován ve formě ICER (inkrementální poměr nákladů a přínosů), který uvádí, o kolik více finančních prostředků je třeba hodnocenou intervencí vynaložit na dosažení 1 QALY navíc oproti současnému stavu. Vzorec pro výpočet ICER je uveden zde:
Pro limitaci nejistoty v modelu byla provedena jednocestná (DSA – deterministic sensitivity analysis) i pravděpodobnostní (PSA – probabilistic sensitivity analysis) analýza senzitivity. V DSA byl vždy měněn jeden vstupní parametr v určitém rozmezí (věk pacientů, účinnost léčby a náklady s variací ± 20 %, pravděpodobnosti přechodů mezi stavy a utility v rozmezí konfidenčních intervalů). V PSA potom náhodně více parametrů v uvedeném rozmezí současně, s obvyklou statistickou distribucí (náklady s distribucí gamma, ostatní parametry s distribucí beta). Výsledek DSA odhaduje parametr s největším vlivem na výsledek modelace, výsledkem PSA je CEAC (cost-effectiveness acceptability curve), která uvádí podíl nákladově efektivních modelací při různých hodnotách hranice ochoty platit.
Výsledek
V kohortě hodnocené intervence bylo reálně léčeno více pacientů než v kohortě komparativní (10 000 vs. 9 505), což bylo dáno skutečností, že ne všichni infikovaní progredovali až do stadia F3/F4. Navzdory této skutečnosti byly průměrné náklady na pacienta při okamžité léčbě nižší a efektivita (daná ziskem QALY) vyšší. Výsledný ICER je záporný ve výši –4 414 Kč/QALY a hodnocená intervence je tzv. dominantní (nižší náklady a vyšší účinnost). Výsledky jsou uvedeny v tab. 5. Náklady medikace jsou při okamžité léčbě o 150 066 Kč vyšší, mírně vyšší jsou i náklady na monitoring (17 502 Kč); naopak okamžitá léčba šetří náklady v segmentu zdravotních stavů, tedy zejména komplikací choroby (rozdíl –157 208 Kč). Z pohledu účinnosti je významné, že pacienti s okamžitou léčbou získávají 1,7 roku života v plné kvalitě oproti nemocným s oddálenou terapií. V kohortě hodnocené intervence je na 10 000 pacientů zabráněno 619 příhodám, zejména HCC a úmrtí (tab. 5). Náklady na jednoho vyléčeného nemocného jsou u okamžité terapie mírně vyšší, a to o 144 530 Kč.
Table 5. Výsledky modelování – základní scénář. Tab. 5. Modelling results – base-case scenario. 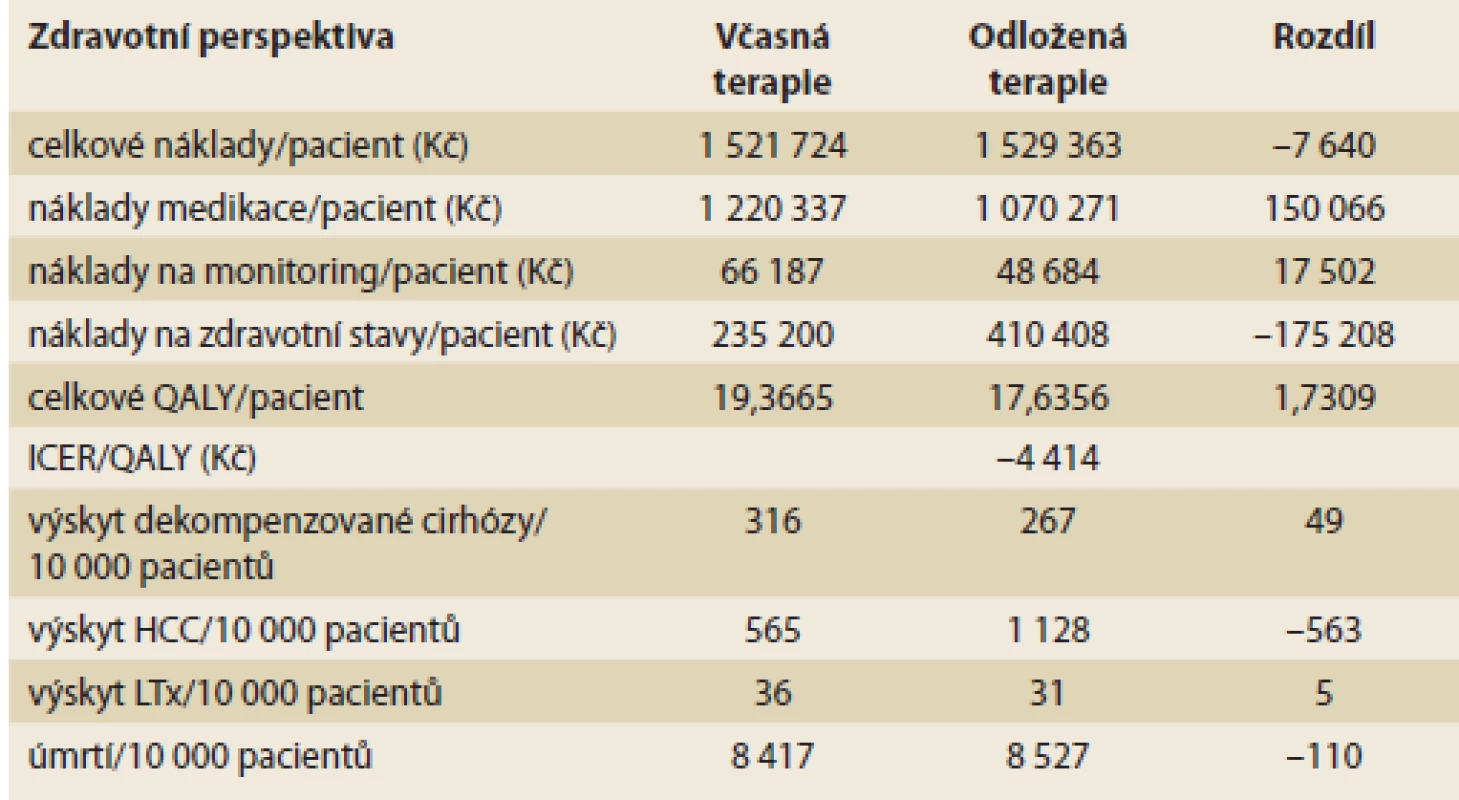
QALY – Quality adjusted life-years, ICER – Incremental cost-eff ectiveness ratio, HCC – hepatocelulární karcinom, LTx – transplantace jater Největší vliv na výsledek v DSA má míra diskontace nákladů (mezní hodnoty 0 a 5 % ročně) a náklady během léčby. Nejvyšší dosažený ICER/QALY je 192 000 Kč, takže hluboko pod hranicí ochoty platit v českém systému na úrovni 1,2 mil. Kč. Na grafu 1 jsou uvedeny výsledky prvních 10 parametrů s největším vlivem na výsledek analýzy.
Graph 1. Výsledky jednocestné analýzy senzitivity – Tornado diagram. Graph 1. Results of one-way sensitivity analysis – Tornado diagram. 
TP – přechodové pravděpodobnosti, SVR – setrvalá virologická odpověď, TN – dosud neléčení (treatment naive), GT – genotyp, LDV/SOF – ledipasvir/sofosbuvir, ICER – Incremental cost-effectiveness ratio, QALY – Quality adjusted life-years Výsledek 1 000 iterací v PSA je konzistentní s průměrnými výsledky v deterministickém scénáři. Jednotlivé body (výsledky iterací) oscilují kolem nulové hodnoty na vertikální ose znázorňující náklady. Na horizontální ose je zobrazen rozdíl v zisku QALY, který je 2,14 ve prospěch hodnocené kombinace, tedy okamžité léčby (graf 2). Z výsledku této analýzy senzitivity vyplývá, že 40 % všech iterací je dominantní pro hodnocenou intervenci (méně nákladné a účinnější), 60 % v pásmu vysoce nákladově efektivní intervence. CEAC potom ukazuje, že 90 % intervencí je nákladově efektivních, a to při hranici ochoty platit 225 000 Kč (graf 3). Tato hranice je hluboko pod oficiální hranicí ochoty platit v ČR (1,2 mil. Kč).
Graph 2. Výsledky pravděpodobnostní analýzy senzitivity. Graph 2. Results of probabilistic sensitivity analysis. 
Jednotlivé šedé body jsou výsledky iterací. Graph 3. Výsledky CEAC (podíl nákladově efektivních intervencí při různé hranici ochoty platit). Graph 3. CEAC results (proportion of cost-e ective interventions at different willingness-to-pay thresholds). 
Při zkrácení časového horizontu modelace na 30 let (tedy do věku 60 let léčených) je okamžitá intervence nadále účinnější, s poněkud vyššími náklady v porovnání s celoživotním časovým horizontem, a ICER je 44 980 Kč/QALY. Tato hodnota je stále hluboce pod hranicí ochoty platit, která je v ČR implicitně stanovena na 1,2 mil. Kč/QALY.
Při započtení jak zdravotních, tak i sociálních nákladů je dominance okamžité intervence potvrzena. I v tomto scénáři je okamžitá léčba méně nákladná a účinnější, ICER je –214 948 Kč/QALY.
Diskuze
Nové DAA režimy přinášejí vyšší účinnost, lepší snášenlivost a zkrácení délky léčby. Jsou nicméně nákladnější, což vede k jejich používání zejména u stavů s pokročilou jaterní fibrózou [1,3].
Tato analýza prokázala, že okamžitá léčba všech HCV pacientů bez ohledu na METAVIR skóre šetří náklady oproti oddálené terapii, tj. stavu, kdy je protivirová léčba zahajována pouze u pacientů s pokročilými stadii fibrózy F3/F4. Tato skutečnost platí při zohlednění zdravotních nákladů, ale i při kombinaci nákladů zdravotního a sociálního systému. Z pohledu pacientů je podstatný zisk 1,7 roku života v plné kvalitě, pokud je léčba zahájena co nejdříve, a přibližně poloviční riziko vzniku HCC.
Silnou stránku provedené analýzy spatřujeme ve vstupních datech, která vychází buď z randomizovaných kontrolovaných studií (účinnost) nebo z publikovaných hodnocení zdravotnických technologií (kvalita života, přechodové pravděpodobnosti mezi jednotlivými stavy). Naopak limitací je nezahrnutí rekurence HCV a současně i nezohlednění nižšího rizika přenosu infekce při dosažení SVR u hodnocené kohorty.
V posledních letech se objevují nové publikace týkající se okamžité vs. oddálené léčby HCV. Leidner et al hodnotili nákladovou efektivitu u pacientů s F2 okamžitě léčených vs. oddálení terapie do METAVIR F3 ve Spojených státech [22]. Léčba byla nákladově efektivní, ICER byl na úrovni 37 700 $/QALY. Chidi et al porovnávali nákladovou efektivitu léčby DAA u pacientů s HCV GT1 bez ohledu na stav jaterní fibrózy vs. oddálenou léčbu při progresi do F3 [23]. DAA režimy užívané bez ohledu na jaterní fibrózu byly dominantní, tedy méně nákladné a účinnější. Younossi et al porovnávali nákladovou efektivitu interferonových a DAA terapií podle stadia fibrózy a u všech pacientů s HCV [24]. Výsledky ukazují, že léčba DAA u všech infikovaných je dominantní oproti režimům s pegylovanými interferony.
Adaptace farmakoekonomického modelu v českém prostředí prokázala podobné výsledky jako zahraniční publikace. DAA je dominantní nejen z pohledu zdravotního, ale i při započtení zdravotních a sociálních nákladů. V modelu byla uvažována léčba kombinací ledipasvir/sofosbuvir. Výsledky lze však považovat za přenositelné i na další DAA vzhledem k jejich blízké účinnosti, bezpečnosti a porovnatelné ceně léčby. Tuto skutečnost potvrzuje i publikovaná literatura používající obdobné farmakoekonomické modely [25].
Závěr
Analýza nákladové efektivity prokázala, že okamžitá léčba pacientů s HCV GT1 režimy bez interferonu je v celoživotním horizontu méně nákladná a účinnější než stejná léčba odložená do stadia pokročilé jaterní fibrózy (F3/F4) v podmínkách ČR. Výsledky jsou konzistentní při započtení přímých (zdravotních) i nepřímých (sociálních) nákladů.
Práce byla podpořena společností Gilead Sciences, s. r. o. Sponzor se nepodílel na validaci modelu, jeho adaptaci na české podmínky anebo na návrhu manuskriptu.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 16. 11. 2017
Přijato: 20. 12. 2017
MUDr. Jana Skoupá
Czechta Institute, o. p. s.
Kateřinská 1660/32
120 00 Praha 2
E-shop: jana.skoupa@iol.cz
Sources
1. Bedossa P, Poynard T. An algorithm for the grading of activity in chronic hepatitis C. The METAVIR Cooperative Study Group. Hepatology 1996; 24 (2): 289–293.
2. European Association for the Study of the Liver. EASL recommendations on treatment of hepatitis C 2016. J Hepatol 2017; 66 (1): 153–194. doi: 10.1016/j.jhep.2016.09.001.
3. Urbánek P, Husa P, Šperl J et al. Standardní diagnostický a terapeutický postup chronické infekce virem hepatitidy C. Gastroent Hepatol 2017; 71 (2): 117–136. doi: 10.14735/amgh2017117.
4. Chahal HS, Merseille EA, Tice JA et al. Cost-effectiveness of early treatment of hepatitis C virus genotype 1 by stage of liver fibrosis in a US treatment-naive population. JAMA Intern Med 2016; 176 (1): 65–73. doi: 10.1001/jamainternmed.2015.6011.
5. Leidner AJ, Chesson HW, Xu F et al. Cost-effectiveness of hepatitis C treatment for patients in early stages of liver disease. Hepatology 2015; 61 (6): 1860–1869. doi: 10.1002/hep.27736.
6. Obach D, Deuffic-Burban S, Esmat G et al. Effectiveness and cost-effectiveness of immediate versus delayed treatment of hepatitis C virus-infected patients in a country with limited resources: the case of Egypt. Clin Infect Dis 2014; 58 (8): 1064–1071. doi: 10.1093/cid/ciu 066.
7. Bennett WG, Inoue Y, Beck JR et al. Estimates of the cost-effectiveness of a single course of interferon-alpha 2b in patients with histologically mild chronic hepatitis C. Ann Intern Med 1997; 127 (10): 855–865.
8. Dienstag JL, Ghany MG, Morgan TR et al. A prospective study of the rate of progression in compensated, histologically advanced chronic hepatitis C. Hepatology 2011; 54 (2): 396–405. doi: 10.1002/hep.24370.
9. Thein H, Yi Q, Dore GJ et al. Estimation of stage-specific fibrosis progression rates in chronic hepatitis C virus infection: a meta-analysis and meta-regression. Hepatology 2008; 48 (2): 418–431. doi: 10.1002/hep.22375.
10. Fattovich G, Giustina G, Degos F et al. Morbidity and mortality in compensated cirrhosis type C: a retrospective follow-up study of 384 patients. Gastroenterology 1997; 112 (2): 463–472.
11. Siebert U, Sroczynski G, Wasem J et al. Using competence network collaboration and decision-analytic modeling to assess the cost-effectiveness of interferon alpha-2b plus ribavirin as initial treatment of chronic hepatitis C in Germany. Eur J Health Econ 2005; 6 (2): 112–123.
12. Afdhal N, Zeuzem S, Kwo P et al. Ledipasvir and sofosbuvir for untreated HCV genotype 1 infection. N Engl J Med 2014; 370 (20): 1889–1898. doi: 10.1056/NEJMoa1402454.
13. Kowdley KV, Gordon SC, Reddy KR et al. Ledipasvir and sofosbuvir for 8 or 12 weeks for chronic HCV without cirhosis. N Engl J Med 2014; 370 (20): 1879–1888. doi: 10.1056/NEJMoa1402355.
14. Gilead Sciences SVR12 by metavir score in subjects whose cirrhosis status determined by liver biopsy 2014. Data on file.
15. Razavi H, Waked I, Sarrazin C et al. The present and future disease burden of hepatitis C virus (HCV) infection with today’s treatment paradigm. J Viral Hepat 2014; 21 (Suppl 1): 34–59. doi: 10.1111/jvh.12248.
16. Český statistický úřad. Úmrtnostní tabulky za ČR, regiony soudržnosti a kraje – 2014–2015. [online]. Dostupné z: https: //www.czso.cz/csu/ czso/umrtnostni-tabulky-za-cr-regiony-soudrznosti-a-kraje.
17. Kind P, Brooks R, Rabin R (eds). EQ-5D concepts and methods. Dordrech: Springer 2006.
18. Wright M, Grieve R, Roberts J et al. Health benefits of antiviral therapy for mild chronic hepatitis C: randomised controlled trial and economic evaluation. Health Technol Assess 2006; 10 (21): 1–113.
19. Státní ústav pro kontrolu léčiv. Správní řízení č. SUKLS240271/2011 [online]. Dostupné z: http: //www.sukl.cz/modules/procedures/detail.php?spzn=SUKLS240271%2F2011.
20. Český statistický úřad. Mzdy a náklady práce. [online]. Dostupné z: https: //www.czso.cz/csu/czso/prace_a_mzdy_prace.
21. Státní ústav pro kontrolu léčiv. SP-CAU-028. Postup pro posuzování analýzy nákladové efektivity. [online]. Dostupné z: http: //www.sukl.cz/leciva/sp-cau-028?highlightWords=SP-CAU-028.
22. Leidner AJ, Chesson HW, Xu F et al. Cost-effectiveness of hepatitis C treatment for patients in early stages of liver disease. Hepatology 2015; 61 (6): 1860–1869. doi: 10.1002/hep.27 736.
23. Chidi AP, Bryce CL, Donohue JM et al. Economic and public health impacts of policies restricting access to hepatitis C treatment for medicaid patients. Value Health 2016; 19 (4): 326–334. doi: 10.1016/j.jval.2016.01.010.
24. Younossi ZM, Singer ME, Mir HM et al. Impact of interferon free regimens on clinical and cost outcomes for chronic hepatitis C genotype 1 patients. J Hepatol 2014; 60 (3): 530–537. doi: 10.1016/j.jhep.2013.11.009.
25. Gonzales YS, Ingram A, Lindsay C et al. Early versus delayed hepatitis C treatment provides increased health benefits at lower costs: a UK cost-effectiveness analysis of genotypes 1 and 4 treatment-naïve patients. J Hepatol 2017; 66 (1): S747–S748. doi: 10.1016/S0168-8278 (17) 31988-8.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology

2018 Issue 1-
All articles in this issue
- Novinky v roce 2018
- Můžeme zvýšit efektivitu léčby anti-TNF protilátkami?
- Kvalita života pacientů s idiopatickými střevními záněty v České republice – multicentrická studie
- Odporúčania Pracovnej skupiny pre IBD Slovenskej gastroenterologickej spoločnosti pre liečbu Crohnovej choroby
- Efekt ustekinumabu u pacienta refrakterního na ostatní biologickou léčbu
- Postavení CT kolografie v algoritmu vyšetření tlustého střeva
- Onemocnění gastrointestinálního traktu a choroby ledvin
- Porovnání nákladové efektivity okamžitě zahájené léčby oproti odložené terapii chronické hepatitidy C v České republice
- Endoskopické řešení Bueveretova syndromu
- K úmrtí doc. MUDr. Zdeňka Slezáka, CSc.
- Výběr z mezinárodních časopisů
- VSL#3 – první vysoce koncentrované probiotikum s mnohočetnými probiotickými kulturami a ověřenou terapeutickou účinností
- Výsledky těhotenství u pacientek s idiopatickými střevními záněty léčených biosimilárním infliximabem
- Terapeutické monitorovanie infliximabu pri nešpecifických zápalových ochoreniach čreva
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- VSL#3 – první vysoce koncentrované probiotikum s mnohočetnými probiotickými kulturami a ověřenou terapeutickou účinností
- Onemocnění gastrointestinálního traktu a choroby ledvin
- Postavení CT kolografie v algoritmu vyšetření tlustého střeva
- Odporúčania Pracovnej skupiny pre IBD Slovenskej gastroenterologickej spoločnosti pre liečbu Crohnovej choroby
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


