-
Medical journals
- Career
Využití neuromodulace v léčbě dysfunkcí dolních močových cest
Authors: Michal Rejchrt
Authors‘ workplace: Praha ; Urologická klinika 2. LF UK a FN Motol
Published in: Ces Urol 2012; 16(1): 5-12
Category: Review article
Overview
Konzervativní léčba dysfunkcí dolních močových cest zahrnuje behaviorální techniky, farmakoterapii a cvičení svalů dna pánevního. Dominující léčebnou metodou je farmakoterapie, která však není u všech pacientů dostatečně účinná a u podstatné části je její použití limitováno závažnými systémovými nežádoucími účinky. Krajním řešením při selhání konzervativní terapie jsou chirurgické metody zahrnující augmentaci močového měchýře a močové derivace, které jsou rezervovány pro nejtěžší pacienty. Neuromodulace v léčbě dysfunkcí dolních močových cest může nejen doplnit mezeru mezi možnostmi konzervativní a chirurgické léčby, ale je i alternativou v případě selhání konzervativní terapie první linie. Cílem práce je podat přehled jednotlivých neuromodulačních metod se zhodnocením jejich efektivity, indikací a komplikací.
Klíčová slova:
hyperaktivní močový měchýř, neuromodulace, stimulátor, urgentní inkontinence.ÚVOD
Dysfunkce dolních močových cest jsou jedním z nejčastějších urologických problémů současné dospělé populace. Symptomy mají negativní vliv na pracovní uplatnění, sociální postavení a v neposlední řadě i partnerské vztahy. Při zahrnutí nepřímých nákladů se v roce 2018 odhaduje nutnost vynaložení 2,3 bilionů dolarů na léčbu 428 milionů nemocných trpících těmito symptomy na celém světě (1). Je tedy zřejmé, že se jedná o závažný socioekonomický problém. Konzervativní léčba zahrnuje behaviorální techniky, farmakoterapii a cvičení svalů dna pánevního. Dominující léčebnou metodou je farmakoterapie, která však není u všech pacientů dostatečně účinná a u podstatné části je její použití limitováno závažnými systémovými nežádoucími účinky. Krajním řešením při selhání konzervativní terapie jsou chirurgické metody zahrnující augmentaci močového měchýře a močové derivace, které jsou rezervovány pro nejtěžší pacienty. Další možností léčby je neuromodulace, kterou lze použít v případě selhání konzervativní terapie první linie. Použití elektrické energie v léčbě sahá hluboko do historie a značně předchází objevení tohoto fyzikálního jevu, který učinil William Gilbert, lékař královny Alžběty I., až v roce 1600. Již ve starověku bylo využíváno účinků elektrických ryb. Hippokrates předepisoval užití elektrických výbojů ryb pro zlepšení stavu u podvyživených nemocných. Římský lékař a spisovatel Scribonius Largus Designatus na počátku 1. století n. l. popisuje léčbu bolestí hlavy a léčbu bolestí při dnavém záchvatu přikládáním rejnoka elektrického druhu Torpedo nobilita na postižená místa, přičemž poznamenává, že léčbu je nutné provádět opakovaně a signálem úspěchu je lokální necitlivost. Rozvoj použití elektřiny v běžném životě se odráží i v lékařství. V 18. století bylo na téma elektroléčby bolestivých projevů rozličných chorob vydáno až pět knih ročně. V urologii první pokusy s intravezikální elektrostimulací provedl již v roce 1887 dánský chirurg Saxtorph (2).
Běžným jevem v české i zahraniční literatuře je nesprávné používání termínu neurostimulace a neuromodulace. Chybné názvosloví je dané historickým vývojem jednotlivých metod,je již hluboce zakořeněné a nelze se mu vyhnout ani v tomto článku. Elektrická neurostimulace označuje přímé řízení cílového orgánu elektrostimulací nervu. V urologii představuje tuto techniku stimulace předních kořenů míšních (sacral anterior root stimulation – SARS) v kombinaci se sakrální deaferentací. Po chirurgicky navozené akontraktilitě detruzoru jsou implantovány elektrody na přední kořeny míšní S2–4. Prostřednictvím zevního vysílače jsou transkutánně indukovány elektrické impulzy umožňující stimulovanou mikci, defekaci a v některých případech i erekci. Tato ekonomicky náročná metoda indikovaná v současnosti výhradně u nemocných s kompletní lézí míchy nad sakrálním mikčním centrem je od roku 2001 prováděna i v České republice (3). Oproti tomu při elektrické neuromodulaci se snažíme odstranit patologickou aktivitu cílového orgánu ovlivněním řídícího nervového centra. Přesný mechanismus účinku neuromodulace je dosud nejasný. Důvodem je velice komplikovaná neurální kontrola mikčního cyklu, do níž jsou významným způsobem zapojeny nejvyšší etáže CNS včetně volní aktivity a emocí. Neuromodulační techniky lze rozdělit na neinvazivní, minimálně invazivní a invazivní. Neinvazivní metody zahrnují anogenitální neurostimulaci a transkutánní neurostimulaci, minimálně invazivní perkutánní stimulaci nervus tibialis posterior a intravezikální elektrostimulaci. Sakrální neuromodulace vyžaduje použití implantabilních systémů a řadí se k invazivním metodám(tab. 1). V současné době se v neuromodulaci používá nábojově vyvážený stejnosměrný elektrický proud s nízkou frekvencí.
Table 1. Indikace metody neuromodulace dle typu dysfunkce detruzoru Table 1. Indications of method of neuromodulation by the type of detrusor dysfunction 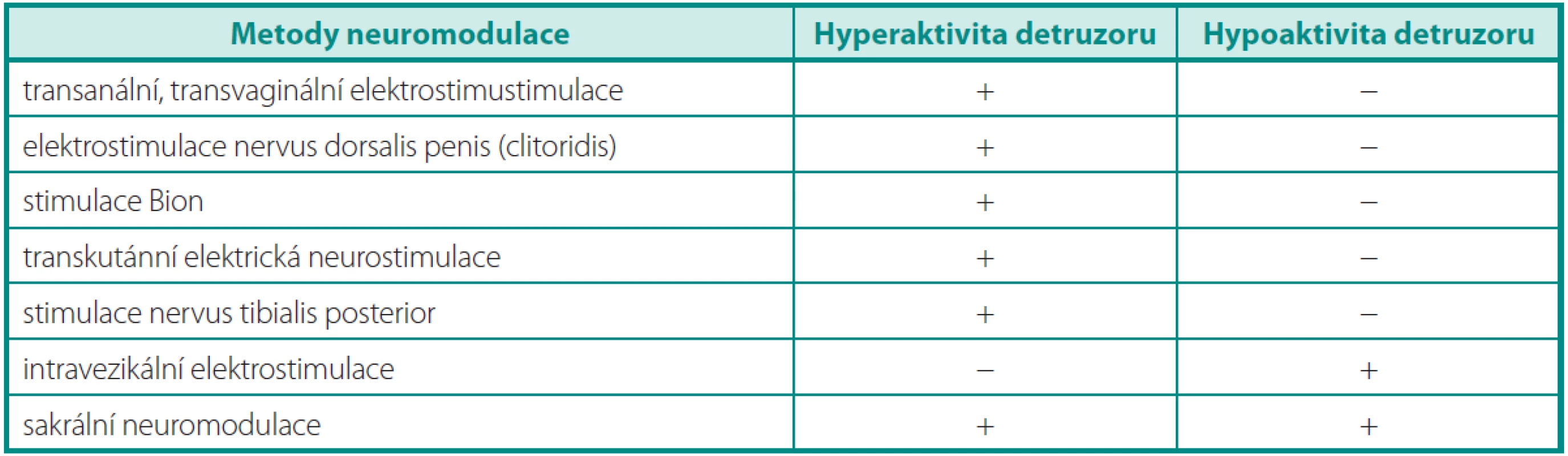
ANOGENITÁLNÍ ELEKTROSTIMULACE
Na efektivitě této metody se podílí několik mechanismů. Stimulací aferentní složky pudendálního nervu dochází k inhibici pelvickéhojádra v sakrální míše. Spinální interakcí dochází k aktivaci hypogastrického nervu, který vyvolá prostřednictvím beta-adrenergních receptorů fundu měchýře jeho relaxaci (4). Dále se předpokládá, že stimulací eferentních vláken pro příčně pruhovaný svěrač dochází k reflexní inhibici detruzoru (5). Tyto hypotézy podporuje i fakt, že dilatace anu vyvolá prostřednictvím pelvického nervu relaxaci detruzoru, nebo skutečnost, že při koitu dochází cestou pudendálního nervu k reflexnímu přerušení kontrakce detruzoru. Významnou úlohu pravděpodobně hrají supraspinální struktury CNS. V roce 1963 provedl Caldwell et al. úspěšnou implantaci análního stimulátoru u nemocného s fekální inkontinencí (6). Na základě těchto zkušeností popsal Godec et al. v roce 1975 anální elektrostimulaci introitální sondou u nemocných s dysfunkcí močových cest (7). Výsledky transvaginální elektrostimulace prezentoval Fall et al. v roce 1977(8). Efektivita obou metod se v jednotlivých publikovaných studiích značně liší, stejně jako léčebná schémata a fyzikální parametry použitého elektrického impulzu. Data jsou obtížně porovnatelná také pro nesourodé skupiny zařazených pacientů, které zvláště ve starších publikacích často zahrnují i nemocné se stresovou inkontinencí. Fall et al. dosáhl více než 50% benefit při 5letém sledování. Primus et al. v roce 1996 uvádí 64% úspěšnost ve skupině nemocných s idiopatickou hyperaktivitou detruzoru po 2 letech sledování, ale zároveň selhání efektu 2 měsíce od ukončení léčby u pacientů s roztroušenou sklerózou (9). Zklamáním byly výsledky u starších nemocných s kognitivní poruchou (10). Ve snaze zvýšit efektivitu léčby použili někteří autoři maximální tolerovatelnou intenzitu proudu většinou ve zkráceném schématu pouze několika sezení. Tato „maximální elektrická stimulace“ často kombinovala současně transvaginální a transanální přístup, někdy ještě doplněný o stimulaci pudendálního nervu jehlovou elektrodou. Většinou byla aplikována u nemocných s neurogenní dysfunkcí dolních močových cest se značně rozdílnými výsledky (20–90 %). Fyzický a psychický dyskomfort výrazně snižoval compliance pacientů, kteří často léčbu nedokončili. K dispozici jsou pouze starší experimentální studie (11). Transvaginální a transanální techniky jsou v současnosti spíše v pozici historických metod. K dosažení přijatelného efektu je nutná dlouhodobá léčba. Značná diskrepance je mezi zlepšením symptomatologie a urodynamického nálezu. Pouze u části nemocných má tato léčba dlouhodobý efekt.
Elektrostimulace nervus dorsalis penis (clitoridis) využívá vysoké koncentrace čistě senzitivních větví pudendálního nervu v oblasti penisu (klitorisu). Provádí se umístěním povrchové elektrody na dorzum penisu u muže, svorkových elektrod na malé stydké pysky, či povrchové elektrody na klitorisu ženy. Již v roce 1984 použil tuto metodu Nakamura et al. a prokázal nárůst cystometrické kapacity u deseti z 22 nemocných s hyperaktivitou detruzoru (12). Wheeler et al. provedl urodynamickou studii u šesti nemocných po míšním traumatu, kde dosáhl nárůstu cystometrické kapacity o 27–150 % v průběhu stimulace u všech nemocných. Kontrolní vyšetření po proběhlé stimulaci vykázalo opět pokles sledovaného parametru, ale ne až na výchozí hodnoty (13). Madersbacher et al. pozoroval lepší vliv terapie na nárůst cystometrické kapacity ve skupině nemocných s neurogenní dysfunkcí, 75 % z nich však vyžadovalo dlouhodobou léčbu oproti 50 % ve skupině non-neurogenní (14).
Vývoj miniaturního bezdrátového stimulátoru Bion (Bionics Corp., Valencia, CA,USA) přinesl renezanci neuromodulace pudendálního nervu. Tento přístroj o velikosti 27 × 3,3 mm lze dálkově programovat i dobíjet. Vlastní implantaci předchází perkutánní screeningový test, který je pozitivní, pokud dojde k minimálně 50% zvýšení itravezikálního objemu při první kontrakci detruzoru, či maximální cystometrické kapacity. V roce 2005 Spinelli et al. prezentoval miniinvazivní techniku implantace přístroje do Alcockova kanálu z perineálního či dorzálního přístupu v lokální anestezii (15). Peters et al. ve stejném roce publikoval srovnávací studii, kde tato metoda vykazovala lepší výsledky než sakrální neuromodulace (16). Týž autor v roce 2010dosáhl u 71 % z 84 nemocných pozitivní odpovědi (zlepšení symptomatologie o více než 50 %), přičemž uspěl u většiny pacientů (93 %) před tím neúspěšně léčených sakrální neuromodulací (17). Tato perspektivní metoda může v budoucnu konkurovat sakrální neuromodulaci.
TRANSKUTÁNNÍ ELEKTRICKÁ NEUROSTIMULACE
Suprapubickou transkutánní stimulaci prezentoval Fall et al. v roce 1980 u pacientů s intersticiální cystitidou, přičemž pozoroval nejen zmírnění algických, ale i mikčních symptomů (18). Další studie byly provedeny i u pacientů s idiopatickou hyperaktivitou detruzoru. Technika spočívá v umístění dvou elektrod 10–15 cm od sebe nad sponu stydkou, parametry elektrického impulzu se v jednotlivých publikacích značně liší. Urodynamické studie mají protichůdné výsledky. Dobrou klinickou i urodynamickou odpověď měla transkutánní stimulace s umístěním elektrod v dermatomech S2 a S3, nebo nad foramen sacrale S2,S3. Hasan et al. odsáhl zmírnění inkontinence o polovinu u 69 % nemocných (19). Walsh et al. dosáhl zlepšení symptomatologie o 76 %, ale u všech 25 pacientů se po 6 měsících od ukončení léčby vrátily obtíže na původní úroveň. Iritaci kůže v místě přiložení elektrody měla třetina nemocných (20). Stejně jakou suprapubického přístupu musí být pacient připraven na nutnost dlouhodobé léčby. Transkutánní elektrická neurotimulace je v současné době spíše využívána v léčbě bolesti.
STIMULACE NERVUS TIBIALIS POSTERIOR
Tato metoda vychází z experimentální studie McGuira et al., v níž prokázal na primátech s poraněním míchy inhibici detruzoru při elektrostimulaci tibiálního nervu. Do lékařské praxe byla metoda uvedena Stollerem již v roce 1995 (21). Využívá aferencí tibiálního nervu vedoucích do segmentů S2–4. Technika spočívá v zavedení jehlové elektrody zhruba 5 cm kraniálně od vnitřního kotníku, povrchová elektroda se přikládá na kalkaneus. Kritériem správného zavedení elektrody je plantární flexe prstů nohy. Je zajímavé, že místo zavedení jehlové elektrody odpovídá akupunkturnímu bodu Sp-6 z tradiční čínské medicíny. Chang et al. dokonce u 26 žen prokázal významné změny maximální cystometrické kapacity po 30 minutách akupunktury s použitím tohoto bodu (22). Stoller použil u 90 pacientů s non-neurogenní dysfunkcí elektrické impulzy o intenzitě 5–10 mA frekvenci 20 Hz v délce30 minut po 12 týdnů a dosáhl úspěchu u 89 % nemocných, dlouhodobého efektu u 80 % při 5letém sledování. Stejného léčebného schématu se drželi i další autoři s efektivitou metody pohybující se mezi 60–80 % u nemocných s nonneurogenní dysfunkcí (23–25). Z českých autorů má s touto metodou zkušenosti Krhut et al., který dosáhl účinnosti u 65 % nemocných (26). Urodynamicky byl opakovaně prokázán bezprostřední efekt probíhající stimulace zvýšením cystometrické kapacity a oddálením první kontrakce detruzoru (27, 28). Přes tyto výsledky k obecnému akceptování metody scházela randomizovaná, placebem kontrolovaná studie. Průlomová byla studie publikovaná Petersem et al. v roce 2010, která přinesla důkaz I. úrovně o účinnosti této metody (29). Ve stejném roce autor publikoval práci vypovídající ve prospěch perkutánní stimulace tibiálního nervu v porovnání s tolterodinem (30). Zkušenosti s léčbou neurogenních dysfunkcí dolních močových cest jsou dosud omezené. Například Gobbi et al. v roce 2011 prezentoval skupinu 21 nemocných s roztroušenou sklerózou, kde pozoroval signifikantní zlepšení v 89 % (31). Obdobné výsledky jsou publikovány na malých souborech pacientů s inkompletní míšní lézí či Parkinsonovou chorobou. Objevují se i práce popisující efekt této metody na fekální inkontinenci při neurogenní dysfunkci střeva. Ačkoliv jsou výsledky povzbudivé a opravňují další výzkum u této skupiny nemocných, lze v současnosti říci, že prospěch mohou mít pouze přísně vybraní jednotlivci. U pacientů s non-neurogenními dysfunkcemi močových cest je tato metoda efektivní, bezpečná a ekonomicky nenáročná. Je vhodná i k domácí léčbě.
INTRAVEZIKÁLNÍ ELEKTROSTIMULACE
Ačkoliv jde o nejstarší metodu neuromodulace používanou v urologii, jsou její výsledky stále rozporuplné. Principem je přímá stimulace A-delta mechanoreceptorů v močovém měchýři s cílem zlepšení vnímání náplně a následného vyprazdňování močového měchýře u nemocných s neurogenním hypoaktivitním detruzorem na podkladě inkompletní léze. Provádí se pomocí katétru zavedeného do močového měchýře. Na konci katétru je umístěna kladná elektroda, přičemž indiferentní elektroda se přikládá nad sponu stydkou. Močový měchýř se plní fyziologickým roztokem. Ebner et al. doporučuje použití pulzu o šířce 2 ms, frekvenci 20 Hz a intenzitě proudu v rozmezí 1–10 mA po dobu 90 minut denně do dosažení maximálního efektu (32). Jiang et al. experimentálně prokázal, že dochází ke zvýšení excitačního synaptického přenosu na centrální úrovni reflexních drah, tedy aferencí z A-delta mechanoreceptorů do mozku (33). To vysvětluje skutečnost, že tato metoda umožňuje zlepšené vnímání náplně močového měchýře s následným zlepšením kontraktility detruzoru a volní kontroly mikce. Velice důležitý je správný výběr pacienta. Měl by mít zachovanou kontraktilitu detruzoru a alespoň částečně zachované aferentní dráhy z močového měchýře do mozku (algické čití v dermatomech S3,4). Vhodným kandidátem je nemocný s neurogenním hyposenzitivním hypoaktivitním detruzorem na podkladě inkompletní centrální či periferní léze. Přínosem před zahájením léčby může být vyšetření viscerosenzitivních kortikálních evokovaných potenciálů (34). Jako výhodná se ukázala kombinace této metody s biofeedbackem. Kaplan et al. dosáhl v souboru 288 dětí u 87 % zlepšení senzitivity močového měchýře a kontroly mikce, z toho u 18 % kontrolovanou synergní mikci a kontinenci (35). K dosažení efektu bylo průměrně potřeba 47 sezení. Oproti tomu přes signifikantní zlepšení urodynamických nálezů nedosáhl Decter et al. u 25 nemocných v průběhu 5 let léčby významného zlepšení mikční symptomatologie (36). Risi et al. dosáhl u skupiny 169 nemocných výborného zlepšení kontinence pacientů s meningomyelokélou (25 z 33), ale u idiopatické dysfunkce léčba selhala v 75 % a autor techniku v této skupině nedoporučuje (37). Publikované výsledky intravezikální elektrostimulace jsou kontroverzní. Práce nejsou porovnatelné pro rozdílnost použitých léčebných schémata vstupních, či výstupních kritérií. V případě pozitivních výsledků se většina autorů shoduje na dlouhodobém efektu léčby.
SAKRÁLNÍ NEUROMODULACE (PERKUTÁNNÍ NEUROSTIMULACE – PNS)
První implantaci provedl Tanagho a Schmidt v roce 1981. Klinické užití metody bylo v Evropě schváleno v roce 1994. Při této invazivní metodě je elektroda implantována přímo na sakrální dorzální kořen, nejčastěji na kořen S3, který se podílí více než 60 % na vedení aferencí pudendálního nervu. Facilitace aferencí při probíhající stimulaci vyvolá na supraspinální úrovni reakci, která se projeví útlumem parasympatiku. Naopak přerušení dlouhodobé stimulace vyvolá zvýšení tonu parasympatiku, a tedy i detruzorové aktivity. Tento mechanismus účinku vysvětluje efektivitu metody nejen u hyperaktivity detruzoru, ale i u jeho hypoaktivity. Mezi schválené indikace tak patří nejen hyperaktivní močový měchýř, ale i neobstrukční retence moči. Léčba probíhá ve dvou fázích. V první fázi zkušebního testování je nejdříve lokalizován kořen nervu zavedením jehlové elektrody do foramen S3. Pozitivní odpovědí je kontrakce anu, prohloubení intergluteální rýhy a dorzální flexe palce nohy. Po té je jehla nahrazena zkušební elektrodou napojenou na zevní stimulátor. Moderní elektrody jsou opatřeny kostními kotvičkami minimalizujícími možnost dislokace, což umožňuje prodloužení zkušební fáze na 2–4 týdny. Pozitivní odpověď je definována jako zlepšení symptomů alespoň o 50 % s následným zhoršením po ukončení stimulace. V případě úspěchu následuje fáze implantace trvalého dálkově programovatelného stimulátoru. Léčba se provádí za skiaskopické kontroly ambulantně v lokální anestezii doplněné analgosedací. Od roku 2006 je k dispozici systém InterStimII (Medtronic, Mineapolis, MN). Jeho miniaturizace snižuje invazivitu léčby, avšak na úkor životnosti baterie, která se pohybuje mezi 3–5 lety oproti 6–10 letům u jeho předchůdce. Lepší software rozšiřuje možnosti programování. Nutnost reimplantace pro migraci elektrody se pohybuje mezi 20–33 % (38). V roce 2007 van Kerrebroeck et al. zhodnotil výsledky léčbyu 163 nemocných s non-neurogenní dysfunkcí močových cest. Při 5letém sledování byla úspěšnost u pacientů s urgentní inkontinencí 68 %, u nemocných s neobstrukční retencí moči 71 % (39). Brazelli et al. vyhodnotili výsledky 34 studií obsahujících celkem 1827 pacientů. Zlepšení symptomatologie o 50 % a více dosáhlo 80 % nemocných (40). U neurogenních dysfunkcídolních močových cest byly dosud publikovány pouze práce s malými soubory pacientů, ale i zde jsou výsledky povzbudivé. V roce 2010 zhodnotil Kessler et al. 357 pacientů z 26 studií s neurogenní dysfunkcí močových cest. Úspěšnost testovací fáze byla 68 %, ve skupině nemocných s trvalou stimulací dosáhla úspěšnost 92 % při střední době sledování 26 měsíců (41). V posledních letech byly opakovaně publikovány dobré výsledky při léčbě fekální inkontinence. V Evropě mezi schválené indikace patří také dysfunkce střeva, která je dokonce nejčastějším důvodem implantace stimulátoru. Sakrální neuromodulace je dnes rutinně používaná efektivní neuromodulační metoda, která je již ale metodou invazivní s výskytem komplikací a cenově náročnější.
ZÁVĚR
Metody neinvazivní periferní neuromodulace dolních močových cest jsou efektivní, bezpečné a ekonomicky nenáročné. Přínosem mohou být zejména pro nemocné, kde došlo k selhání či intoleranci léčby první linie. Jejich použití bychom měli zvážit vždy před indikací invazivních metod. S použitím implantabilních systémů stoupá ekonomická náročnost léčby. Snížení výskytu komplikací lze předpokládat s rozvojem miniinvazivních technik implantace a dalším technologickým zdokonalením přístrojů. Detailnější znalost mechanismu účinku neuromodulace snad v budoucnu umožní přesněji definovat pacienta, který bude mít z léčby prospěch, a předpovědět míru jeho odpovědi na léčbu. Dosud nebyly provedeny randomizované studie porovnávající jednotlivé neuromodulační metody či hodnotící přínos jejich kombinování. Nebyl zhodnocen efekt bilaterální léčby v případě párových lokalit. U některých metod nebyla standardizována léčebná schémata ani stanoveny optimální parametry elektrického impulzu. Dosavadní výsledky neuromodulace neurogenních dysfunkcí dolních močových cest vybízejí k provedení studií na větších souborech pacientů.
Práce byla podpořena grantem IGA MZ ČR NT 11409.
Došlo: 2. 11. 2011.
Přijato: 12. 1. 2012.
Kontaktní adresa:
MUDr. Rejchrt Michal
Urologická klinika 2. LF UK a FN Motol
V Úvalu 84, 150 00 Praha 5
e-mail: mirejchrt@seznam.cz
Sources
1. Milson I. Epidemiology of urinary and faecal incontinence and pelvic organ prolapse. 4th International Consultation on Incontinence (Paris, 2008) 4th ed. Plymouth: Health Publications Ltd. 2009, 35–112.
2. Houdek M. Neuromodulace. Praha: Grada Publishing 2007, 27–38.
3. Doležel J, Cejpek P, Miklánek D. Sakrální deaferentace a neurostimulace předních kořenů míšních v léčbě neuropatického močového měchýře u pacientů s kompletní transverzální míšní lézí - první klinické zkušenosti. Rozhl Chir 2002; 81 : 203–209.
4. Vodusek DB, Light JK, Libby JM. Detrusor inhibition induced by stimulation of pudendal nerve aff erents. Neurourol Urodyn 1986; 5 : 381–389.
5. Shafi k A. A study of the kontinence mechanism of the external urethral sphincter with identifi cation of tPráce byla podpořena grantem IGA MZ ČR NT 11409.he voluntary urinary inhibition refl ex. J Urol 1999; 162 : 1967–1971.
6. Caldwell KP. Th e electrical control of sphincter incompetence. Lancet 1963; 2 : 174–175.
7. Godec C, Cass AS, Ayala GF. Bladder inhibition with functional electrical stimulation. Urol 1975; 6 : 663–666.
8. Fall M, Erlandson BE, Nilson AE, et al. Long-term intravaginal electrical stimulation in urge and stress incontinence. Scand J Urol Nephrol 1977; 44(Suppl): 55–63.
9. Primus G, Kramer G. Maximal external electrical stimulation for treatment of neurogenic or non-neurogenic urgency and/or urge incontinence. Neurourol Urodyn 1996; 15 : 187–194.
10. Lamhut P, Jackson TW, Wall LL. Th e treatment of urinary incontinence with electrical stimulation in nursing home patients: a pilot study. J Am Geriatr Soc 1992; 40 : 48–52.
11. Geirsson G, Fall M. Maximal functional electrical stimulation in routine practice. Neurourol Urodyn 1997; 16 : 559–565.
12. Nakamura M, Sakurai T. Bladder inhibition by penile electrical stimulation. Br J Urol 1984; 56 : 413–415.
13. Wheeler JS, Walter JS, Zaszczurynski PJ. Bladder inhibition by penile nerve stimulation in spinal cord injury patients. J Urol 1992; 147 : 100–103.
14. Madersbacher H, Kiss G, Mair D. Transcuataneous electrical stimulation of the pudendal nerve for treatment of detrusor overactivity. J.Neurourol Urodyn 1995; 14 : 501–502.
15. Spinelli M, Malaguti S, Giardiello G. A new minimaxy invasive procedure for pudendal nerve stimulation to treat neurogenic bladder: description of the method and preliminary data. Neurourol Urodyn 2005; 24 : 305–309.
16. Peters KM, Feber KM, Bennett RC. Sacral versus pudendal nerve stimulation for voiding dysfunction: a prospective, single-blinded, randomized, crossover trial. Neurourol Urodyn 2005;
24 : 643–647.
17. Peters KM, Killinger KA, Boguslawski BM, et al. Chronic pudendal neuromodulation: expanding available treatment options for refractory urologic symptoms. Neurourol Urodyn
2010; 29(7): 1267–1271.
18. Fall M, Carlsson CA, Erlandson BE. Electrical stimulation in interstitial cystitis. J Urol 1980; 123 : 192–195.
19. Hasan ST, Robson WA, Pridie AK, et al. Transcutaneous electrical nerve stimulation and temporary S3 neuromodulation in idiopathic detrusor instability. J Urol 1996; 155 : 2005–2011.
20. Walsh IK, Johnston RS, Keane PF. Transcutaneous sacral neurostimulation for irritative voiding dysfunction. Eur Urol 1999; 35 : 192–196.
21. Stoller, M. Needle stimulation (through the skin) for the treatment of incontinence. Quality care 1988; 16 : 1–4.
22. Chang PL. Urodynamic studies in acupuncture for women with frequency, urgency and dysuria. J Urol 1988; 140 : 563–566.
23. Govier FE, Litwiller S, Nitti V, et al. Percutaneous aff erent neuromodulation for the refraktory overactive bladder: results of a multicenter study. J Urol 2001; 165 : 1193–1198.
24. van Balken MR, Vandoninck V, Messelink BJ, et al. Percutaneous tibial nerve stimulation as neuromodulative treatment of chronic pelvic pain. Eur Urol 2003; 43 : 158–163.
25. Vandoninck V, van Balken MR, Agro EF, et al. Posterior tibial nerve stimulation in the treatment of urge incontinence. Neurourol Urodyn 2003; 22 : 17–23.
26. Krhut J, Mainer K. Stollerova aferentní stimulace v léčbě hyperaktivního měchýře – dvouleté zkušenosti. Urologie pro praxi 2001; 5 : 204–206.
27. Kabay SC. Urodynamic eff ect of acute transcutaneous posterior tibial nerve stimulation in overactive bladder. Neurourol Urodyn 2009; 28(1): 62–67.
28. Amarenco G. Acute urodynamic eff ects of percutaneous posterior tibial nerve stimulation on neurogenic detrusor overactivity in patients with Parkinson‘s disease. J Urol 2003; 169(6):
2210–2215.
29. Peters KM, Carrico DJ, Perez-Marrero RA, et al. Randomized trial of percutaneous tibial nerve stimulation versus sham effi cacy in the treatment of overactive bladder syndrome: Results
from the SUmiT trial. J Urol 2010; 183 : 1438–1443.
30. Peters KM, MacDiarmid SA, Wooldridge LS, et al. Randomized trial of percutaneous tibial nerve stimulation versus extended-release tolterodine: results from the overactive bladder nnovative therapy trial. J Urol 2010; 182 : 1055–1061.
31. Gobbi C, Digesu G, Khullar V, et al. Percutaneous posterior tibial nerve stimulation as an eff ective treatment of refractory lower urinary tract symptoms in patients with multiple sclerosis:
preliminary data from a multicentre, prospective, open label trial. Mult Scler 2011; 17(12): 1514–1519.
32. Ebner A, Jiang C, Linström S. Intravesical electrical stimulation – an experimental analysis of the mechanism of action. J Urol 1992; 148(3): 920–924.
33. Jiang CH, Lindström S, Mazieres L. Segmental inhibitory control of ascending sensory information from bladder mechanoreceptors in cat. Neurourol Urodyn 1991; 10 : 286.
34. Kiss G, Madersbacher H, Poewe W. Cortical evoked potentials of the vesicourethral junction a predictor for the outcome of intravesical electrostimulation in patients with sensory and motor
detrusor dysfunction. World J Urol 1998; 16 : 308.
35. Kaplan WE. Intravesical electrical stimulation of the bladder. Urol 2000; 56(1): 2–4 [Pro. Editorial].
36. Decter RM. Intravesical electrical stimulation of the bladder. Urol 2000; 56(1): 2–4 [Contra. Editorial].
37. Risi O, Spinelli M, Sandri S, et al. Is intravesical electrical stimulation a satisfactory therapy in overactive bladder? Our experience in 162 patients. Neurourol Urodyn 2000; 19(4): 422–423.
38. Starkman JS, Wolter CE, Scarpero HM, et al. Management of refractory urinary urge incontinence following urogynecological surgery with sacral neuromodulation. Neurourol Urodyn
2007; 26(1): 29–35.
39. van Kerrebroeck PE, van Voskuilen AC, Heesakkers JP, et al. Results of sacral neuromodulation therapy for urinary voiding dysfunction: outcomes of a prospective, worldwide clinical
study. J Urol 2007; 178(5): 2029–2034.
40. Brazelli M, Murray A, Fraser C. Effi cacy ans safety of sacral nerve stimulation for urinary urge incontinence: a systematic review. J Urol 2006; 175(3): 835–841.
41. Kessler TM, Framboise D, Trelle S, et al. Neuromodulation for neurogenic lower urinary tract dysfunction: Systematic review and meta-analysis. Eur Urol 2000; 58(6): 53–62.
Labels
Paediatric urologist Nephrology Urology
Article was published inCzech Urology

2012 Issue 1-
All articles in this issue
- Využití neuromodulace v léčbě dysfunkcí dolních močových cest
- Do akej miery je aktívne sledovanie malých nádorov obličiek bezpečná stratégia?
- Srovnání výsledků miniinvazivní léčby ženské stresové inkontinence metodou AjustTM a MiniArcTM
- Urologické komplikace po zavedení močového katétru po náhradách velkých kloubů u mužů
- Matematické modelování deformace penisu při induratio penis plastica po terapii rázovými vlnami (SWT)
- Možnosti intervenční radiologie při léčbě nádorů ledvin
- Korelace výsledku pozitronové emisní tomografie a nálezu při resekci reziduálních lézí po chemoterapii neseminomových germinálních nádorů
- Stanovení exprese SHB v tkáni karcinomu prostaty: využití v diagnostice a prognostice
- Oboustranná adrenalektomie – u pacientů s Cushingovým syndromem při ektopické sekreci ACTH
- Czech Urology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Urologické komplikace po zavedení močového katétru po náhradách velkých kloubů u mužů
- Do akej miery je aktívne sledovanie malých nádorov obličiek bezpečná stratégia?
- Využití neuromodulace v léčbě dysfunkcí dolních močových cest
- Oboustranná adrenalektomie – u pacientů s Cushingovým syndromem při ektopické sekreci ACTH
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

