-
Medical journals
- Career
Péče o děti s infantilním hemangiomem léčené systémově propranololem
Authors: J. Mališ 1; A. Mišove 1; S. Zimová 1; K. Bláhová 2; V. Stará 2; N. Krejčová 2; M. Kynčl 3; M. Dvořáková 3; B. Prosová 3; M. Šimsová 4; R. Katra 5; A. Sukop 6
Authors‘ workplace: Klinika dětské hematologie a onkologie 2. LF UK a FN Motol, Praha 1; Pediatrická klinika 2. LF UK a FN Motol, Praha 2; Klinika zobrazovacích metod 2. LF UK a FN Motol, Praha 3; Klinika dětské chirurgie 2. LF UK a FN Motol, Praha 4; Klinika ušní, nosní a krční 2. LF UK a FN Motol, Praha 5; Klinika plastické chirurgie 3. LF UK a FN Královské Vinohrady, Praha 6
Published in: Čes-slov Pediat 2020; 75 (5): 285-291.
Category: Review
Overview
S infantilním hemangiomem (IH) se můžeme setkat u 5 až 10 % dětí do jednoho roku věku. Tento benigní cévní tumor charakterizují tři fáze růstu – proliferace, stagnace a involuce. Moderní systémová terapie neselektivním β-blokátorem (propranololem) nabízí dětem účinné, bezpečné a neinvazivní řešení. Pro efektivitu terapie je maximálně klíčové načasování zahájení terapie v proliferační fázi.
Klíčová slova:
infantilní hemangiom – propranolol
ÚVOD
Infantilní hemangiomy (IH) jsou benigní nádory, se kterými se v dětském věku setkáváme nejčastěji [1]. IH jsou součástí každodenní praxe všech lékařů, kteří ošetřují děti, především novorozence a kojence. V naprosté většině se jedná o nevýznamné afekce (obr. 1), ale přibližně jedna desetina z nich vyžaduje pozornost nebo léčbu, protože jsou rozsáhlé (obr. 2, 3) nebo život ohrožující, případně mohou způsobovat funkční (obr. 4, 5, 6) či závažné kosmetické obtíže (obr. 7), nebo je jejich povrch sekundárně změněn (obr. 8). Skutečnost, že významná část IH má schopnost spontánní involuce, způsobuje, že se některé závažné hemangiomy neléčí. Řešení závažného rezidua hemangiomu se začne hledat v době, kdy účinnou systémovou léčbu již nelze použít. Cílem tohoto sdělení je upozornit na typy a formy IH, které jsou indikovány ke včasnému vyšetření a systémové léčbě.
Image 1. Nevýznamný hemangiom.
Insignificant hemangioma.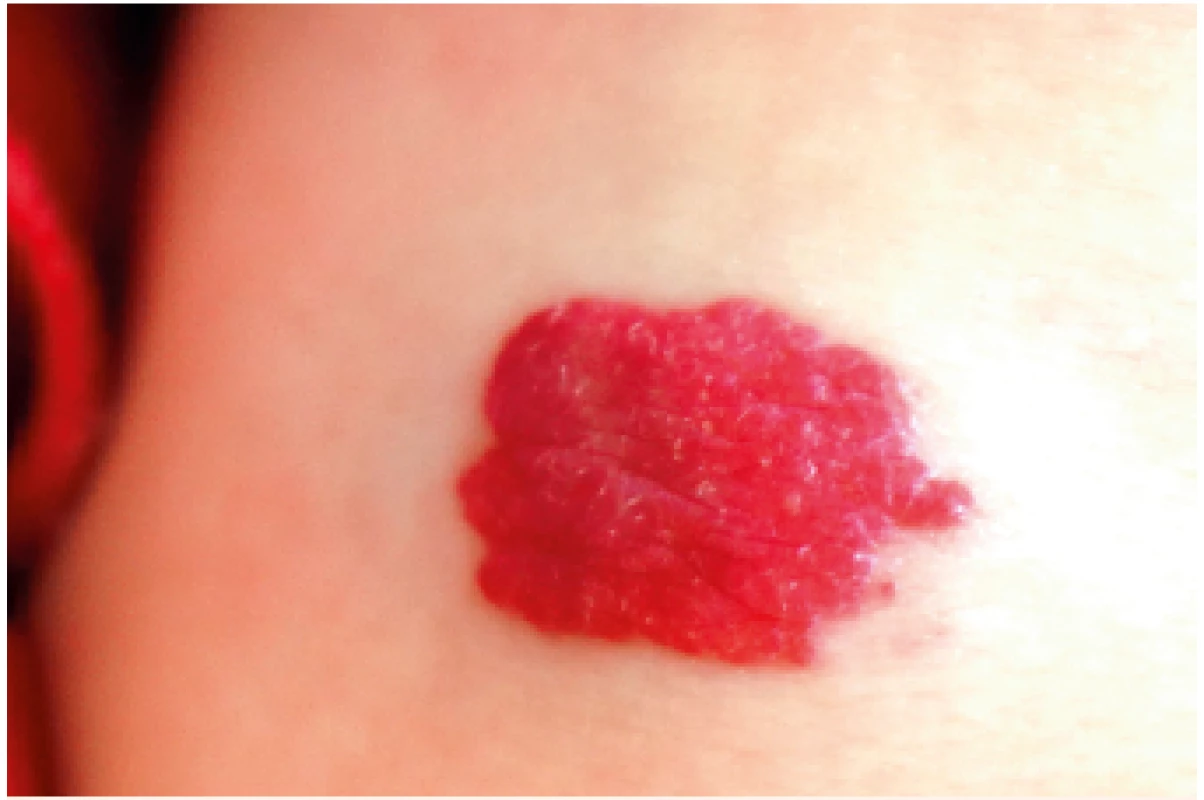
Image 2. Rozsáhlý IH krku a boltce.
Extensive neck and ear IH.
Image 3. Rozsáhlý IH dolní končetiny.
Extensive lower limb IH.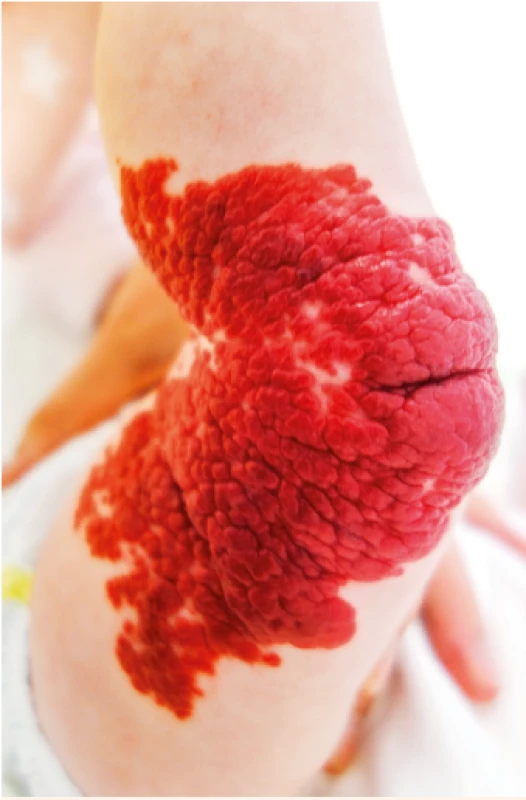
Image 4. Hluboký IH horního víčka.
Deep IH of the upper eyelid.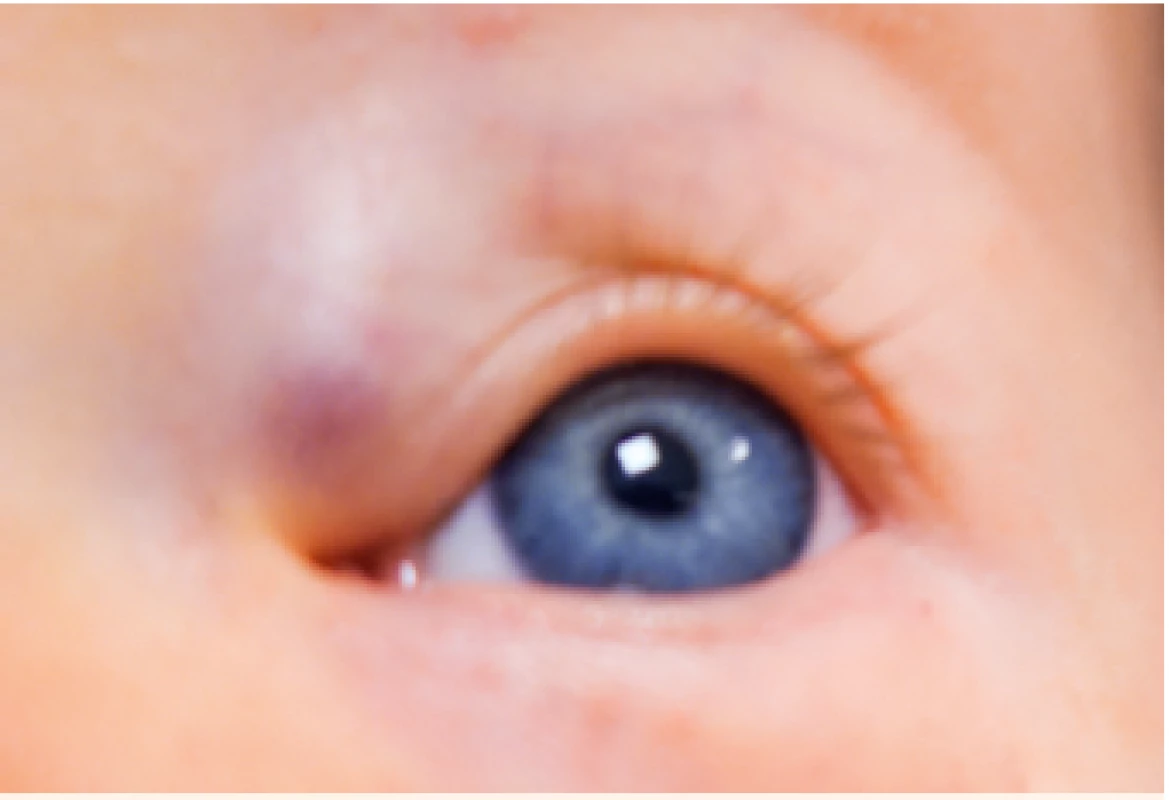
Image 5. Smíšený IH na glans penis.
Mixed IH of the glans penis.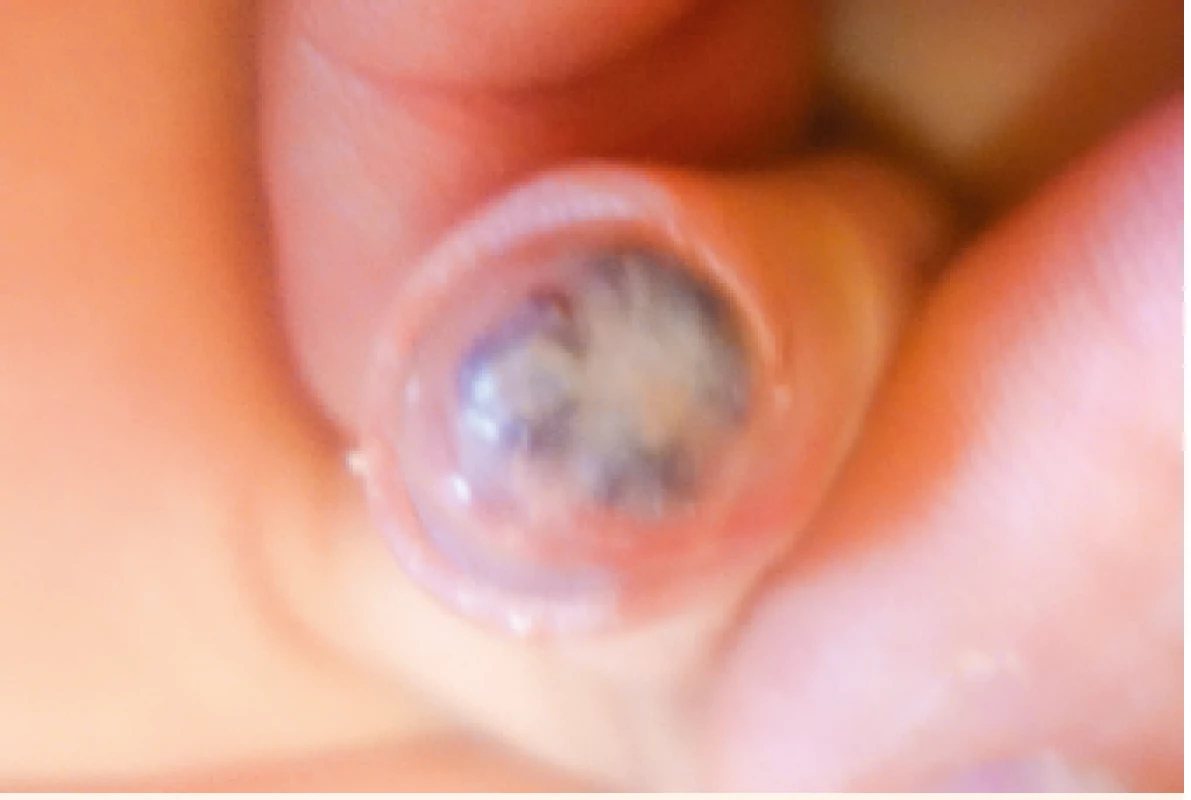
Image 6. Smíšený IH v oblasti parotis.
Mixed parotid gland IH.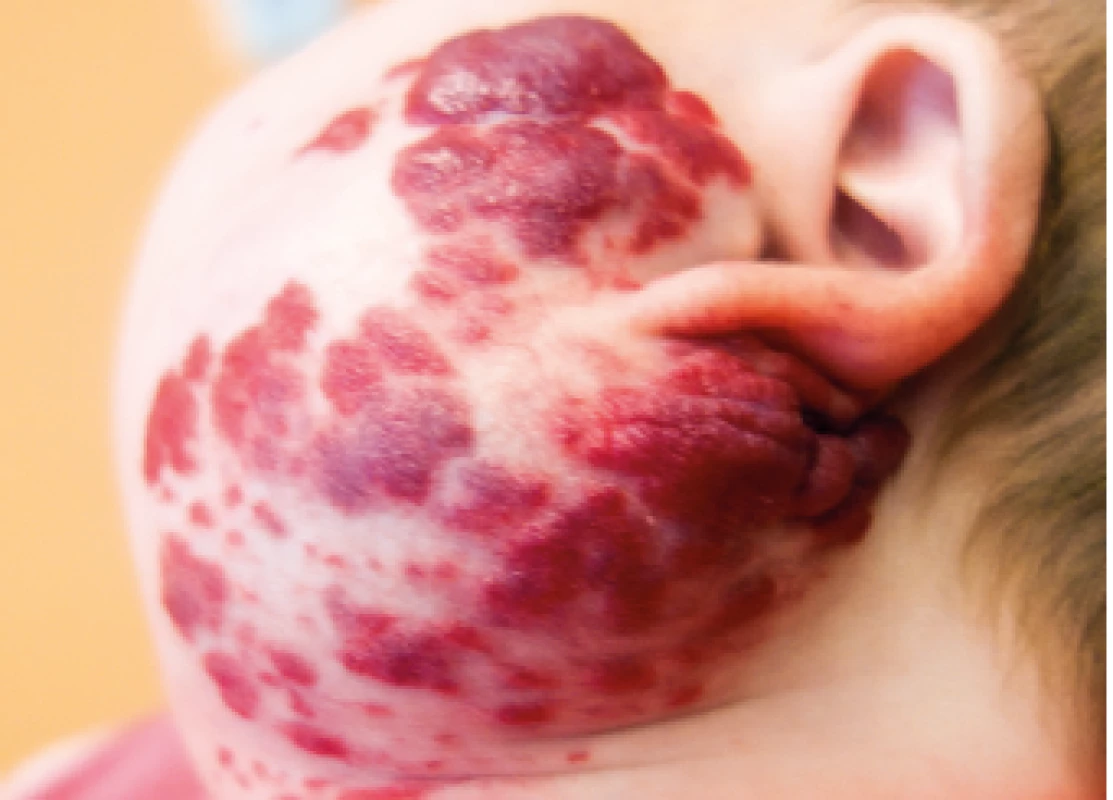
Image 7. Smíšený IH v oblasti mléčné žlázy ohrožující její budoucí vývoj.
Mixed mammary gland IH endangering its future development.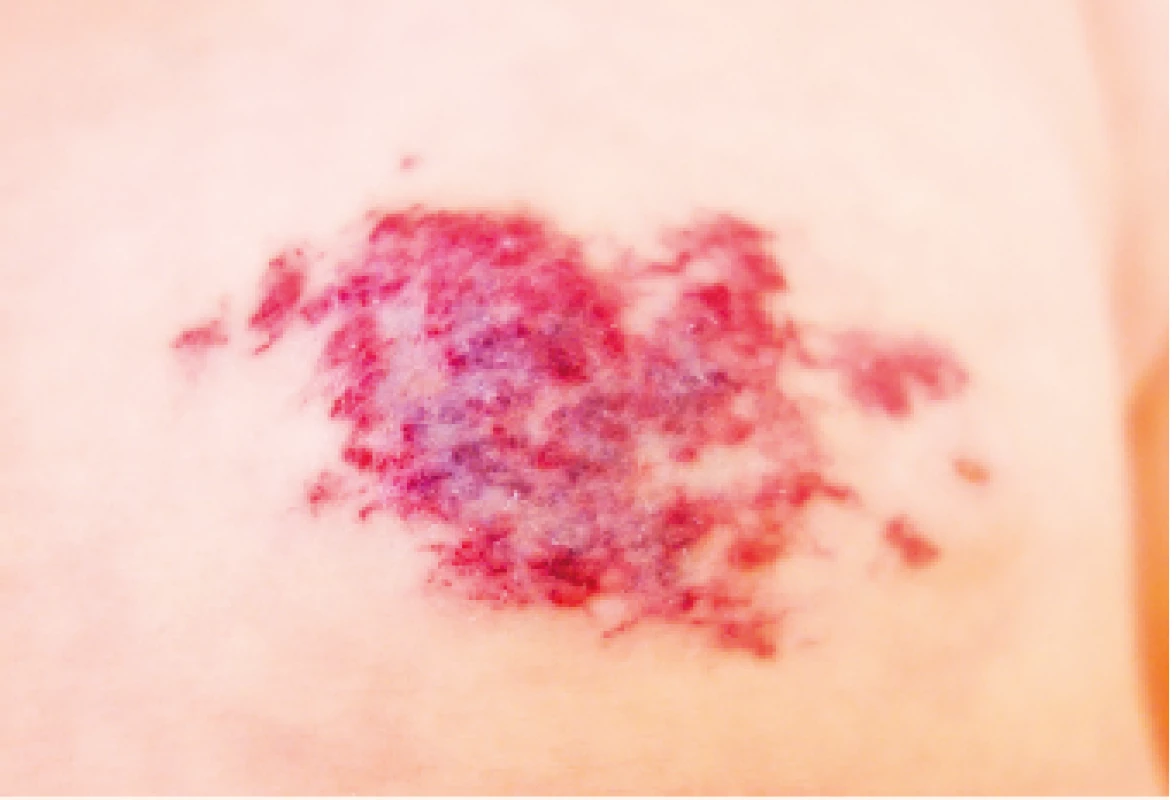
Image 8. Sekundárně změněný povrch IH.
Secondarily altered surface of IH.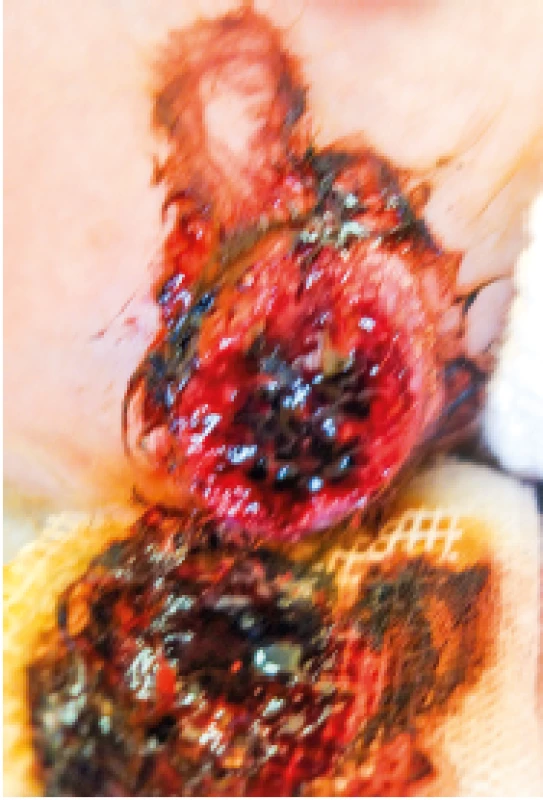
Infantilní hemangiomy vznikají proliferací endoteliálních buněk kapilár. Biologickým chováním jde o benigní nádory charakterizované typickým vývojem v čase. Obvykle se objevují v prvním až druhém týdnu života, avšak nikoliv po 12. týdnu. Nejrychlejší růst (fáze proliferace) je patrný v prvních 12 týdnech života a tato rychlost postupně klesá mezi 4.–6. měsícem života. Až 80 % IH dosahuje své definitivní velikosti koncem 4. měsíce věku. Avšak některé segmentální a hluboké hemangiomy, např. v oblasti parotis, vykazují růstovou aktivitu i ve 2. až 3. roce života. Po proliferační fázi následuje klidové stadium (stagnace) trvající několik měsíců, které postupně přechází v involuci (graf 1). Až 90 % IH spontánně involuje mezi 2. až 6. rokem věku. Některé hluboké nebo smíšené hemangiomy však involují pomaleji a delší dobu, a to až do 8. nebo 9. roku [2]. Involuce ovšem neznamená, že hemangiom vymizí bez jakéhokoliv rezidua (teleangiektázie, fibrózně-tuková tkáň, atrofie kůže; obr. 9, 10, 11 [3].
Graph 1. Schéma vývoje infantilního hemangiomu. 
Image 9. Reziduální teleangiektázie po involuci IH.
Residual telangiectasia after IH involution.
Image 10. Fibrózně ztukovatělé reziduum po spontánní involuci neléčeného IH.
Fibrous-fatty residuum after spontaneous IH involution without any treatment.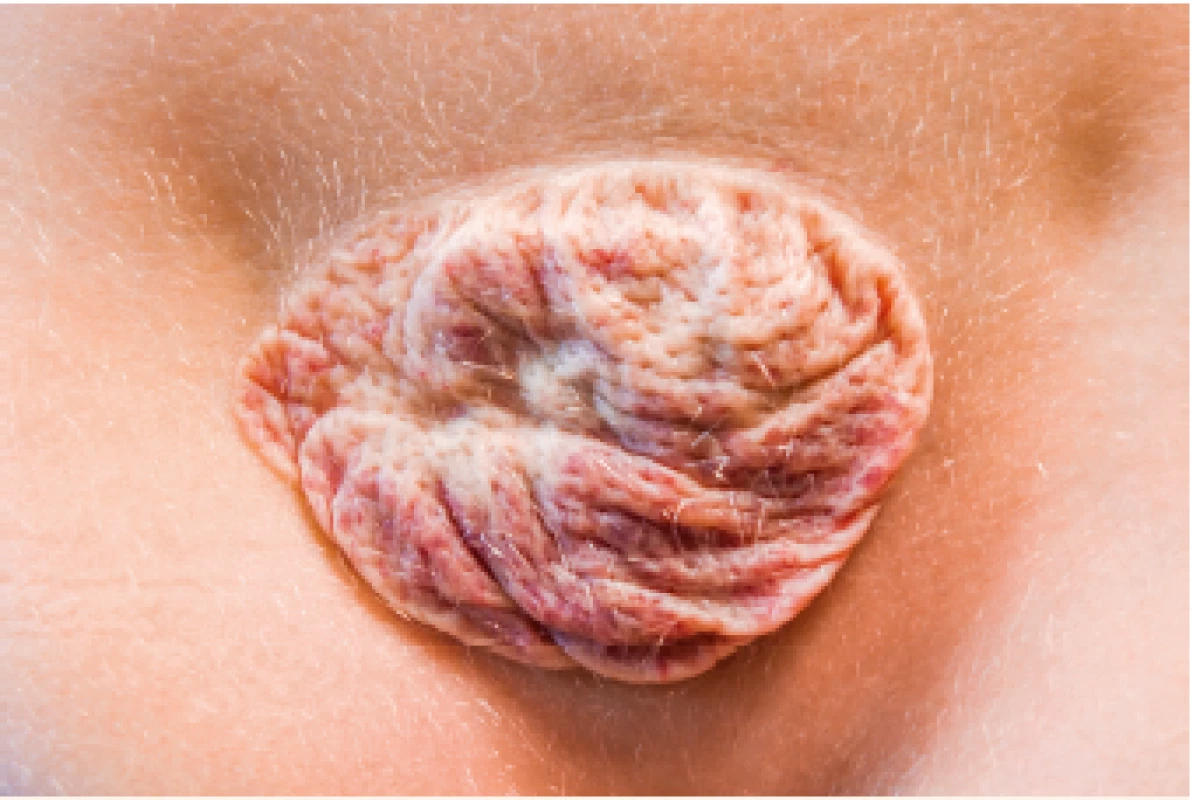
Image 11. Hypopigmentace a teleangiektázie po involuci IH.
Hypopigmentation and telangiectasia after IH involution.
Absolutní indikací k zahájení terapie jsou potencionálně letální a ulcerující IH nebo hemangiomy, které mohou vést k postižení vitálních funkcí. Zahájení léčby si vyžadují také hemangiomy, které mohou potenciálně ohrozit funkční schopnosti dítěte – periorbitální, nazální oblast, v okolí zvukovodů, hluboké a smíšené hemangiomy na krku. Léčba je dále indikovaná u kosmeticky závažných, někdy znetvořujících hemangiomů – obličej, nos, rty, čelo, tváře, ušní boltce [4, 5]. Níže uvedená referenční skóre (obr. 12, 13), která recentně vznikla, mají usnadnit pediatrům rozhodování, kdy odeslat pacienta do specializovaného centra pro léčbu infantilních hemangiomů [6].
Image 12. Schéma indikace do centra pro hemangiomy, str. 1.
The indication scheme for the IH center investigation, p. 1.
Image 13. Schéma indikace do centra pro hemangiomy, str. 2.
The indication scheme for the IH center investigation, p. 2.
Zvláštní pozornost je nutné věnovat nedonošeným pacientům, a pokud IH neohrožuje vitální funkce, zahajujeme systémovou terapii až po vyřešení komplikací souvisejících s perinatálním obdobím.
IH mohou imitovat různé jiné afekce – od vaskulárních malformací až po závažné stavy, jako jsou například nádory. Při diagnostických nejasnostech je potřeba doplnit vyšetření zobrazovacími metodami (sonografie, magnetická rezonance).
SYSTÉMOVÁ LÉČBA IH
V minulosti se k terapii hemangiomů používaly různé léčebné možnosti. Šlo především o kortikoidy podávané po dobu několika týdnů až měsíců, často ve vysokých dávkách. Dále se používal interferon alfa, někdy i cytostatika (vinkristin), později sirolimus. V roce 2008 publikovala Cristine Labreze překvapivě účinnou terapii hemangiomů systémově podávaným propranololem. Po dalším klinickém zkoušení se systémově podávaný propranolol stal první volbou v léčbě závažných IH, které vyžadují urgentní léčbu [7].
U všech dětí je před zahájením terapie nutné vyšetřit krevní obraz a biochemii včetně glykémie. Dále je u pacientů indikované kardiologické vyšetření a v případě nejasných nálezů, podezření na anatomickou nebo funkční vadu, také echokardiografické vyšetření. U nerizikových kojenců se léčba zahajuje ambulantně nebo za krátké hospitalizace. U pacientů s vyšším rizikem rozvoje nežádoucích účinků, zejména bradykardie a hypoglykémie, se terapie zahajuje vždy za hospitalizace.
Celková denní (cílová) dávka (2–3 mg/kg/den) je rozdělena do dvou denních dávek. U rizikových kojenců je vhodnější podávat maximální denní dávku 2 mg/kg/den.
Při ambulantním zahájení léčby provádějí proškolení rodiče monitoraci tepové frekvence fonendoskopem v průběhu zvyšování dávky propranololu až do dosažení cílové dávky. Při zahájení terapie za hospitalizace již další monitorace tepové frekvence v domácím prostředí není nutná. Jako prevence hypoglykémie se podává lék vždy při krmení. V případě, že dítě opakovaně zvrací nebo má průjmy, je vhodné terapii přerušit. Léčbu propranololem je nutné okamžitě přerušit, jestliže jsou podávány bronchodilatační léky při respiračním infektu.
Nežádoucí účinky vyplývají z povahy beta-blokátorů. Téměř všechny děti mají v průběhu terapie chladnější akra. Nejčastější závažnější nežádoucí účinek, který můžeme pozorovat až u 10 % pacientů, jsou poruchy spánku. Tomuto lze předejít časnějším podáním večerní dávky. Rozestup mezi dávkami musí být alespoň 9 hodin. Ukončení terapie nemusí probíhat postupným vysazováním léku, ale může být ukončeno ze dne na den. Průměrná délka léčby je 6 měsíců, jedná se však o parametr velmi individuální a řídí se léčebnou odpovědí. U hlubokých a viscerálních hemangiomů může léčba trvat 12 měsíců i déle.
Sonografické vyšetření břicha (při podezření na přítomnost jaterních hemangiomů) je indikováno pouze při klinické hepatomegalii nebo při přítomnosti 5 a více lézí hemangiomů. V ostatních případech toto vyšetření indikováno není. Echokardiografické vyšetření je indikováno u dětí s mnohočetnými a objemnými nádory z důvodu možného oběhového selhání či nedostatečnosti. U těchto dětí by měl být proveden také screening na hypotyreózu. Segmentální hemangiomy na krku a na obličeji mohou být asociovány s cerebrovaskulárními nebo kardiovaskulárními anomáliemi, proto je u těchto lokalizací prováděna MRI mozku. Někdy mohou na přítomnost hemangiomatózy upozornit i klinické příznaky: stridor, kašel, ztráta hlasu u hemangiomů, krvácení do gastrointestinálního traktu, srdeční selhání, dechové obtíže či hypotyreóza [8].
Systémová léčba propranololem nemusí být ve všech případech zárukou úplné regrese infantilního hemangiomu. Pokud však léčba propranololem proběhne ve správný čas (v době proliferace), je případné reziduum řešitelné lokální terapií pomocí chirurgického odstranění, nebo u povrchových hemangiomů laserem. S lokální léčbou reziduí je vhodné vyčkat do mladšího předškolního věku.
Spontánně involující neléčené hemangiomy zanechávají významné reziduum až v 70 % a některé typy IH, např. segmentální, zanechávají reziduum až ve 100 % případů. Rezidua po přirozené neúplné involuci jsou často závažným kosmetickým, ale i funkčním handicapem, který nemusí být vždy řešitelný plastickým chirurgem nebo jiným kosmetickým zákrokem.
Systémovou léčbu IH musíme zahájit do prvních pěti měsíců života dítěte. Nejintenzivnější růst hemangiomů je však v prvních třech měsících života a je statisticky prokázáno, že pokud zahájíme léčbu před dosažením 75. dne života kojence, je naděje na úplné vyléčení takřka 100%, v porovnání s léčbou zahájenou v pozdějším věku (obr. 14). Právě proto bychom neměli vždy jen čekat na spontánní involuci a v případě, že se tak nestane, hledat až posléze nějaké terapeutické řešení. V naprosté většině pak vyšetřujeme pacienta, jenž už není kojencem, ale batoletem se závažným neaktivním reziduem IH, které již nelze systémovou léčbou zásadně ovlivnit (obr. 15, 16, 17).
Image 14. a. Rozsáhlý, včas léčený superficiální IH obličeje (rodiče souhlasí s publikací obrázků jejich dítěte).
Fig. 14a. Extensive superficial face IH treated in time (parents consent with the publication).
Obr. 14b. Rozsáhlý, včas léčený superficiální IH obličeje (rodiče souhlasí s publikací obrázků jejich dítěte).
Fig. 14b. Extensive superficial face IH treated in time (parents consent with the publication).
Obr. 14c. Rozsáhlý, včas léčený superficiální IH obličeje (rodiče souhlasí s publikací obrázků jejich dítěte).
Fig. 14c. Extensive superficial face IH treated in time (parents consent with the publication).
Image 15. IH u osmiměsíčního kojence s významnými involučními změnami, mimo indikační období pro terapii propranololem.
IH in 8-months old infant with significant marks of involution, too old for the propranolol treatment.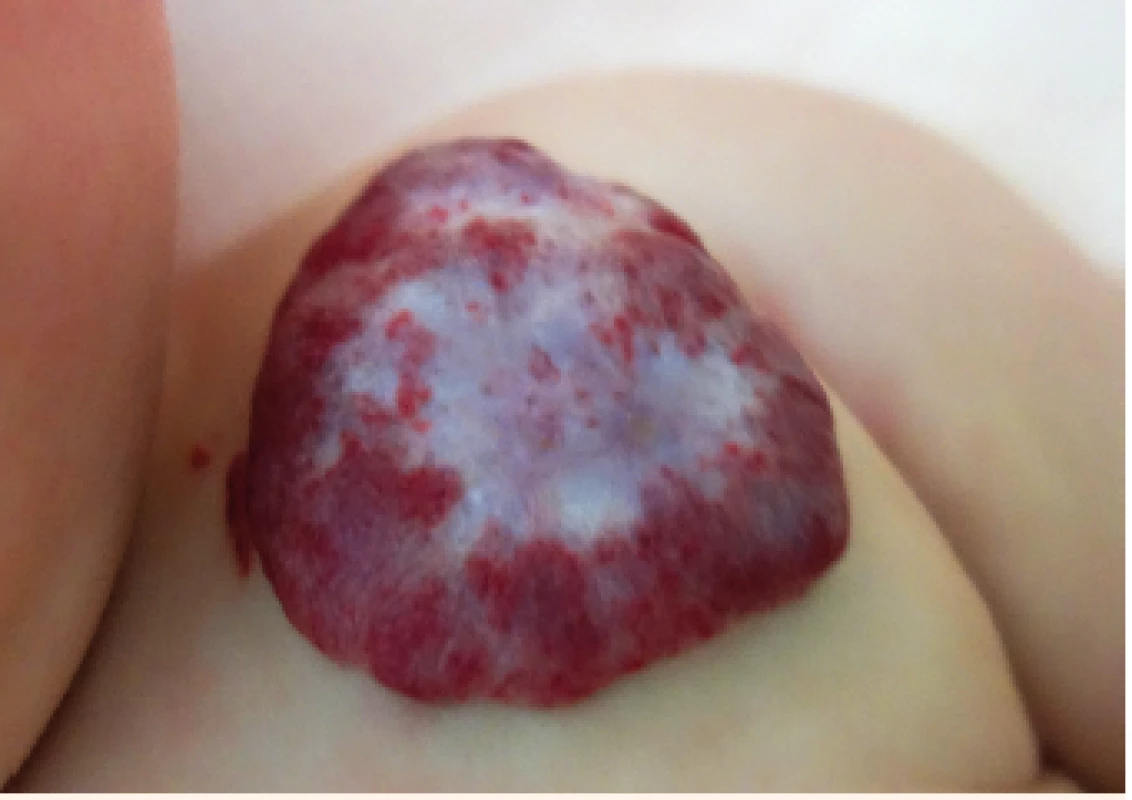
Image 16. Konzervativně neřešitelné reziduum IH (věk 2 roky).
Conservatively untreatable IH residuum (age of 2 years).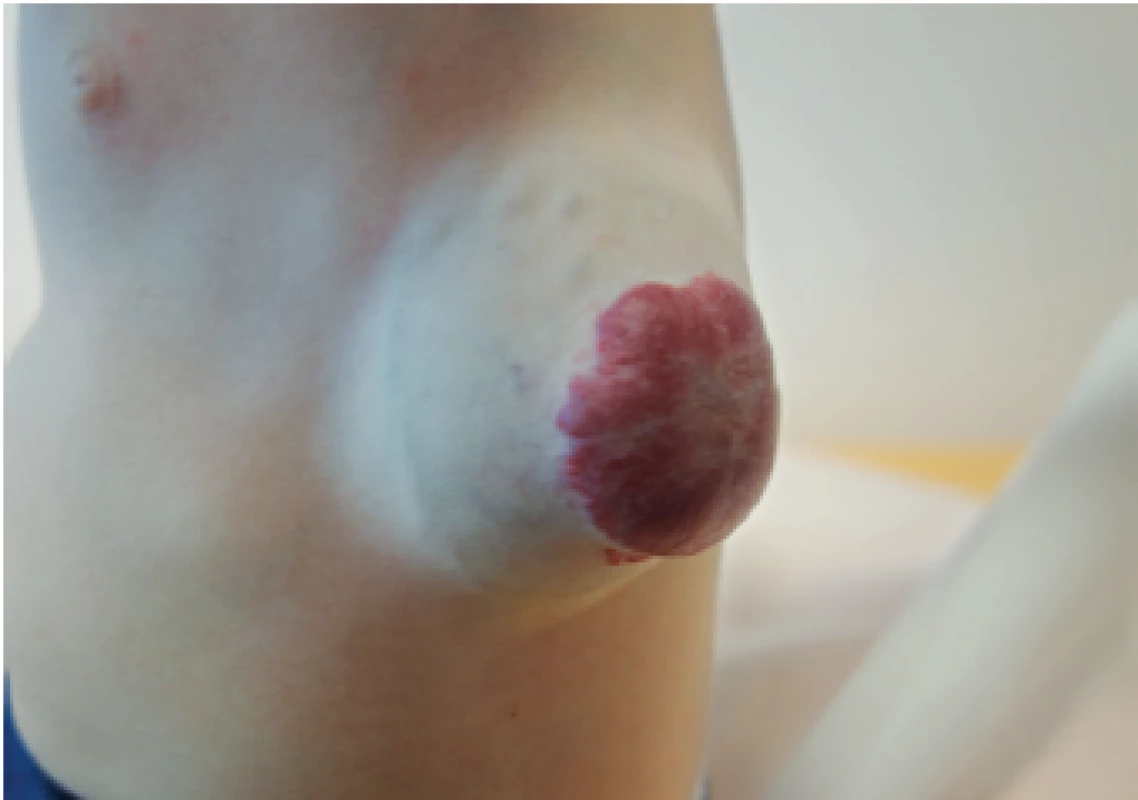
Image 17. Reziduum plastického neléčeného IH (věk 9 měsíců).
Raised untreated IH residuum (age of 9 months).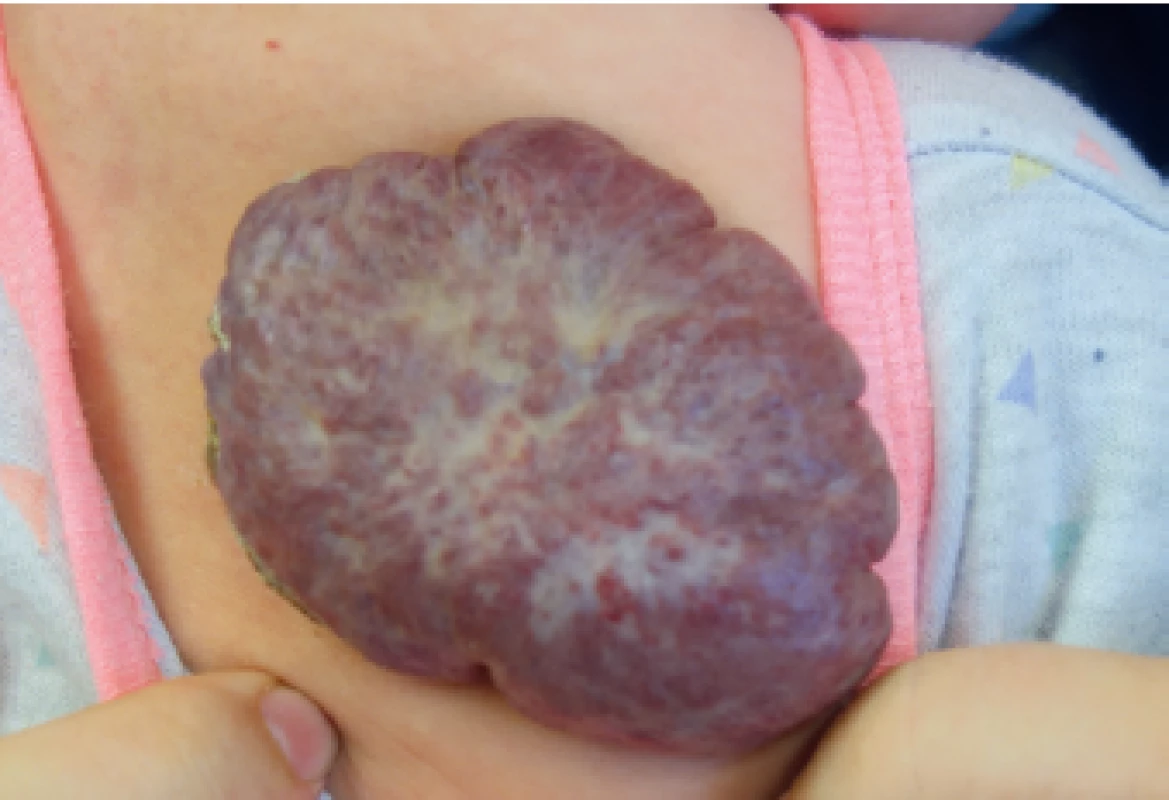
Riziko recidivy hemangiomů je po ukončení léčby propranololem podle dostupné literatury 10–15% [9, 10]. U našich pacientů dosahujeme významně nižší incidenci recidivy do 5 % a zaznamenáváme ji převážně u hlubokých a smíšených hemangiomů, především v oblasti parotis a šíje (obr. 18, 19). Prevencí recidiv je, podle našich zkušeností, včasné zahájení léčby v dostatečné denní dávce při dodržení správné délky léčby. Recidiva obvykle nastává do 6 měsíců od ukončení medikace. Opakované recidivy jsou extrémně vzácné [11]. Pokud má pediatr (v ordinaci PLDD) v péči kojence léčeného propranololem, může být toto dítě standardně očkováno. Mezi léky, které nelze běžně užívat současně se systémově podávaným propranololem, patří blokátory kalciových kanálů, zvláštní pozornost vyžadují antiarytmika a kortikosteroidy, kdy jejich současné užívání je nutné řešit konziliárně.
Image 18. Hluboký hemangiom v oblasti parotis.
Deep parotid gland IH.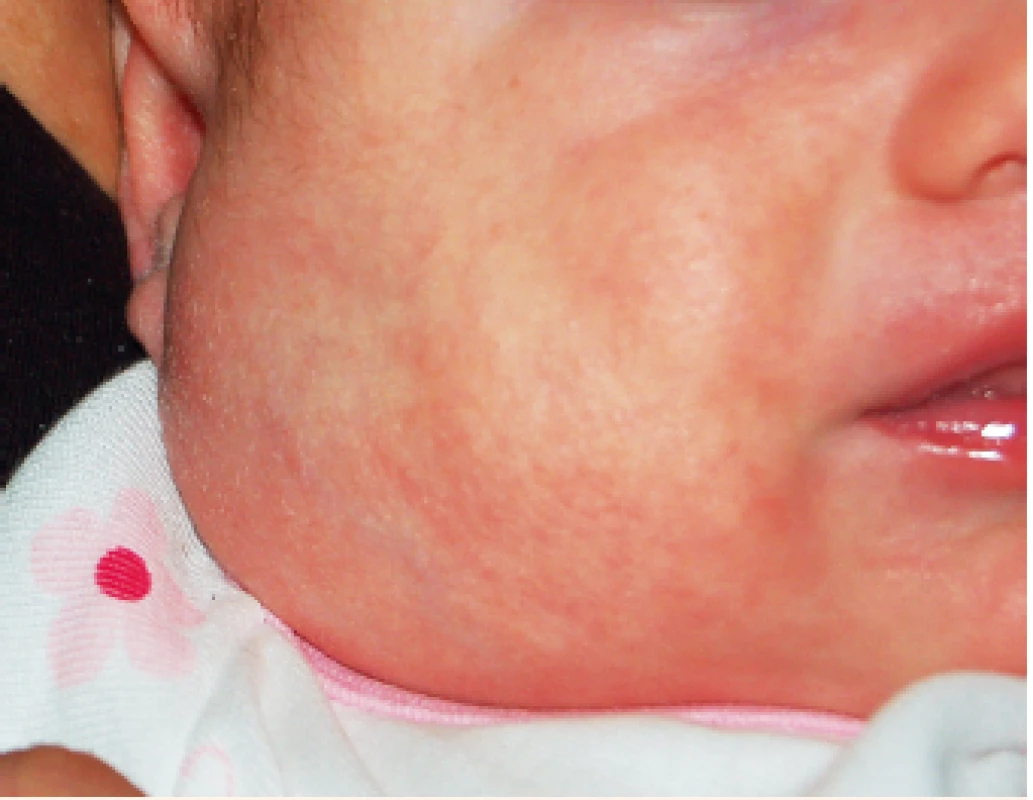
Image 19. Smíšený hemangiom v oblasti šíje.
Mixed nape hemangioma.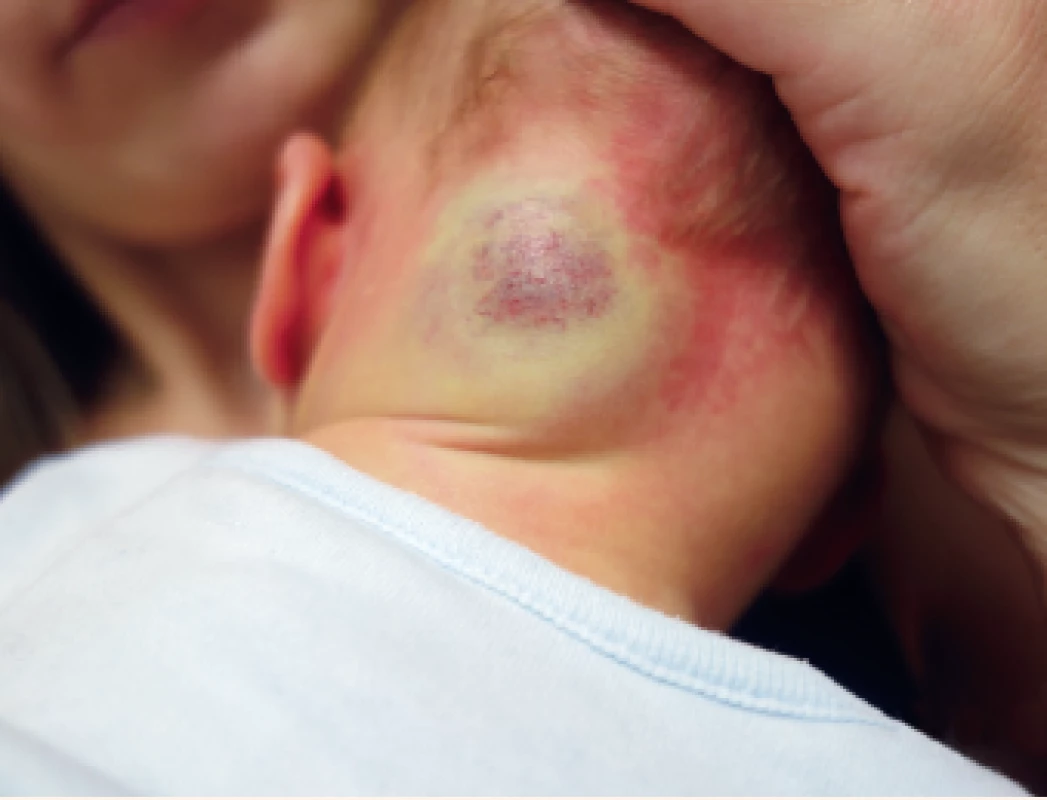
ZÁVĚR
Léčba IH je prováděna v příslušných centrech a při dobré spolupráci s rodiči a pediatrem probíhá nekomplikovaně a účinně. Indikace k zahájení terapie je nutné znát, aby byli pacienti adekvátně a včas odesíláni na pracoviště zabývající se terapií IH. Klíčové je zahájení systémové terapie v době proliferace infantilního hemangiomu. Průměrný optimální věk pro zahájení terapie jsou 4 týdny až 4 měsíce věku dítěte.
Došlo: 22. 6. 2020
Přijato: 3. 7. 2020
MUDr. Josef Mališ
Klinika dětské hematologie a onkologie
2. LF UK a FN Motol
V Úvalu 84
150 06 Praha 5
e-mail: josef.malis@fnmotol.cz
Sources
1. Kilcline C. Infantile hemangiomas: How common are they? A systematic review of the medical literature. Pediatr Dermatol 2008; 25 (2): 168–173.
2. Léauté-Labrèze C. Infantile haemangioma: Part I. Pathophysiology, epidemiology, clinical features, life cycle and associated structural abnormalities. J Eur Acad Dermatol Venereol 2011; 25 (11): 1245–1253.
3. Baselga E. Risk factors for degree and type of sequelae after involution of untreated hemangiomas of infancy. JAMA Dermatol 2016; 152 (11): 1239–1243.
4. Léauté-Labrèze C. A randomized, controlled trial of oral propranolol in infantile hemangioma. N Engl J Med 2015; 372 (8): 735–746.
5. Mališ J, Faberová R, Bučková H, et al. Současné terapeutické možnosti u infantilních hemangiomů. Čes-slov Dermatol 2017; 92 (2): 103–108. ISSN: 0009-0514.
6. Léauté-Labrèze C, Baselga Torres E, et al. The infantile hemangioma referral score: A validated tool for physicians. Pediatrics 2020 Apr; 145 (4): e20191628. doi: 10.1542/peds.2019-1628.
7. Léauté-Labrèze C. Propranolol for severe hemangiomas of infancy. N Engl J Med 2008; 358 (24): 2649–2651.
8. Vredenborg AD. Multiple cutaneous infantile haemangiomas and the risk of internal haemangioma. Br J Dermatol 2013; 169 (1): 188–191.
9. Chang L, Lv D, Yu Z, et al. Infantile hemangioma: factors causing recurrence after propranolol treatment. Pediatr Res 2018; 83 : 175–182.
10. Bagazgoitia L, Hernandez-Martin A, Torrelo A. Recurrence of infantile hemangiomas treated with propranolol. Pediatr Dermatol 2011; 28 : 658–662.
11. Mališ J, Stará V, Bláhová K, et al. Infantilní hemangiomy. Současné léčebné postupy. Čes-slov Pediat 2017; 72 (4): 245–254. ISSN: 0069-2328; 1805-4501
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2020 Issue 5-
All articles in this issue
- Pandemie COVID-19 z pohledu dětské kliniky krajské nemocnice
- Bolesti břicha způsobené retrokaválním ureterem
- Anémie u dětí s nespecifickými střevními záněty
- Péče o děti s infantilním hemangiomem léčené systémově propranololem
- Doporučení pro diagnostiku a léčbu uveitidy asociované s juvenilní idiopatickou artritidou: Česko-slovenská adaptace evropských doporučení SHARE
- Prof. MUDr. Jiří ZEMAN, DrSc. – jubileum
- Zprávy
- Lucia Časnocha Lúčanová: Infekcie novorodencov
- Inhibitory angiotenzin konvertujícího enzymu u dětských kardiologických pacientů – současné zkušenosti a praxe
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Prof. MUDr. Jiří ZEMAN, DrSc. – jubileum
- Pandemie COVID-19 z pohledu dětské kliniky krajské nemocnice
- Anémie u dětí s nespecifickými střevními záněty
- Bolesti břicha způsobené retrokaválním ureterem
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

