-
Medical journals
- Career
Desať rokov novorodeneckého skríningu cystickej fibrózy na Slovensku
: S. Dluholucký 1,2; M. Knapková 1; A. Revťáková 1
: Skríningové centrum novorodencov SR, Detská fakultná nemocnica s poliklinikou, Banská Bystrica, Slovensko 1; Slovenská zdravotnícka univerzita v Bratislave, Fakulta zdravotnictva SZÚ, Banská Bystrica, Slovensko 2
: Čes-slov Pediat 2019; 74 (7): 387-391.
:
Autori prezentujú 10-ročné skúsenosti so skríningom cystickej fibrózy (NSCF) na Slovensku (2009–2018), pomocou novej súpravy neo-IRT ILMA.
Metodika: Počas testovania súpravy (2007) až 31 % detí s vysokou hladinou IRT bolo rómskeho etnika. Pre riziko neprimerane vysokého percenta falošnej pozitivity si to vyžiadalo stanovenie vyššieho cut-off limitu pre rómskych novorodencov formou prospektívnej štúdie porovnávajúcej hladiny IRT1a IRT2 v majoritnom (M) a rómskom (R) etniku. Po ich zavedení do praxe sú vyhodnotené výsledky 10 rokov NSCF.
Výsledky: Na súbore 8742 novorodencov M skupiny a 1500 novorodencov R skupiny boli zistené vysoko štatisticky signifikantné rozdiely hladín IRT (p <0,001) a boli stanovené cut-off limity IRT1 = 72 ng/ml, IRT2 = 60 ng/ml pre M skupinu a IRT1 = 84 ng/ml, IRT2 = 72 ng/ml pre R skupinu. Za 10 rokov NSCF bolo celkom vyšetrených 558 938 novorodencov (85,2 % M a 14,8 % R skupiny), percento pozitivity IRT (recall rate) bolo napriek vyššiemu cut-off limitu vyššie v skupine R (0,48 % vs. 0,28 %). Celkom bolo zachytených a potvrdených 75 prípadov CF, všetky v skupine M, ani jeden prípad nebol zistený u rómskeho novorodenca. Celková incidencia CF v súbore bola 1 : 7452, prepočítane na M populáciu 1 : 5110 živonarodených detí.
Závery: Etnicky vykonávaný NSCF potvrdil potrebu rozdielnych cut-off limitov IRT vzhľadom na jeho vyššie hodnoty u rómskeho etnika, ako aj prakticky nulový výskyt CF v 10-ročnom súbore rómskeho etnika na Slovensku. Tento prístup môže v etnicky zmiešaných populáciách znížiť neprimerane vysoký recall a tým stres rodiny etnika s vyššími IRT a posunúť aj poznatky o reálnej incidencii CF v daných podmienkach.
Klíčová slova:
cystická fibróza – rómske etnikum – etnický novorodenecký skríning
ÚVOD
Základnou podmienkou zaradenia tej ktorej vrodenej, genetickej chyby do novorodeneckého skríningu (NS) je splnenie tzv. Wilsonových-Jungnerových (W-J) kritérií [1, 2]. V prvom rade je to jej závažnosť, vysoká incidencia a liečiteľnosť. Musí byť dostupný skríningový test, ktorý je jednoduchý, lacný, akceptovateľný laickou aj odbornou verejnosťou. Musí mať takmer sto percentnú senzitivitu (nulové riziko úniku postihnutých detí), čo najvyššiu špecificitu (minimum falošne pozitívnych výsledkov – potrebu ďalších vyšetrení). Nezanedbateľná je aj ekonomická efektívnosť – či už samotného NS, ale aj následného manažmentu a liečby. Uvedené požiadavky od počiatku splňovali fenylketonúria (FKU), kongenitálna hypotyreóza (KH), ktoré sú v NS v 70 % štátov EÚ, kongenitálna adrenálna hyperplázia (CAH) v 12 štátoch EÚ [1–3] a čoraz širšie spektrum genetických metabolických porúch (DMP), diagnostikovaných pomocou tandemovej hmotnostnej spektrometrie (MS/MS) [4, 5].
Novorodenecký skríning cystickej fibrózy (NSCF) sa stal aktuálnym od zavedenia vyšetrenia imunoreaktívneho trypsinogénu (IRT) v suchej kvapke krvi (ILMA). K splneniu kritérií pre NSCF prispeli aj výsledky komplexnej liečby CF, zásadne zlepšujúce prognózu kvality života a prežitia, hlavne pri jej včasnom zahájení [6–8]. V roku 2004 NSCF realizovalo 6 štátov EÚ a v ďalších 6 prebiehali pilotne štúdie [9]. NSCF je založený na stanovení hladiny IRT. Pozitívne nálezy (suspektné z CF – tzv. recall) sa verifikujú vyšetrením genetickej mutácie DNA (PCR, DNA sekvenácia) a vyšetrením hladiny chloridov v pote (potný test).
Schémy recall vyšetrení sú rôzne: Najjednoduchšou je schéma IRT1 - IRT2 - Cl-. Používané sú však aj postupy IRT1 - DNA - IRT2 - Cl- a IRT1 - DNA - Cl- [10–12]. Prvý model ponecháva DNA diagnostiku až po potvrdení diagnózy CF. Pretože PCR-DNA analýza nepokrýva všetky možné mutácie CFTR, definitívna diagnóza CF sa robí vždy stanovením chloridov v pote. Skríningové centrum novorodencov SR Detskej fakultnej nemocnice s poliklinikou Banská Bystrica (SCN SR) sa v spolupráci s firmou Immunotech podieľalo na vývoji diagnostického kitu IRTDBS a v roku 2007 testovalo jeho parametre a model NSCF v prospektívnej štúdii. Získané výsledky a poznatky, včítane 10 rokov celoplošného NSCF na Slovensku, sú predmetom tohto zdelenia.
MATERIÁL A METODIKA
- A. Testovanie súpravy neo-IRT ILMA a úvodný NSCF
Stanovenie hladiny IRT je na princípe chemoimunoluminiscencie (ILMA), používanom aj pri iných skríningových analýzach zo suchej kvapky krvi [3, 5]. Pilotná štúdia bola realizovaná v čase 1. 5.–4. 10. 2007 so stanovenou strednou hodnotou IRT negatívnych prípadov 24,22 ng/ml. Hranicou pozitivity testu nad 99,5 percentil je hodnota 100 ng/ml. Ako skríningová hraničná hodnota pozitivity v prvom odbere (cut-off limit) bola stanovená hodnota IRT1 90 ng/ml, a o 10 ng/ml menej v druhom odbere – IRT2. Odber bol štandardne robený 4. deň po narodení, protokol údajov a kódovanie zostalo bez zmien [3]. V rozmedzi IRT1 90–130 ng/ml sa vyžiada a vyšetruje druhá vzorka IRT2 („studený recall“). Dieťa sa nahlasuje regionálnemu centru diagnostiky a liečby CF, ktoré dieťa komplexne vyšetruje, včítane overenia diagnózy potným testom. Ak je prvý výsledok IRT1 nad 130 ng/ml, značí to „horúci recall“ s priamym avízom do diagnostického centra, ktoré dieťa predvolá, vyšetruje a stanovuje čím skôr definitívnu diagnózu (vč. DNA analýzy). SCN SR vyšetruje výlučne IRT1 a IRT2 skríningové testy a pozitívne prípady nahlasuje regionálnym CF recall pracoviskám detských fakultných nemocnic: NÚDCH Bratislava (západ), DFNsP Banská Bystrica (stred) a DFNsP Košice (východ). Ďalší manažment (diagnostika, liečba, sledovanie) je realizovaný štandardným postupom – výsledky sú hlásené späť na SCN SR.
- B. Etnický NSCF
V priebehu testovania súpravy v zmysle bodu A bolo zistené, že až 31 % IRT pozitívnych prípadov vyžadujúcich ďalšie vyšetrenia bolo rómskeho etnika. Uvedená okolnosť si vyžiadala vyhodnotenie hladín IRT1 a IRT2 v priebehu realizovaného NSCF (1. 3.–31. 5. 2010) podľa etnika – väčšinovej – majoritnej (M) populácie a rómskej (R) populácie novorodencov. Na základe vyhodnotenia výsledkov IRT1 a IRT2 u M a R skupiny boli upravené cut-off limity podľa etnika, s použitím robustnej bootstrapovej štatistickej modifikácie t-testu [13]. Označenie rómskeho etnika písmenom „R“ na odberovom papieriku realizovala pri odbere vzorky sestra, na základe fenotypu, mena dieťaťa a iných znakov. Tento postup bol schválený etickou komisiou DFNsP Banská Bystrica a etickou komisiou Ministerstva zdravotníctva SR. Údaj etnika je považovaný za dôverný, použiteľný len pri hodnotení výsledku NS a pri globálnom štatistickom vykazovaní údajov.
- C. Výsledky pravidelného NSCF
Výsledky pravidelného NSCF, realizovaného v čase od 1. 1. 2009 do 31. 12. 2018 sú spracované celkovo a podľa etník M a R. V týchto rokoch bola hodnotená početnosť populácie M a R, záchyt populácie, percento falošnej pozitivity (recall-rate, RR), počty potvrdených prípadov CF s ich genotypmi, ako aj incidencia CF, celková a podľa etník.
VÝSLEDKY
- A. V priebehu 5 mesiacov NSCF bolo vyšetrených 27 974 novorodencov. Z nich bolo v prvom kroku (IRT1) 27 887 (99,67 %) negatívnych, IRT1 pozitívnych bolo 87 detí (0,31 %), z nich 10 detí (0,04 %) splnilo kritériá „horúceho recallu“ (IRT1 nad 130 ng/ml), u 59 detí išlo o „studený recall“. Z týchto detí sa 18 detí nedostavilo na druhý odber – je to únik z vyšetrenia (IRTesc). IRT2 malo vyšetrené 59 detí, z nich bolo 51 negatívnych a 8 pozitívnych. Tieto, spolu s 10 deťmi „horúcim recallom“ absolvovali komplexné vyšetrenie, včítane potného testu. U trinástich z nich bola CF vylúčená, u piatich potvrdená. Prevalencia CF v tomto súbore bola 1 : 5595 novorodencov, percento pozitivity IRT (recall-rate RR) bolo 0,31 %. Počas prešetrenia IRT pozitívnych detí sa ukázalo, že z 87 detí bolo až 27 rómskeho etnika (31 %) a u žiadneho z nich CF nebola potvrdená. Značilo by to, že v rómskom etniku Slovenska by bol viac ako trojnásobný recall v porovnaní s majoritnou populáciou. Táto okolnosť si vyžiadala realizáciu prospektívnej štúdie B.
- B. V priebehu realizovaného NSCF v algoritme bodu A sa v čase od 1. 3.–31. 5. 2010 realizovala štúdia porovnávajúca hladiny IRT u 8742 novorodencov majoritnej (M) a 1500 novorodencov rómskej (R) populácie.
Výsledky štatistického spracovania sú v tabuľke 1, kde rozdiel medzi hladinami IRT1 skupiny M (20,7 ng/ml) a skupiny R (26,3 ng/ml) je vysoko štatisticky signifikantný (p <0,001). Na základe kalkulácie boli stanovené rozdielne cut-off limity pre IRT1 a IRT2 pre majoritné a rómske etnikum, presahujúce 99. percentil spoľahlivosti:
M – IRT1 = 72 ng/ml, R – IRT1 = 84 ng/ml
M – IRT2 = 60 ng/ml, R – IRT2 = 72 ng/ml
- C. Výsledky desať rokov trvania etnického NSCF (2009 až 2018) sú zhrnuté v tabuľke 2. V priebehu desať rokov bolo v NSCF celkom vyšetrených 558 938 novorodencov, čo predstavuje prakticky 100% záchyt narodenej populácie. Od roku 2011 už bola sledovaná etnicita detí (v rokoch 2009–2010 vyšetrených 109 055 detí bez etnického určenia), takže v NSCF bolo v rokoch 2011–2018 vyšetrených 383 289 detí M etnika (85,2 % rokov 2011–2018) a 66 590 detí rómskeho etnika (14,8 %). Počet IRT pozitívnych detí bol celkom 1707 detí (0,3 %) a napriek zvýšeniu cut-off limitu pozitivity v rómskom etniku bolo percento pozitivity takmer dvojnásobné voči majoritnej skupine (0,48 % R vs. 0,28 % M).
Za 10 rokov NSCF bolo celkom potvrdených 75 prípadov CF. Incidencia CF v celom súbore bola 1 : 7452 živonarodených. Pretože však všetkých 75 prípadov CF bolo v majoritnej skupine a ani jedno dieťa v rómskej skupine, reálna incidencia CF je 1 : 5110 majoritnej skupiny, zatiaľ čo incidencia CF v rómskej skupine je nižšia ako 1 : 66 590. Detailné výsledky genotypizácie CF sú uvedené v tabuľke 3. Vyšetrených bolo 67 prípadov zo 75, t.j. 89,3 %. Z nich bolo 33 prípadov ∆F508 homozygótov, 24 prípadov ∆F508 heterozygótov, 10 prípadov boli iné mutácie. Pochopiteľne išlo o prípady CF v majoritnej populácii.
1. Porovnanie priemerných hodnôt a intervalov spoľahlivosti IRT u novorodencov majoritného a rómskeho etnika. 
2. Sumárne výsledky etnického novorodeneckého skríningu cystickej fibrózy v rokoch 2009–2018 na Slovensku. 
1roky 2011–2018
2roky 2009–20183. Výsledky stanovenia genotypov cystickej fibrózy u diagnostikovaných prípadov. 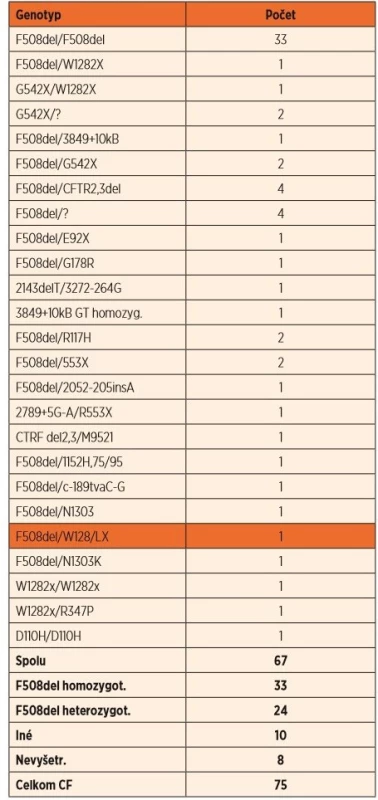
DISKUSIA
Prezentované výsledky NSCF na Slovensku dovoľujú urobiť niekoľko záverov. Prvým z nich je konštatovanie, že použitá a testová súprava neo IRT ILMA je optimálnym testom pre NSCF. Rozsah hodnôt, stabilita cut-off limitov, percento recallu dovoľujú jednoznačný algoritmus interpretácie výsledkov a postup. Osvedčil sa aj model jedného skríningového centra pre všetky DMP, v ktorom sa využije jednotná dokumentácia, vzorky suchej kvapky krvi, kódovanie, prístroje pre diagnostiku, personál a zariadenie. NSCF je tak efektívnou „pridanou hodnotou“ do spektra vyšetrení. Skríningové centrum realizuje len samotný skríning a prvé opakovanie pozitívnych vzoriek (recall IRT2), konfirmáciu diagnózy a následnú starostlivosť robia už špecializované CF pracoviská (regionálne recall centrá), čím sa rozložia ekonomické náklady a dostupnosť zariadenia pre rodičov.
NSCF na rozdiel od FKU, KH, CAH, si nevyžaduje statimovú diagnostiku. Expertná komisia pre NSCF (ECFNBS) považuje za optimum stanovenie diagnózy do konca druhého mesiaca života [14, 15]. Vyšetrením mutácií CFTR PCR-DNA sa v algoritme NSCF dosiahne 100% špecificita, avšak len pre testovanú mutáciu. Aj vtedy je potrebné odlíšiť heterozygótnych nosičov alely od homozygótov [11, 14]. Takže aj v modeloch NSCF s PCR-DNA krokom v diagnostike je, okrem DNA homozygótov [14], koncovým konfirmujúcim testom stanovenie chloridov v pote. Jeho realizácia pomocou pilokarpínovej iontoforézy je možná v cca 5. týždni po narodení. Treba zdôrazniť, že základnou požiadavkou k definitívnej diagnostike patrí okrem zmienených testov včasný odborný klinický pohľad a manažment [6, 8, 4], čo výsostne patrí do kompetencie recall pracovísk, nie skríningového centra. Prezentovaný model NSCF zohľadňuje tieto požiadavky a postup je možné korigovať zavedením vyšetrenia PAP v druhom konfirmačnom kroku.
Celoplošný NS v priebehu viac ako 40 rokov realizácie preukázal jednoznačný prínos v prevencii ireverzibilného poškodenia a zlepšení kvality života [1–3] a predstavuje optimálny model preventívneho zdravotníctva – nielen u novorodencov. Avšak, v priebehu jeho realizácie sa ukázalo, že aj NS nesie so sebou riziká „poškodenia“ [15] a tiež neprimeranej ekonomickej záťaže [16]. V našej štúdii NSCF sa tieto riziká špecificky prejavili v niekoľkých oblastiach. V pilotnej štúdii A sa zistili výrazne vyššie hodnoty IRT u rómskych novorodencov. Vysoký podiel falošnej pozitivity CF by si vyžiadal recall vyšetrenia u cca 31 % rómskych detí, čo by predstavovalo neprimeraný stres pre ich rodiny a vysoké náklady na následné vyšetrenia. Etnický NS s úpravou referenčných hodnôt a cut-off limitov IRT sa ukázal byť efektívnym riešením. Etnický NSCF potvrdil aj neoverený tradovaný údaj, že cystická fibróza je v Slovenskej rómskej populácii výnimočná. Za desať rokov NSCF nebol potvrdený ani jeden prípad CF. Zvýšené hodnoty IRT boli zistené u afro-amerických novorodencov [17] a novorodencov severnej Afriky [18], incidencia CF v jednotlivých etnických skupinách je tiež často rozdielna. Napriek tomu, že je publikovaných niekoľko prác o NSCF v multietnickom prostredí [17, 18], nenašli sme prácu, ktorá by upravovala etnický cut-off limit. Zaujímavou je aj skutočnosť, že v susednom Maďarsku je výskyt CF aj u rómskeho etnika [19]. Fakt, že predbežná prevalencia CF u slovenských novorodencov rómskeho etnika je nižšia ako 1 : 66 000, si zaslúži samostatnú pozornosť.
Demografické štatistiky Slovenska uvádzajú, že majoritná spoločnosť kaukazského (slovensko-maďarského) etnika predstavuje cca 90 % populácie a rómske etnikum cca 10 %. Celková incidencia CF pred zavedením NS sa odhadovala okolo 1 : 2500 (Národný register CF). Incidencia v 10-ročnom NSCF je 1 : 7452 v prepočte na celú populáciu, resp. 1 : 5110 v majoritnom etniku – teda významne nižšia, ako tradovaný údaj. Túto skutočnosť bude potrebné detailne analyzovať, pretože to môže signalizovať, že niektoré varianty CF unikajú z NSCF pomocou IRT a na možnosť výskytu CF treba pomýšľať aj u detí, ktoré boli v NSCF negatívne. Alebo boli doterajšie odhady incidencie CF na Slovensku nepresné. Táto okolnosť bude predmetom ďalšej analýzy.
Prof. MUDr. Svetozár Dluholucký, CSc.
Fakulta zdravotníctva SZÚ
Sládkovičova 21
974 05 Banská Bystrica
Slovenská republika
e-mail: svetozar.dluholucky@szu.sk
Sources
1. Loeber JG, Burgard P, Cornel MC, et al. Newborn screening programmes in Europe: arguments and efforts regarding harmonization. Part 1. J Inherit Metab Dis 2012; May 3.
2. Burgard P, Rupp K, Linder M, et al. Newborn screening programmes in Europe, arguments and efforts regarding harmonization. Part 2. J Inherit Metab Dis 2012; April 28.
3. Dluholucký S, Knapková M. Newborn screening in Slovakia – from 1985 till today. Acta Facul Pharm Univ Commeniannae 2013; Suppl VIII: 32–37.
4. Watson MS, Mann MY, Lloyd-Puryear MA, et al. Newborn screening: Toward a uniform screening panel and system – executive summary. Pediatrics 2006; 117: S296–S307.
5. Dluholucký S, Knapková M. The first results of extended newborn screening in Slovakia – differences between the majority and the Roma ethnic group. Internat J Neonatal Screen (IJNS) 2017; 3 (3): 25–30.
6. Vávrová V, Zemková D, Skalická V, Votava F. Problémy v diagnostice cystické fibrózy – potřeba novorozeneckého screeningu. Čes-slov Pediat 2006; 61 (12): 703–709.
7. Wilcken B, Gaskin K. More evidence for favour newborn screening for cystic fibrosis. Comment. Lancet 2007; 369 : 1146–1147.
8. Ditterová L, Vávrová V, Skalická V, et al. Novorozenecký screening cystické fibrózy (souborný referát). Čes-slov Pediat 2006; 60 (6): 373–378.
9. Loeber JG. Neonatal screening in Europe: the situation in 2004. J Inherit Metab Dis, doi 10 : 2007/s.10545-007-0644-5.
10. Holubová A, Balaščáková M, Skalická V, et al. Novorozenecký screening cystické fibrózy v České republice: závěry pilotní studie. Čes-slov Pediat 2007; 62 (4): 187–195.
11. Balaščáková M, Piskáčková T, Holubová A, et al. Současné metodické postupy a přehled preimplantační, prenatální a postnatální DNS diagnostiky cystické fibrózy v České republice. Čes-slov Pediat 2008; 53 (2): 62–75.
12. Roussey M, Munck A, Dhondt J-L, et al. Four years experience of the French nationwide cystic fibrosis (CF) newborn screening (NBS) strategy and results on more than 2 million births. Database Eurocordis, code 122, IP: 90.32.238.341.
13. Efron B, Tibshirani R. Bootstrap methods for standard errors: Confidence intervals and other measures of statistical accuracy. Statistical Science 1986; 1 : 54–77.
14. Castellani C, Massie J. Emerging issues in cystic fibrosis newborn screening. Curr Opin Pulm Med 2010; 16 : 584–590.
15. Cornel M, Rigter T, Weinreich S, et al. Newborn screening in Europe. Expert opinion document. Assessed 24 Febr. 2012.https://www.iss.it/enmr/prog/cont.php?id=1621&lang=1&tipo=64.
15. Raffle A, Gray M. Screening. Evidence and Practice. Oxford Univ Press, 2007.
16. Simps E, Mugford M, Clark A, et al. Economic implications of newborn screening for cystic fibrosis: a cost of illness retrospective cohort study. Lancet 2007; 369 : 1187–1195.
17. Giusti R, Comber P, Gernmana J, et al. Elevated IRT levels in African--American infants: implications for newborn screening in an ethnically diverse population. Pediat Pulmonol 2008; 43 (7): 638–641.
18. Cheillan D, Vercherat M, Chevaier-Porst F, et al. False-positive results in neonatal screening for cystic fibrosis based on three-stage protocol (IRT/DNA/IRT). Should we adjust IRT cut-off to ethnic origin? J Inherit Metab Dis 2005; 28 (6): 813–818.
19. Endreffy E, Németh K, Fekete G, et al. Molecular genetic diagnostic difficulties in two Hungarian gypsy samples with cystic fibrosis. IJHG 2002; 2 (1): 41–44.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2019 Issue 7-
All articles in this issue
- Historie cystické fibrózy u nás – editorial
- Cystic fibrosis newborn screening and CFSPID diagnostics
- Ten years of neonatal screening of cystic fibrosis in Slovakia
- Lung function in a group of Czech infants with cystic fibrosis
- Pletysmografické a biochemické metody jako nové možnosti neinvazivního hodnocení endotelové dysfunkce u dětí s cystickou fibrózou – kombinovaný diagnostický přístup
- Allergic bronchopulmonary aspergillosis in pediatric patients with cystic fibrosis
- Bone health in children with cystic fibrosis
- Viscoelastic method rotational thromboelastometry (ROTEM)
- Recenzia knižnej publikácie: Ivan Frič, Mirko Zibolen, Viera Haľamová, František Bauer a kolektív: História neonatológie na Slovensku
-
Odešel prof. MUDr. Václav Špičák, CSc.
(14. ledna 1929–13. září 2019)
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Cystic fibrosis newborn screening and CFSPID diagnostics
- Viscoelastic method rotational thromboelastometry (ROTEM)
- Historie cystické fibrózy u nás – editorial
- Allergic bronchopulmonary aspergillosis in pediatric patients with cystic fibrosis
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

