-
Medical journals
- Career
Současný pohled na diagnostiku a léčbu astmatu u dětí
: J. Chládková
: Dětská klinika Lékařské fakulty v Hradci Králové, Univerzity Karlovy v Praze a Fakultní nemocnice, Hradec Králové
: Čes-slov Pediat 2018; 73 (3): 124-129.
:
Průduškové astma je nejčastější chronické onemocnění u dětí. Jeho podkladem je zánět průdušek. Stanovení diagnózy vychází ze zhodnocení typických příznaků a průkazu variabilní průduškové obstrukce. Pravidelná farmakoterapie pomocí nízké dávky inhalačních kortikosteroidů je vysoce účinná a vede k potlačení astmatických příznaků, snížení rizika astmatických exacerbací, hospitalizace a úmrtí na astma.
Klíčová slova:
průduškové astma, děti, variabilní průdušková obstrukce, nízké dávky inhalačních kortikosteroidůÚVOD
Průduškové astma je nejčastější chronické onemocnění u dětí charakterizované zánětem dýchacích cest. Epidemiologické studie ukázaly, že v České republice trpí astmatem 10 % dětí a 8 % dospělých. Bylo prokázáno, že u poloviny dospělých pacientů průduškové astma vzniká v prvních 5 letech života, dříve u chlapců než u dívek.
Astma je onemocnění dědičné. Průduškovým astmatem jsou více ohroženy děti, jejichž rodiče či sourozenci jsou astmatici. Průduškové astma se také častěji vyskytuje u pacientů s alergickou rýmou, atopickou dermatitidou a obezitou. Dispozice k nemoci však není dána jedním či několika geny, ale uplatňuje se řada genů. Při současných možnostech genetické diagnostiky byly objeveny desítky „kandidátních“ genů, které mohou ke vzniku astmatu více či méně přispívat. Dalším důležitým faktorem je kombinace poruch genů u jednoho jedince. Jedna porucha třeba ještě astma nevyvolá, nebo jen velmi lehkou formu, kombinace dvou a více poruch již může být faktorem predisponujícím pro těžší průběh astmatu. Interakce genů a vlivů prostředí má důležitou úlohu. Některé geny jsou považovány za potenciálně zvyšující riziko vzniku astmatu, jiné za protektivní. Byly např. prokázány interakce mikrobiálního prostředí jedince s geny pro receptory pro endotoxin. Větší nálož bakteriálního endotoxinu v prostředí je považována za protektivní faktor.
Mezi rizikové faktory pro rozvoj astmatu v prvních letech života dítěte patří bezesporu expozice tabákovému kouři, a to i prenatálně. Negativní vliv u kojenců a batolat s významnou alergickou zátěží v rodině mají trichloraminy v ovzduší plaveckých bazénů dezinfikovaných chlorem. Mezi látky s nepříznivým účinkem na dýchací cesty patří také průmyslové zplodiny, chemické látky vznikající spalováním fosilních paliv a dopravní smog.
Astma je komplexní choroba, která má i u dětí různé klinické fenotypy. Mezi příznaky průduškového astmatu patří opakující se záchvaty suchého, dráždivého kašle, pískotů při dýchání, dušnosti a pocitů tlaku na hrudníku. Pískoty jsou slyšitelné především při výdechu a dechové obtíže se často vyskytují v nočních hodinách (mezi 2. a 4. hodinou ranní). U těžších stavů se přidružuje i zatahování mezižebří. Naopak mírnější formy průduškového astmatu se mohou projevovat pouze záchvaty suchého dráždivého kašle. Ke zhoršení klinického stavu pacientů dochází při expozici alergenům, tělesné námaze, virových infekcích dýchacích cest a při inhalaci dráždivých látek.
Diagnózu astmatu lze u většiny spolupracujících dětí (od 3–4 let věku) stanovit na základě rozboru anamnestických údajů, správného zhodnocení příznaků a vyšetření plicní funkce s průkazem reverzibility průduškové obstrukce.
U dětí starších 3 let se většinou jedná o atopické (alergické) průduškové astma. U kojenců a batolat se kašel a pískoty při dýchání objevují často při virových infekcích horních dýchacích cest. O průduškovém astmatu v této věkové skupině uvažujeme, pokud se kašel s pískoty objevují i mimo akutní respirační infekce, při fyzické námaze, pláči a smíchu. V případě, že dítě má nebo mělo atopickou dermatitidu anebo alergickou rýmu a jeho rodiče či sourozenci trpí na průduškové astma. O stanovení správné diagnózy svědčí i vymizení obstrukčních příznaků při dýchání do 2–3 měsíců po zahájení preventivní léčby nízkou dávkou IKS (inhalační kortikosteroidy) a následné zhoršení klinického stavu dítěte po jejím ukončení.
Příznaky průduškového astmatu lze zaměnit za jiné onemocnění. U dětí v prvních letech života jsou to nejčastěji virové infekce dolních dýchacích cest (rinoviry a RS virus) a adenoidní vegetace jako infekční ložisko v horních dýchacích cestách. Bylo prokázáno, že adenoidní vegetace přispívají k těžšímu průběhu alergické rýmy a průduškového astmatu, proto je v tomto případě indikována adenoidektomie. Méně často se uplatňují nedonošenost a některé vrozené vývojové nebo získané vady a aspirace cizího tělesa. U školních dětí je třeba pomýšlet na atypickou bakteriální infekci dýchacích cest vyvolanou chlamydiemi a mykoplazmaty, ale také na psychogenní kašel, který je projevem úzkostné poruchy. Důležitou úlohu má i přidružená symptomatická refluxní nemoc jícnu s mimojícnovými projevy, která je indikací k zahájení režimových opatření a farmakoterapie inhibitorem protonové pumpy.
Průduškové astma není možné vyléčit. Farmakoterapie průduškového astmatu v současnosti je ale vysoce účinná a umožňuje u většiny dětských astmatiků dosáhnout dobrou kontrolu nad onemocněním a vést plnohodnotný život včetně vrcholové sportovní aktivity.
Základem preventivní léčby u všech stupňů perzistujícího astmatu jsou IKS. Přínos farmakoterapie IKS v doporučených denních dávkách vysoce převažuje nad rizikem systémových nežádoucích účinků. Bylo prokázáno, že časná léčba astmatu nízkou dávkou IKS vede k významnějšímu nárůstu plicní funkce a nižší spotřebě IKS ve srovnání s jejím opožděním o 2–4 roky. Všichni dětští pacienti a jejich zákonní zástupci musejí být vybaveni písemným plánem léčby astmatu s instrukcí, za jakých okolností přidat inhalace salbutamolu, zvýšit dávku IKS, vyhledat lékařskou péči a případně zahájit perorální léčbu prednisonem. Nezastupitelnou úlohu mají režimová opatření, jejichž cílem je vyloučit nebo alespoň omezit negativní vliv vyvolávajících faktorů včetně tabákového kouře. Z tohoto hlediska jsou u alergiků přínosná protiroztočová opatření, která zahrnují pořízení matracového polyuretanového chrániče do lůžka, vyprání ložního prádla 1krát za 14 dnů a lůžkovin 1krát za 2 měsíce, odstranění koberce minimálně z dětského pokoje, setření podlahy na vlhko 2x týdně. Neméně důležité je u přecitlivělých dětí vyloučení nebo alespoň omezení kontaktu s domácími zvířaty (zábrana jejich vstupu do dětského pokoje) a důsledné odstranění plísní z bytu.
Primární prevence astmatu u jedinců s genetickou vlohou je s ohledem na faktory vnějšího prostředí obtížná. Za nejdůležitější je považováno vyhnutí se tabákovému kouři a zvýšené vlhkosti v bytech spojené s výskytem plísní. Prospěšná je věku přiměřená sportovní aktivita a pobyt v přírodě. Je třeba předcházet obezitě. Doporučuje se strava bohatá na vitaminy a omega-3 nenasycené mastné kyseliny.
Vzhledem k dobré informovanosti zdravotníků i laické veřejnosti se významně zlepšil časný záchyt průduškového astmatu, ale nelze vyloučit i případy, kdy je astma poprvé diagnostikováno až u dětí s těžšími příznaky onemocnění. Časné stanovení správné diagnózy a dobrá prognóza astmatu závisí na spolupráci mezi praktickými lékaři pro děti a dorost, alergology a pneumology, ale zejména na dodržování léčebného režimu ze strany dětského pacienta a jeho rodiny, které je založeno na přátelském přístupu zdravotníků a vzájemné důvěře.
STANOVENÍ DIAGNÓZY PRŮDUŠKOVÉHO ASTMATU
Při stanovení diagnózy astmatu vycházíme z rozboru anamnestických údajů a správného zhodnocení příznaků. U spolupracujících dětí starších 3–4 let je třeba vyšetřit za použití animačních programů plicní funkci a provést bronchodilatační test, protože průkaz reverzibility průduškové obstrukce významně přispívá ke správné diagnóze.
Anamnéza
V anamnéze se vždy ptáme na variabilitu dechových obtíží (opakované epizody kašle, pískotů při dýchání, pocitu tlaku nebo tíže na hrudníku a dušnosti) a rodinnou zátěž pro astma a další alergická onemocnění.
Fyzikální vyšetření
Fyzikální vyšetření hrudníku je v období mezi exacerbacemi astmatu normální. Pískoty při dýchání se objevují při zhoršení kontroly nad astmatem. U školních dětí jsou považovány za typický astmatický příznak, ale někteří astmatici mají normální poslechový nález i při těžké astmatické exacerbaci. V tomto stavu jsou ale přítomny další varovné příznaky (obtíže při mluvení, inspirační postavení hrudníku, zapojení pomocných dýchacích svalů a zatahování měkkých tkání hrudníku, tachykardie, ospalost a cyanóza).
Funkční vyšetření plic
Vyšetření plicní funkce (vyšetření vitální kapacity a výdechových rychlostí pomocí křivky průtok-objem) je důležité pro potvrzení diagnózy astmatu a slouží k monitorování jeho kontroly u spolupracujících dětí. Naměřené hodnoty jsou porovnávány s náležitými populačními hodnotami a v rámci dispenzarizace pacienta i s jeho osobními nejlepšími hodnotami [1].
Pro diagnózu astmatu v běžné praxi je zvlášť přínosný průkaz reverzibility průduškové obstrukce (bronchodilatační test), který se provádí i u dětí s normálními (náležitými) hodnotami plicní funkce. Bronchodilatační test spočívá ve zhodnocení změny plicní funkce za 30 minut po inhalaci 4 dávek salbutamolu (400 mikrogramů) přes inhalační nástavec. Reverzibilita průduškové obstrukce je prokázána, dojde-li k nárůstu hodnoty FEV1 nejméně o 12 %. Negativní odpověď v bronchodilatačním testu ale astma nevylučuje. Významné zlepšení hodnot plicní funkce může nastat také za 3–6 měsíců po zahájení farmakoterapie inhalačními kortikosteroidy nebo kúře prednisonem (test s kortikoidy).
Bronchoprovokační test, který slouží k průkazu bronchiální hyperreaktivity u dětí s podezřením na astma a normální plicní funkcí, se provádí výjimečně.
Neinvazivní monitorování zánětu v průduškách
Zcela novým přístupem v diagnostice astmatu a monitorování jeho kontroly je stanovení koncentrace oxidu dusnatého (FENO) ve vydechovaném vzduchu pomocí běžně dostupných elektrochemických analyzátorů. Techniku vyšetření zvládne většina dětí starších 6 let.
Vysoké hodnoty FENO u dětí s příznaky astmatu potvrzují přítomnost eozinofilního zánětu v průduškách, který dobře odpovídá na léčbu IKS (tab. 1). Po zahájení farmakoterapie se hodnoty FENO v závislosti na dávce IKS rychle snižují a pokles hodnot předchází vymizení příznaků a zlepšení plicní funkce. Přetrvávání vysokých hodnot FENO při léčbě IKS může upozornit na nesprávnou inhalační techniku, nedostatečnou dávku, nespolupráci astmatika a významnou expozici alergenům. Zvýšení koncentrace FENO po ukončení farmakoterapie IKS nastává velmi rychle a předchází zhoršení klinického stavu, plicní funkce i nárůstu průduškové hyperreaktivity. Pravidelné sledování individuální hodnoty FENO (sledování relativní změny oproti výchozí hodnotě stavu před léčbou nebo oproti hodnotě spojené s dobrou kontrolou nad astmatem) může upozornit na blížící se exacerbaci astmatu.
1. Klasifikace hodnot FENO. 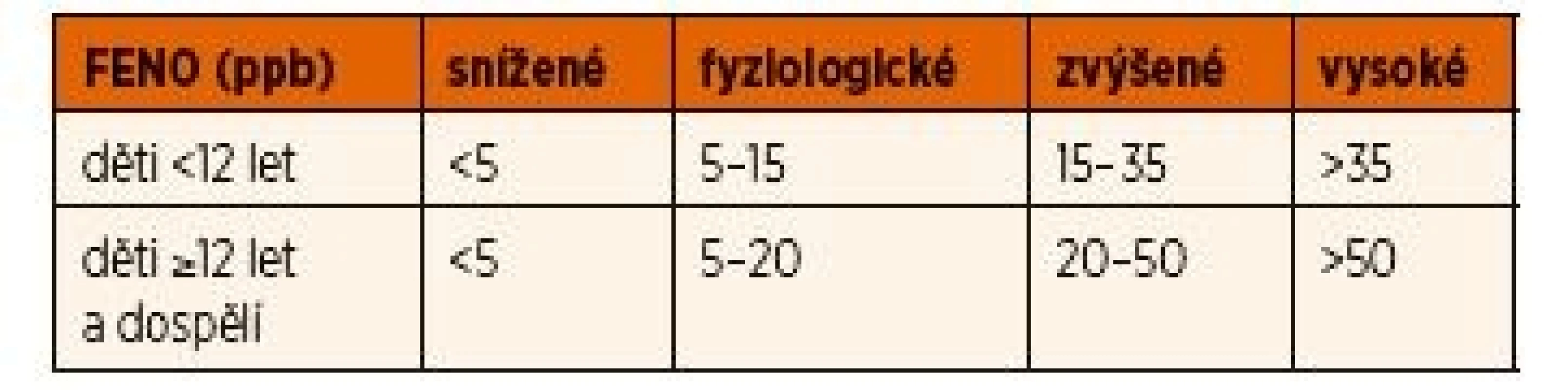
FENO – koncentrace oxidu dusnatého Z klinického hlediska je u dětí s respiračními příznaky a bez léčby IKS důležitá nízká hodnota FENO, která znamená, že se s vysokou pravděpodobností jedná o jinou diagnózu než o atopické průduškové astma [2].
Alergologické vyšetření
U dětí s podezřením na astma se provádí vyšetření kožních prick testů a v indikovaných případech i vyšetření specifických IgE protilátek v séru, které potvrdí přecitlivělost na inhalované alergeny (atopie). Pro interpretaci výsledků vyšetření jsou důležité anamnestické údaje o souvislosti mezi expozicí alergenům a objevením se astmatických příznaků, protože samotná pozitivita kožních testů ještě neznamená potvrzení spouštěčů alergické reakce [3].
Zobrazovací metody
Rentgenový snímek hrudníku má význam při vyloučení jiné příčiny obstruktivních příznaků při dýchání (např. aspirace cizího tělesa).
ORL vyšetření
U každého dítěte s recidivujícím kašlem je třeba provést epifaryngoskopické vyšetření a vyloučit adenoidní vegetace jako infekční ložisko.
FARMAKOTERAPIE PRŮDUŠKOVÉHO ASTMATU U DĚTÍ
V roce 2017 byla vydána aktualizovaná Globální strategie péče o astma a jeho prevence (GINA). Jde o mezinárodně uznávaný dokument vycházející z nejnovějších poznatků medicíny založené na důkazech [4]. Preventivní farmakoterapie astmatu je vedena podle pětistupňové léčebné strategie.
Nejúčinnějšími léky v dlouhodobé preventivní farmakoterapii astmatu jsou již více než 20 let IKS, které mají protizánětlivý účinek, potlačují příznaky astmatu, snižují četnost a tíži exacerbací astmatu, zlepšují funkci plic, snižují stupeň bronchiální hyperreaktivity, zlepšují kvalitu života a snižují úmrtnost na astma. Na buněčné úrovni IKS potlačují zánět v průduškách snížením počtu a aktivace eozinofilů, T lymfocytů, žírných buněk a makrofágů, snižují zánětlivou odpověď epiteliálních a endoteliálních buněk, propustnost kapilár a sekreci hlenu v průduškách a zlepšují účinek beta-2 agonistů tím, že zvyšují počty beta-2 receptorů v hladké svalovině průdušek.
Místo inhalačních kortikosteroidů ve farmakoterapii průduškového astmatu u dětí
V ČR se u dětí používají beklometason, budesonid a flutikason. Děti starší 12 let mohou být léčeny také mometasonem a ciklesonidem. Podle ukazatelů kontroly nad astmatem má flutikason v poloviční dávce stejný účinek jako beklometason a budesonid.
Hlavní výhodou inhalační cesty podání je vysoká koncentrace léčiva v průduškách a snížení rizika systémových nežádoucích účinků. V současnosti se běžně používají tlakové aerosolové dávkovače a práškové inhalátory. Astmatik musí dobře zvládnout inhalační techniku, kterou je potřeba v pravidelných intervalech kontrolovat. Důležitá je správná volba inhalačního systému s ohledem na věk dítěte. Pro obtížnou koordinaci mezi spuštěním tlakového aerosolového dávkovače a nádechem mají být tlakové aerosolové dávkovače u dětí používány s inhalačním nástavcem (u dětí do 3 let s maskou, u starších 4 let s náustkem). Tím se docílí vyšší plicní a nižší depozice v ústech a hltanu, dýchací cesty jsou méně drážděny studeným aerosolovým oblakem a snižuje se riziko lokálních (kandidóza dutiny ústní a dysfonie) i systémových nežádoucích účinků. U šikovných dětí starších 4–5 let lze použít některé práškové inhalátory.
Podle dokumentu GINA 2017 k pravidelné dlouhodobé léčbě průduškového astmatu u dětí většinou postačují nízké denní dávky IKS (tab. 2) se zhodnocením účinku v odstupu nejméně 3 měsíců. Po dosažení kontroly nad astmatem (nejdříve po 3 měsících) se počáteční denní dávka IKS postupně snižuje až na nejnižší dávku, která udrží astma pod kontrolou.
2. Dávky inhalačních kortikosteroidů (upraveno podle GINA 2017). 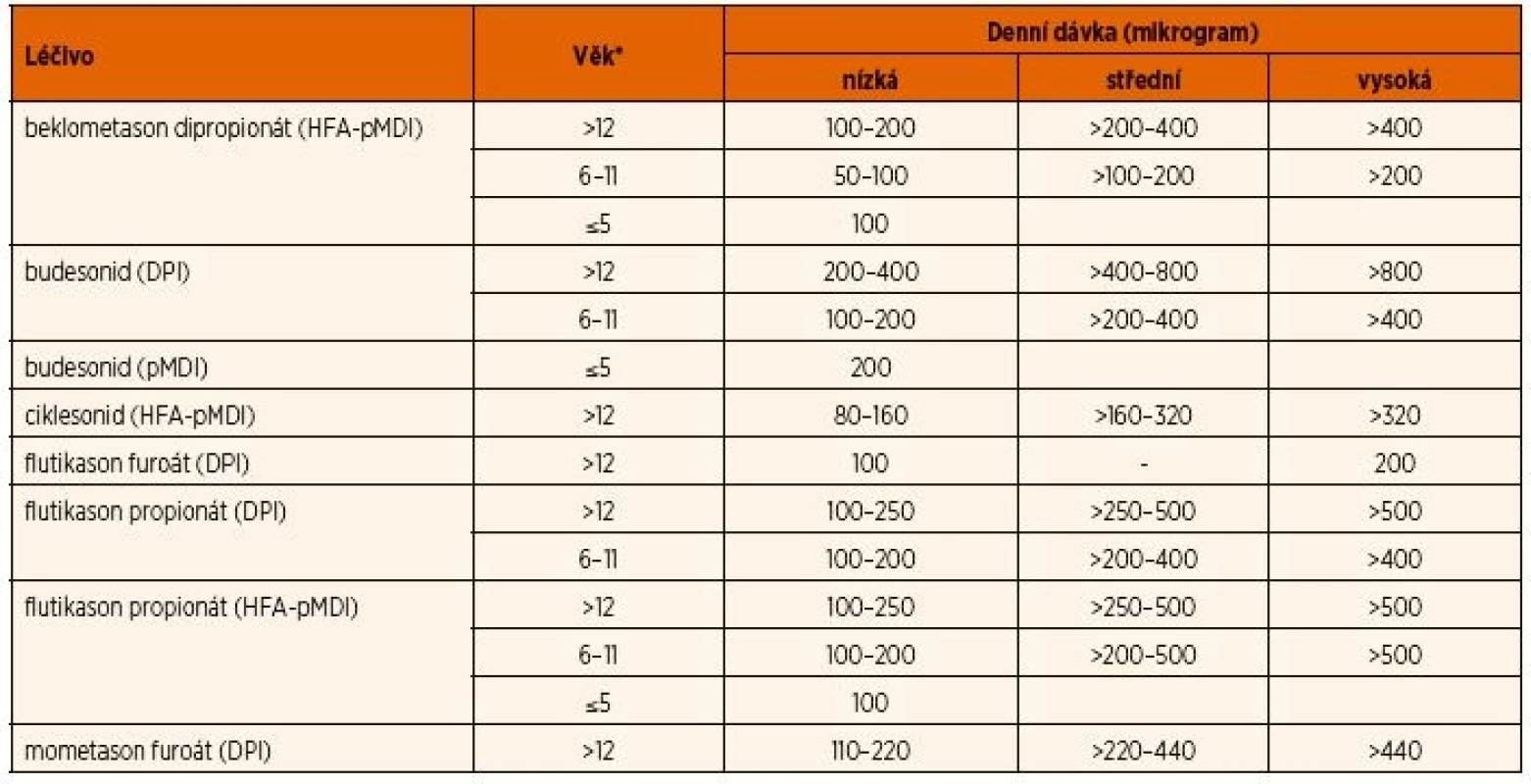
Vysvětlivky: *u dětí ≤4 roky se používají inhalační nástavce s náustkem nebo obličejovou maskou (0–3 roky); DPI – inhalátor s práškovou formou léčiva; HFA – hydrofluoroalkanový hnací plyn; pMDI – tlakový aerosolový dávkovač Podle analýzy klinických studií nelze u pacientů s lehkým perzistujícím astmatem doporučit nepravidelnou farmakoterapii IKS, např. jen v období zhoršení příznaků při akutní respirační infekci [5].
Všechny děti a jejich zákonní zástupci musejí být vybaveni písemným plánem léčby astmatu. Součástí písemného plánu je terapie astmatické exacerbace v domácích podmínkách s opakovanou aplikací salbutamolu (2–4 dávky po 20 minutách během první hodiny), zdvojnásobením dávky IKS, event. rozepsáním dávek prednisonu u těžšího astmatu a doporučením, kdy je nutné vyhledat lékařskou péči.
Počáteční léčba IKS závisí na tíži astmatu (tab. 3). Děti s intermitentním astmatem nevyžadují preventivní léčbu IKS. Podle potřeby inhalují pro ojedinělé denní lehké astmatické příznaky (méně než 2x měsíčně) salbutamol. Perorální bronchodilatancia se nedoporučují pro pomalejší nástup účinku a vyšší riziko systémových nežádoucích účinků. U dětí, které v posledním roce prodělaly astmatickou exacerbaci nebo měly častější příznaky, je třeba zahájit pravidelnou léčbu IKS.
3. Doporučený postup pro zahájení farmakoterapie astmatu u dětí starších 12 let (upraveno podle GINA 2017). 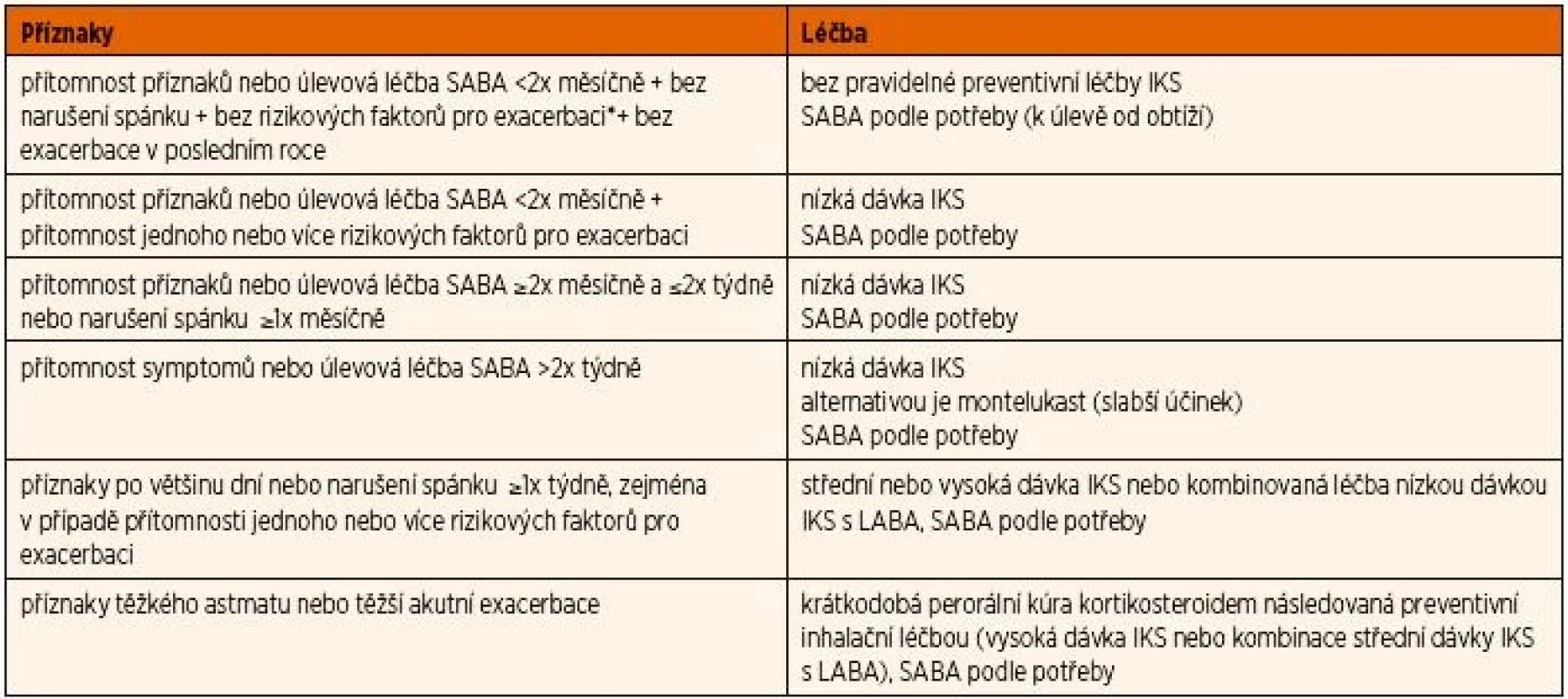
* rizikové faktory pro exacerbaci: snížení plicní funkce (FEV1 <60 % náležité hodnoty), astmatická exacerbace v posledním roce vyžadující perorální kortikosteroidy, častá inhalace SABA, expozice tabákovému kouři a alergenům aj.
SABA – beta-2 agonista s krátkodobým účinkem (salbutamol); LABA – beta-2 agonista s dlouhodobým účinkem; IKS – inhalační kortikosteroidU dětí s lehkým perzistujícím astmatem bez ohledu na věk se doporučuje pravidelná léčba nízkou dávkou IKS. Podle potřeby lze navíc použít salbutamol jako úlevový nebo preventivní léčivý přípravek před zvýšenou fyzickou aktivitou (např. běh nad 500 m v hodinách tělesné výchovy). Jiné terapeutické alternativy se před IKS neupřednostňují (např. montelukast).
Pokud naopak nemá pravidelná léčba dostatečný účinek, je třeba se před zvýšením dávky IKS přesvědčit o správnosti inhalační techniky a dodržování dávkovacího schématu, prověřit kontakt s alergeny a dráždivými látkami, vyloučit přidružená onemocnění (např. refluxní nemoc jícnu) a v diagnostické rozvaze uvažovat i o jiném onemocnění, které se projevuje obstruktivními příznaky při dýchání (např. primární ciliární dyskineze, cystická fibróza, tracheobronchomalacie, cévní prstence, imunodeficience, aspirace cizího tělesa, dysfunkce hlasivek aj.).
U dětí starších 12 let se v případě nedostatečné kontroly nad astmatem doporučuje od stupně 3 léčebné strategie kombinovaná léčba nízkou dávkou IKS s LABA (salmeterol nebo vilanterol) a podle potřeby se k potlačení astmatických příznaků používá salbutamol. Druhou možností je farmakoterapie kombinací nízké dávky IKS s formoterolem (jde o beta-2 agonistu s rychlým nástupem účinku i dlouhodobým účinkem), která se používá v rámci preventivní, ale i úlevové léčby. To znamená, že se místo salbutamolu podle potřeby podá další dávka z kombinovaného inhalátoru, který obsahuje IKS a formoterol. V ČR je u dětí od 12 do 18 let v této indikaci povoleno používat práškový inhalátor Symbicort Turbuhaler 100/6 obsahující v jedné dávce 100 mikrogramů budesonidu a 6 mikrogramů formoterolu.
U astmatiků ve věku 6–11 let se naopak dává podle stupně 3 přednost středním dávkám IKS, a to pro doložený větší účinek. Inhalační salbutamol lze použít navíc podle potřeby.
U dětí mladších 5 let se doporučuje zdvojnásobit předchozí nízkou dávku IKS. Pro astmatiky této věkové skupiny není kombinace IKS s LABA doporučována pro nedostatečně ověřený účinek.
Alternativou je u dětí starších dvou let přidání montelukastu k nízké dávce IKS.
Léčba astmatické exacerbace u dětí
Astmatická exacerbace je definována jako zhoršení klinického stavu pacienta s významným nárůstem astmatických příznaků a zhoršením plicní funkce, které vyžaduje změnu farmakoterapie. Častou příčinou je svévolné ukončení dlouhodobé preventivní léčby IKS nebo virová infekce dýchacích cest. Těžká astmatická exacerbace vyžaduje komplexní terapii na JIRP. Po proběhlé astmatické exacerbaci je třeba vždy upravit preventivní léčbu astmatu.
Děti a jejich zákonní zástupci jsou vybaveni písemným plánem léčby astmatu, podle kterého postupují v případě exacerbace. Prvním krokem je opakované podání salbutamolu optimálně pomocí inhalačního nástavce pro dosažení co největší plicní depozice a zdvojnásobení dávky IKS. U pacientů s těžší astmatickou exacerbací je třeba zahájit krátkodobou kúru perorálním kortikosteroidem (nejčastěji prednison). U dětí starších 12 let se užívá prednison v denní dávce 40–50 mg po dobu 5–7 dnů. Ve věkové skupině do 11 let je doporučena denní dávka prednisonu 1–2 mg/kg po dobu 3–5 dnů (od 6–11 let max. 40 mg denně, od 2–5 let max. 30 mg a mladších 2 let max. 20 mg). Alternativou je během prvního dne léčby při hospitalizaci intravenózní aplikace methylprednisolonu v dávce 1 mg/kg po 6 hodinách. Po prodělané astmatické exacerbaci se doporučuje používat dvojnásobnou dávku IKS po dobu 2–4 týdnů.
Nežádoucí účinky inhalačních kortikosteroidů
Nežádoucí účinky IKS jsou závislé na dávce, inhalačním systému a na inhalační technice. Je důležité, aby dlouhodobá udržovací dávka IKS odpovídala tíži astmatu. U většiny dětí s astmatem stačí k dlouhodobé kontrole nad onemocněním nízké denní dávky IKS, jejichž používání není spojeno s rizikem systémových nežádoucích účinků. Všechny IKS se vstřebávají z plic do systémového oběhu v závislosti na tíži astmatu. Farmakokinetické studie ukázaly, že u nemocných s těžkým astmatem jsou po stejné dávce IKS až čtyřikrát nižší koncentrace IKS v krvi než u zdravých osob. Důvodem je větší plicní depozice a absorpce větší části dávky IKS z plicních sklípků u zdravých osob. To znamená, zaprvé, že nemocný léčený dávkami IKS odpovídajícími tíži astmatu je do značné míry uchráněn před systémovými nežádoucími účinky IKS. A zadruhé, z tohoto pohledu je také zcela správná strategie postupného snižování dávek IKS až na minimální dávku, při které je astma pod kontrolou. Část dávky IKS, která se deponuje v dutině ústní a hltanu, může být spolknuta a vstřebána ve střevě. Inhalační nástavec, dechem aktivované inhalátory a výplach úst po inhalaci množství IKS v GIT snižují. Důležitý je metabolismus kortikosteroidů, ke kterému dochází po vstřebání během prvního průchodu játry. Budesonid a flutikason jsou tímto mechanismem velmi účinně eliminovány z krve, zatímco asi 30 % ze vstřebané dávky beklometasonu je dostupných v systémové cirkulaci ve formě aktivního metabolitu.
Vzhledem k tomu, že narůstá počet dětí s lehkým perzistujícím astmatem léčených IKS, věnuje se riziku nežádoucích účinků IKS velká pozornost. V závislosti na dávce všechny IKS přechodně snižují růstovou rychlost pouze v prvním až druhém roce terapie přibližně o 0,4 až 2 cm/1–2 roky [6]. Jedná se o klinicky nevýznamné snížení růstové rychlosti nejčastěji studované u dětí s lehkým a středně těžkým astmatem před nástupem puberty, kdy průměrná růstová rychlost je 5,5 cm za rok. V dalším období se růstová rychlost vyrovnává a definitivní tělesná výška je podle závěru dlouhodobé studie CAMP (The Childhood Asthma Management Program) ovlivněna jen velmi málo (1,2 cm) [7]. Je nutné zdůraznit, že neléčené těžší astma vede nejen ke snížení růstové rychlosti, ale i k významně nižší konečné tělesné výšce. Nízké dávky IKS nevyvolávají ani přechodné zpomalení růstu.
Existují také obavy z možného negativního vlivu IKS na kostní hmotu, který by mohl v konečném důsledku vést až k osteoporóze a frakturám. Nebyly publikovány studie nebo zprávy o zvýšeném riziku fraktur u dětí léčených IKS. Dlouhodobá inhalační léčba IKS je z pohledu přírůstků kostní hmoty mnohem bezpečnější než opakované kúry perorálním kortikosteroidem. Důležitá je také kvalitní výživa s dostatečným přísunem vápníku a vitaminu D [8].
Nežádoucí účinky montelukastu
Montelukast patří mezi antagonisty leukotrienových receptorů, které mají protizánětlivý a preventivní účinek proti bronchokonstrikci vyvolané tělesnou námahou, expozicí alergenům a dráždivým látkám. Hlavní výhoda je perorální cesta podání, nicméně jeho účinek byl v kontrolovaných klinických studiích slabší než účinek IKS v nízké dávce. Recentní studie zabývající se bezpečností montelukastu v každodenní praxi ukázala na riziko neuropsychických změn. Jedná se o bolest hlavy, deprese a u dětí především o noční děsy a agresivitu. Tyto nežádoucí účinky se objevují záhy po zahájení farmakoterapie a po jejím ukončení vymizí [9].
ZÁVĚR
Důležitou roli v úspěšné léčbě astmatu má edukace dětských astmatiků a jejich rodičů, aby porozuměli svému onemocnění, neukončovali svévolně preventivní farmakoterapii IKS a při zhoršení kontroly nad astmatem použili v domácích podmínkách léčivé přípravky podle doporučení uvedeného v písemném plánu léčby astmatu.
Doc. MUDr. Jiřina Chládková, Ph.D.
Dětská klinika FN
Sokolská 581
500 05 Hradec Králové
e-mail: chladkovajirina@gmail.com
Sources
1. Pohunek P. Průduškové astma v dětském věku. Funkční vyšetření plic. In: Petrů V, a kol. Dětská alergologie. Praha: Mladá fronta, 2012 : 1–239.
2. Alving K, Malinovski A. Basic aspects of exhaled nitric oxide. In: Horvath I, de Jongste JC. Exhaled Biomarkers. European Respiratory Society Momograph 2010; 49 : 1–31.
3. Petrů V. Klinická diagnostika. Alergenové testy. In: Petrů V, a kol. Dětská alergologie. Praha: Mladá fronta, 2012 : 77.
4. 2017 GINA Report. Global Strategy for Asthma Management and Prevention Global Initiative for Asthma. NHLBI/WHO. NIH Publication No.02-3659.
5. Rodrigo GJ. Daily versus intermittent inhailed coticosteroid treatment for mild president asthma. Curr Opin Allergy Clin Immunol 2014; 3 : 186–191.
6. Zhang L, Priettsch SOM, Ducharme FM. Inhaled corticosteroids in children with persistent asthma. Effects on growth. Cochrane Database Syst Rev 2014; 7: CD 009471.
7. The Childhood Asthma Management Program (CAMP) Research Group. Long-term effects of budesonide or nedocromil in children with asthma. N Engl J Med 2000; 343 : 1054–1063.
8. Fuhlbrigge A, Kelly WHEN. Inhaled corticosteroid in children: effects on bone mineral density and growth. J Paediatr Child Health 2016; 52 : 964–966.
9. Haarman MG, van Hunsel F, De Vries TW. Adverse reactions of montelukast in children and adults. Pharma Res Per 2017; 5 : 1–8.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2018 Issue 3-
All articles in this issue
- Current approach to asthma diagnosis and treatment in children
- The small gardener
- Retrospective analysis of minor head injuries at the Department of Paediatrics, the Teaching Hospital and the Faculty of Medicine, Charles University in Pilsen in the years 2010–2014
- C3 glomerulopathy – a new clinical entity
- Macro AST – cause of asymptomatic aspartate aminotransferase elevation – case report
- Transitory hypertrophic cardiomyopathy in newborn with a neonatal withdrawal syndrome
- Alternating antipyretic treatment of fever increases the risk of side effects
- Diagnostics, treatment and prognosis of congenital hypothyroidism
- Low birth weight and other risk factors for later diseases in children and adults (prenatal and postnatal programming
- News in cardiopulmonary resuscitation – „guidelines 2018“
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- C3 glomerulopathy – a new clinical entity
- Current approach to asthma diagnosis and treatment in children
- News in cardiopulmonary resuscitation – „guidelines 2018“
- Macro AST – cause of asymptomatic aspartate aminotransferase elevation – case report
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

