-
Medical journals
- Career
Dievča s karyotypom 46, XY
Authors: Z. Blusková; Ľ. Košťálová
Authors‘ workplace: II. detská klinika LFUK a DFNsP, Bratislava prednosta prof. MUDr. L. Kovács, DrSc., MPH
Published in: Čes-slov Pediat 2013; 68 (2): 113-118.
Category: Case Report
Overview
Popisujeme prípad dieťaťa, ktoré sa narodilo s poruchou sexuálnej diferenciácie. V novorodeneckom veku mu bolo len na základe väčšej makroskopickej podobnosti vonkajších genitálií k ženským rodidlám priradené ženské pohlavie. Klitoris „rástol s dieťaťom“, vo veku 6 rokov bola jeho veľkosť cca 3 cm, vyčnieval z lábií. To bolo dôvodom, prečo sa rodina rozhodla vyhľadať lekára. Genetickým vyšetrením sa zistil karyotyp 46, XY. V priebehu nasledujúcich vyše 2 rokov bola pre stanovenie diagnózy a liečby postupne odosielaná viacerým špecialistom. Až vo veku 8,5 roka prišla bezradná matka svojvoľne na konzultáciu do endokrinologickej ambulancie II. Detskej kliniky LFUK a DFNsP v Bratislave. Následne bolo dieťa hospitalizované za účelom doriešenia stavu.
MR vyšetrením sme zistili prítomnosť rudimentárnych mužských vnútorných orgánov, ženské vnútorné orgány prítomné neboli. Laboratórne výsledky boli pre daný vek v medziach normy. Za daných okolností nebolo možné stanoviť u pacientky definitívnu diagnózu. Vzhľadom na vek, výchovu ženským smerom a dievčenské správanie a cítenie, s prihliadnutím na želanie rodičov, bolo u pacientky ponechané ženské pohlavie. Tkanivo v ingvínach (susp. semenníky) bolo exstirpované, s histologickým nálezom hypoplastických semenníkov bez prítomnosti Leydigových buniek. U pacientky bola vykonaná chirurgická úprava vonkajších genitálií ženským smerom.Kľúčové slová:
poruchy sexuálnej diferenciácie, 46, XY, nedostatočná tvorba a pôsobenie androgénovKAZUISTIKA
Pacientka sa narodila po fyziologickom priebehu tehotenstva. Jej sestra, nevlastná sestra i rodičia sú zdraví. Z rodinnej anamnézy sú pozoruhodné dve úmrtia novorodencov mužského pohlavia – z nejasných príčin v novorodeneckom veku zomrel otcov brat i brat otcovej matky. Naša pacientka sa narodila s virilizovanými vonkajšími genitáliami, kde prominoval zväčšený klitoris. Na základe ich vzhľadu, ktorý sa viac podobal na ženské vonkajšie pohlavné orgány, bolo dieťaťu určené ženské pohlavie. Bolo prepustené z pôrodnice a ďalej vychovávané ako dievča. Prečo sú pacientkine genitálie virilizované, sa nedodiagnostikovalo a nebol urobený ani karyotyp.
Keď mala dievča 6 rokov, matke sa začalo zdať, že klitoris dieťaťa sa zväčšuje, preto navštívila detskú lekárku. Tá odoslala pacientku ku gynekológovi. Po vyšetrení detským gynekológom, ktorý popísal maskulinizáciu vonkajších rodidiel – zväčšený klitoris, vchod do pošvy prekrytý pablanou, ústie uretry na perineu – bolo dievčatku prvýkrát odporučené genetické a endokrinologické vyšetrenie. Vo veku 6,5 roka genetik u pacientky popísal mierne známky ďalšej stigmatizácie: hypertelorizmus, mierne predĺžený chrbát nosa, znížené ušnice, zvýšené podnebie. Cytogenetickým vyšetrením sa zistil karyotyp 46, XY.
Skoro 7-ročná pacientka sa prvýkrát dostala k detskému endokrinológovi. Hormonálny profil dieťaťa bol vtedy fyziologický: hladiny hormónov štítnej žľazy boli v norme (fT4 : 16,4 pmol/l, fT3 : 4,85 pmol/l, TSH: 3,1 mIU/l), dieťa malo nízke hladiny pohlavných hormónov (estradiol <3,0 pg/ml, testosterón <0,07 ng/ml, DHEAS <10 µg/100 ml) i nízke hladiny gonadotropínov (LH <0,2 IU/l, FSH: 0,31 IU/l), čo je typické pre detský vek. Nízka hladina 17-hydroxyprogesterónu (0,2 ng/ml) nesvedčila pre najčastejšiu z porúch steroidogenézy – jednoduchú virilizujúcu formu kongenitálnej adrenálnej hyperplázie. USG zobrazením sa nenašli gonády, v strednej rovine v malej panve však bol popísaný väzivový pruh, ktorý bol považovaný za možnú maternicu.
Pacientke bola doporučená konzultácia u detského chirurga s cieľom nájsť a odstrániť dysgenetické gonády a upraviť malformované genitálie. Podľa výpovede matky chirurg odporučil viesť operáciu mužským smerom a zmenu pohlavia dieťaťa na mužské.
S týmto rodičia nesúhlasili a s 8,5-ročným dieťaťom prišli na konzultáciu do endokrinologickej ambulancie 2. Detskej kliniky DFNsP a LFUK v Bratislave. Klinicky bol prítomný hypertrofický klitoris dĺžky cca 3 cm, vyústenie uretry na perineu, fúzované lábiá, gonády neboli hmatné. Pacientka mala predpubertálny hormonálny profil a normálny ionogram. Pri USG zobrazení malej panvy sonografista popísal, že videl pravé ovárium s folikulmi milimetrovej veľkosti, kým uterus, ľavé ovárium ani žiaden iný útvar nenašiel. Na MRI nebola zobrazená maternica ani ováriá. Medzi symfýzou a ventrálnou stenou uretry bol zobrazený útvar veľkosti 18 x 12 x 10 mm, so signálom podobným prostatickému tkanivu. V ingvínach bol obraz rudimentárnych spermatických funikulov a tkaniva, ktoré bolo podobné semenníkom.
Vzhľadom na to, že 8,5-ročné dieťa bolo vychovávané ako dievča, hrávalo sa s bábikami, cítilo sa byť dievčaťom, vzhľadovo vyzeralo ako dievča až na vonkajšie genitálie, rodičia si želali „pokračovať“ u dieťaťa v ženskom pohlaví a predpokladali sme hypofunkčné semenníky (s otáznou možnosťou malignizácie), rozhodli sme sa nájsť a odstrániť pohlavné žľazy laparoskopicky a v ďalšom kroku vykonať chirurgickú úpravu vonkajších genitálií ženským smerom. Počas laparoskopie sa v ingvínach našli bilaterálne semenníky, ktoré boli hypoplastické, prítomný bol ductus spermaticus obojstranne a nenašla sa žiadna z Mülleriánskych štruktúr (maternica, vajcovody). Pri histologickom vyšetrení sa zistilo, že semenníky sú anatomicky správne formované, ale chýbali v nich Leydigove bunky.
DISKUSIA
Výsledky histológie by mohli mylne viesť k stanoveniu diagnózy hypoplázie Leydigových buniek. V predpubertálnych semenníkoch však dochádza fyziologicky k regresii počtu i funkcie Leydigových buniek, ktoré sa obnovujú do normálneho stavu až v období puberty [1]. Navyše, istý stupeň hypoplázie semenníkov možno pozorovať pri dlhšom pretrvávaní ich umiestnenia mimo skrótum. Preto na základe histológie nemôžeme jednoznačne stanoviť diagnózu a do úvahy prichádzajú všetky poruchy sexuálnej diferenciácie 46, XY s nedostatkom funkčných androgénov, zodpovedných za vývoj vnútorných i vonkajších mužských pohlavných orgánov.
Na upresnenie etiológie ochorenia sú potrebné ďalšie vyšetrenia (stimulačné testy), ktoré vzhľadom k okolnostiam v našom prípade nebolo možné zrealizovať. Ďalšou možnosťou je molekulárno-genetické vyšetrenie (prehľad porúch zo skupiny 46, XY DSD s vyvinutými semenníkmi a vývoj pohlavného systému nájdete nižšie). Definitívna diagnóza u dieťaťa zostala teda zatiaľ bohužiaľ neodhalená. Klinický postup bol však v tomto prípade jednoznačný – po orchiektómii bola u pacientky vykonaná chirurgická úprava vonkajších genitálií ženským smerom a vo veku 10 rokov jej malými dávkami estrogénov navodzujeme pubertu.
PORUCHY SEXUÁLNEHO VÝVOJA 46, XY
Embryológia vývoja pohlavných orgánov
Pre pochopenie patofyziológie a zvažovanie manažmentu u detí s poruchou sexuálnej diferenciácie je nutné poznanie embryonálneho vývoja pohlavného ústrojenstva. Sexuálna diferenciácia bipotentných gonád prebieha od 7. týždňa a ukončuje sa v 14. týždni vývoja plodu. Najskôr sa vyvíjajú pohlavné žľazy, potom nasleduje vývoj ostatných vnútorných pohlavných orgánov, posledné sa vyvíjajú vonkajšie pohlavné orgány.
Na vznik semenníkov je nutná prítomnosť neporušeného SRY-génu (sex determinujúci gén), ktorý sa nachádza na krátkom ramienku Y chromozómu. SRY-gén kóduje tvorbu testes determinujúceho faktoru, pod vplyvom ktorého sa rozbieha kaskáda reakcií, do ktorých je zahrnuté ďalšie množstvo génov a ich pôsobkov (napr. SOX9, DMRT 1, 2, GATA-4, Dhh, testatin, SF-1, WT 1), nie všetky sú v súčasnosti dostatočne preskúmané [2, 3].
Prvým príznakom diferenciácie gonád v semenníky je agregácia pre-Sertoliho buniek okolo zárodočných buniek. Z nich sa vyvinú Sertoliho bunky, ktoré riadia diferenciáciu ostatných buniek. Sertoliho bunky produkujú antimüleriánsky hormón (AMH), vďaka ktorému medzi 8.–10. gestačným týždňom dochádza k regresii Müllerovho duktu. Ak chýba inhibičné pôsobenie AMH, vyvinie sa uterus, vajíčkovody a horná časť vagíny.
Ku koncu 9. týždňa sa diferencujú Leydigove bunky. Tieto sú zo začiatku gravidity pod vplyvom ľudského chóriogonadotropínu (hCG) z placenty a produkujú dva hormóny: testosterón (TST) a INSL3. Testosterón stimuluje ďalší vývoj Wolffových vývodov na strane, kde sa testes vyskytujú. Vznikajú tak epididymidis, vas deferens, vesiculae seminales. Pri nedostatku androgénov sa tieto štruktúry riadne nevyvinú.
Medzi 9.–12. týždňom sú androgény, najmä metabolit testosterónu dihydrotestosterón, ktorý vzniká pôsobením enzýmu 5-alfa reduktázy, zodpovedné za maskulinizáciu vonkajších genitálií.
INSL3, produkovaný Leydigovými bunkami a regulovaný hCG a luteinizačným hormónom (LH), je zodpovedný za 1. fázu descensu testis z brušnej dutiny, čo sa deje počas II. trimestra gravidity. Za 2. fázu descensu semenníkov a za rast penisu sú opäť zodpovedné androgény, produkované Leydigovými bunkami, hlavným stimulom pre ich syntézu v tomto období (III. trimester) je však už LH.
46, XY, DSD s deficitom a poruchou funkcie androgénov
Podľa konsenzu odborníkov a podľa novej navrhovanej klasifikácie z roku 2006 delíme poruchy sexuálneho vývoja (DSD) podľa karyotypu [4]. Pacienti s karyotypom 46, XY DSD majú buď narušený testikulárny vývoj, alebo poruchy tvorby či funkcie androgénov (tab. 1).
Table 1. Nová navrhovaná klasifikácia porúch sexuálnej diferenciácie (DSD). 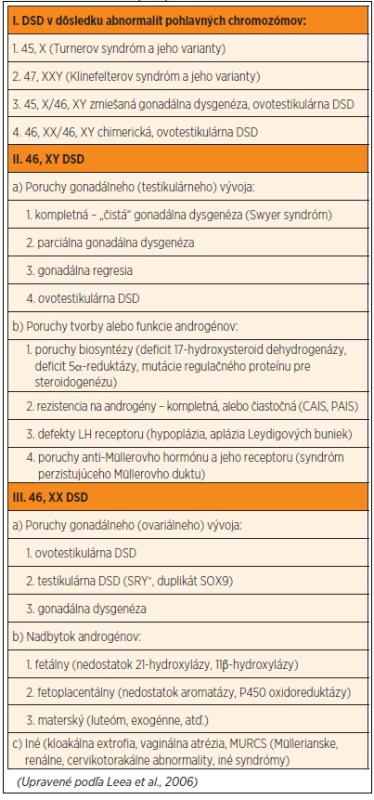
Pri syndróme androgénovej insenzitivity (AIS) tkanivá postihnutých jedincov nevedia odpovedať na androgény. Prítomná je mutácia génu pre androgénový receptor, ktorá spôsobuje jeho nedostatočnú funkciu a podľa jeho zostatkovej aktivity rozoznávame syndróm kompletnej androgénovej necitlivosti (CAIS) a syndróm parciálnej androgénovej necitlivosti (PAIS), v niektorej literatúre aj syndróm necitlivosti na androgény v jemnej forme (MAIS) [5]. Pri všetkých formách má postihnutý normálne vyvinuté semenníky, produkujúce AMH i TST, semenníky však bývajú nezostúpené.
Pri kompletnej necitlivosti na androgény je prítomná ťažká porucha virilizácie. Takýto jedinec vyzerá ako žena, má vyvinuté vonkajšie genitálie ženského vzhľadu, nemá prítomné štruktúry vznikajúce z Wolffovho duktu. Produkovaný AMH je funkčný, v dôsledku čoho postihnutý nemá vyvinuté ani vnútorné ženské pohlavné orgány. V niektorých prípadoch je však zriedkavo popisovaná ich prítomnosť [6]. V pubertálnom období sa toto ochorenie prejavuje primárnou amenoreou a chýbajúcim pubickým a axilárnym ochlpením pri normálnom vývoji prsníkov, pretože dochádza k premene časti testosterónu na estrogény.
Pri syndróme parciálnej necitlivosti na androgény je rôzne veľká reziduálna funkcia androgénového receptora, podľa ktorej varíruje aj klinický obraz. Postihnutí mávajú nejednoznačný vzhľad vonkajších genitálií, rôzne vyvinuté vnútorné mužské pohlavné orgány, absenciu štruktúr, vychádzajúcich z Müllerovho duktu (hoci boli popísané aj ich remnanty [7]. V prípade MAIS môže byť prítomná mierna nedostatočná virilizácia, alebo len hypospádia. V puberte býva prítomná gynekomastia, riedke ochlpenie, vysoký hlas, impotencia. Môže byť zachovaná fertilita jedinca [5]. Laboratórne nachádzame normálnu alebo zvýšenú hladinu TST a DHT, normálnu alebo zvýšenú hladinu AMH a LH a normálny pomer testosterón/dihydrotestosterón. Diagnózu možno potvrdiť dôkazom mutácie génu pre androgénový receptor. Možnou príčinou poruchy biosyntézy androgénov je päť známych defektov (tab. 2) [8]. Z toho prvé 4 sú späté aj s poruchou tvorby kortikoidov a vzniká súčasne obraz adrenálnej insufi-ciencie. U pacientov s poruchou steroidogenézy sú normálne vyvinuté testes, často však býva prítomný kryptorchizmus. V dôsledku funkčného AMH nemajú títo pacienti prítomné vnútorné ženské pohlavné orgány. Vnútorné mužské pohlavné orgány a vonkajšie genitálie bývajú vyvinuté v závislosti od zostatkovej aktivity androgénov. Laboratórne u týchto pacientov nachádzame hromadenie steroidových produktov nad enzymatickým blokom.
Table 2. Známe enzymatické defekty pri poruche biosyntézy androgénov, vedúce k 46, XY DSD. 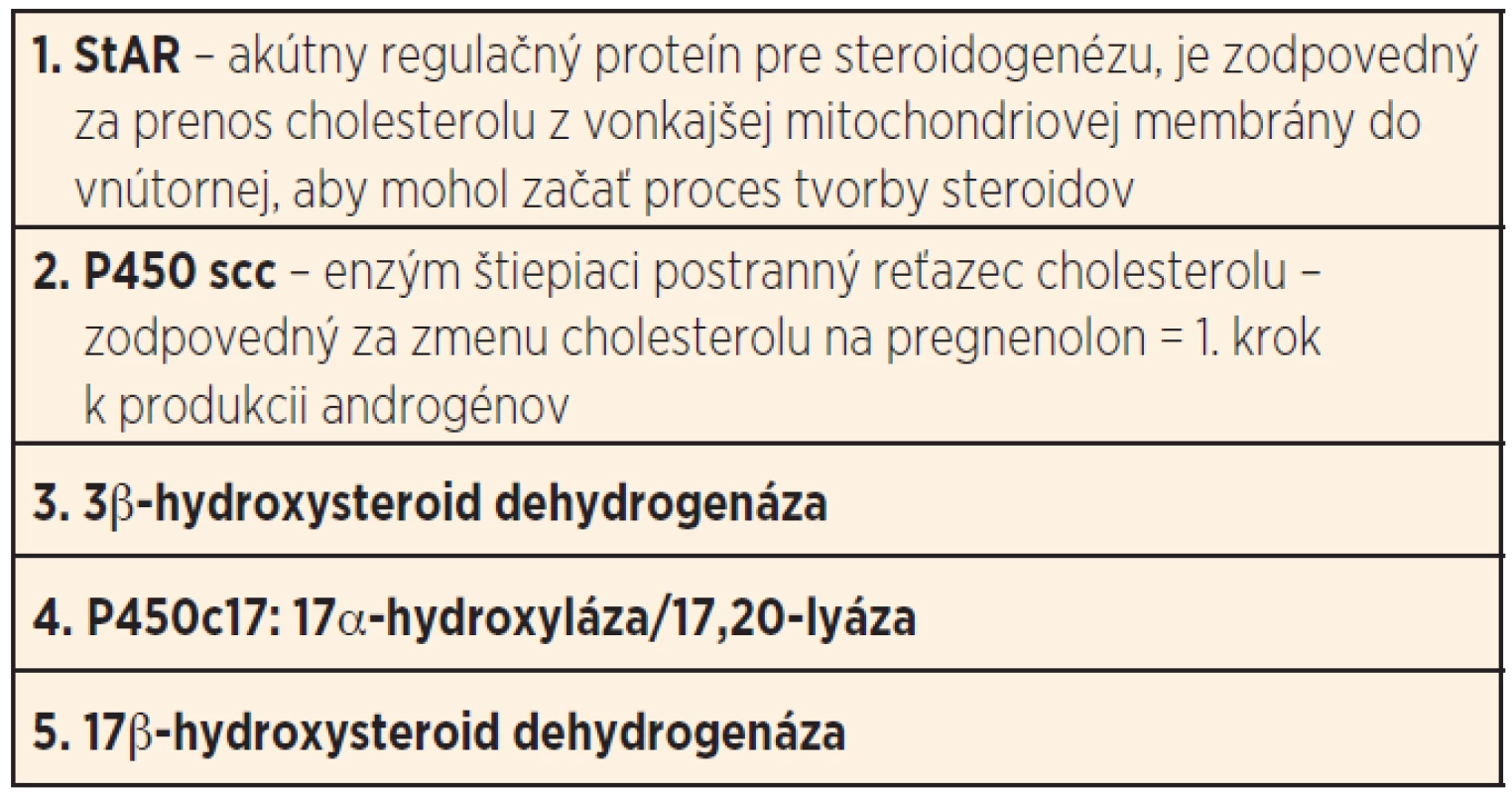
Pri defekte enzýmu 5α-reduktázy, ktorý katalyzuje premenu testosterónu na dihydrotestosterón, sa vytvárajú ambisexuálne vonkajšie genitálie. Testes zostávajú intaktné, väčšinou lokalizované intraabdominálne či v ingvínach. Vyvinú sa vnútorné mužské pohlavné orgány. V puberte nastáva virilizácia, ale so slabým ochlpením, neobjavuje sa gynekomastia. Spermatogenéza býva zhoršená [9]. Prostata chýba, alebo je hypoplastická. Laboratórne sú bazálne hladiny testosterónu normálne (horná hranica) alebo zvýšené, hladina dihydrotestosterónu je nízka, je zvýšený pomer testosterón/dihydrotestosterón v sére, čo je výrazné najmä pri stimulačnom teste s hCG [10].
Pri hypoplázii Leydigových buniek sa v dôsledku inaktivačnej mutácie génu pre LH/hCG receptor nemôžu správne vyvinúť Leydigove bunky a následne je porušená sekrécia androgénov [11]. U postihnutých jedincov je preto narušená virilizácia plodu a v pubertálnom období nedochádza k adekvátnemu vývoju sekundárnych pohlavných znakov. Pri I. type ochorenia je kompletne blokovaný prenos signálu po stimulácii LH či hCG. Vzniká ženský fenotyp vonkajších genitálií, so slepo končiacou vagínou. Prítomné testes bývajú nezostúpené, histologicky bývajú vyvinuté seminiformné tubuly, Leydigove bunky však nie sú prítomné, alebo sú prítomné len nezrelé formy. Postihnuté semenníky produkujú funkčný AMH, v dôsledku čoho nie sú prítomné vnútorné ženské pohlavné orgány. V dôsledku nedostatku androgénov nedochádza k fyziologickému vývoju štruktúr pochádzajúcich z Wolffovho duktu, v literatúre sú však popisované prípady s prítomnosťou rudimentárneho epididymis a vas deferens. V období puberty sa ochorenie prezentuje primárnou amenoreou a chýbaním sekundárnych pohlavných znakov. Pri II. type ochorenia je prenos signálu blokovaný len čiastočne. Tento typ má široké spektrum klinického obrazu. Väčšina pacientov má zjav vonkajších genitálií viac mužský, s hypospádiou alebo mikropenisom. Semenníky sú nezostúpené, alebo i v skróte. Vnútorné ženské pohlavné orgány nie sú vyvinuté a vnútorné mužské pohlavné orgány sú vyvinuté v závislosti od zostatkovej funkcie LH/hCG receptoru. V puberte nastupuje čiastočná virilizácia [12]. Laboratórne je prítomná veľmi nízka bazálna aj stimulovaná hladinu testosterónu a nie sú zvýšené hladiny prekurzorov testosterónu. Hladina LH je vysoká a hladina FSH je buď normálna, alebo zvýšená.
ZÁVER
Poruchy pohlavného vývoja sa vyskytujú približne u 1 : 4500 živo narodených detí [13]. Určiť dieťaťu správne pohlavie, predpokladať jeho budúcu možnú funkciu, možnosti chirurgickej korekcie, schopnosť normálneho pohlavného života a fertilitu jedinca, je niekedy v prvých dňoch života ťažké. Preto rozhodnutie o ďalšom vývoji pacienta nemôže zostať len na neonatológoch.
Podľa konsenzu odborníkov z Lawson Wilkins Pediatric Endocrine Society a Európskej spoločnosti pre detskú endokrinológiu by každé dieťa s poruchou diferenciácie vonkajších genitálií malo podstúpiť v novorodeneckom veku komplexný diagnostický postup [4]. Na základe interdisciplinárneho konzília skúsených odborníkov by malo mať, v spolupráci s rodičmi, čo najskôr určené pohlavie a terapeutický plán.
Došlo: 29. 12. 2011
Přijato: 30. 8. 2012
MUDr. Zuzana Blusková
II. Detská klinika LFUK a DFNsP
Limbová 1
833 40 Bratislava
Slovenská republika
e-mail: zuzana.bluskova@gmail.com
Sources
1. Svechnikov K, Landreh L, Weisser J, et al. Origin, development and regulation of human Leydig cells. Horm Res Paediatr 2010; 73 : 93–101.
2. Nef S, Parada LF. Hormones in male sexual development. Genes&Dev 2000; 14 : 3075–3086.
3. Hughes IA. Minireview: Sex differentiation. Endocrino-logy 2001; 142 : 3281–3287.
4. Lee PA, Houk CHP, Ahmed SF, Hughes A. Consensus statement on management of intersex disorders. Pediatrics 2006; 118 : 488–500.
5. Galani A, Kitsiou-Tzeli S, Sofokleous CH, et al. Androgen insensitivity syndrome: clinical features and molecular defects. Hormones (Athens) 2008; 7 : 217–229.
6. Swanson ML, Coronel EH. Complete androgen insensitivity with persistent Mullerian structures. A case report. J Reprod Med 1993; 38 : 565–568.
7. Tanaka Y, Matsuo N, Aya M, et al. Persistent Müllerian duct remnants in three siblings with partial androgen insensitivity. Horumon To Rinsho 1995; 43 : 3–8.
8. Miller WL, Auchus RJ. The molecular biology, biochemistry, and physiology of human steroidogenesis and its disorders. Endocr Rev 2011; 32 : 81–151.
9. Lisá L. Poruchy gonád na genetickém podkladě. In: Lisá L, Seemanová E, Zuntová A. Poruchy funkce gonád. Praha: Triton, 2004 : 11–93.
10. Imperato-McGinley J, Zhu YS. Androgens and male physiology the syndrome of 5alpha-reductase-2 deficiency. Mol Cell Endocrinol 2002; 198 : 51–59.
11. Latronico AC, Segaloff DL. Naturally occurring mutations of the luteinizing-hormone receptor: lessons learned about reproductive physiology and G protein – coupled receptors. Am J Hum Genet 1999; 65 : 949–958.
12. Mendonca BB, Domenice S, Arnhold IJ, Costa EM. 46, XY disorder of sexual development (DSD). Clin Endocrinol (Oxf) 2009; 70 : 173–187.
13. Pleskačová J, Šnajderová M, Lebl J. Poruchy pohlavního vývoje: Současná doporučená klasifikace a nové poznatky o poruchách vývoje gonád. Čes-slov Pediat 2010; 65 : 79–85.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2013 Issue 2-
All articles in this issue
- Přehled pacientů s diagnózou X-vázaného lymfoproliferativního onemocnění (XLP) diagnostikovaných v České republice a na Slovensku
- Emoční reakce vyvolaná textovými zdravotními varováními na obalech tabákových výrobků u dětí staršího školního věku a adolescentů
- Súvis génových polymorfizmov glutatión S-transferázy T1 a M1 s mikroalbuminúriou a incipientnou nefropatiou u detí s diabetes mellitus 1. typu
- Deficit transkripčního faktoru GATA-2: nová imunodeficience se širokým fenotypovým spektrem. První pacienti diagnostikovaní v České republice a přehled literatury
- Dievča s karyotypom 46, XY
- Vývoj střevní mikroflóry a rizika používání probiotik u imunosuprimovaných dětí
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Dievča s karyotypom 46, XY
- Vývoj střevní mikroflóry a rizika používání probiotik u imunosuprimovaných dětí
- Přehled pacientů s diagnózou X-vázaného lymfoproliferativního onemocnění (XLP) diagnostikovaných v České republice a na Slovensku
- Deficit transkripčního faktoru GATA-2: nová imunodeficience se širokým fenotypovým spektrem. První pacienti diagnostikovaní v České republice a přehled literatury
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

