-
Medical journals
- Career
Rabdomyolýza, stručná kazuistika a komentář
: M. Hrbek
: Interní oddělení nemocnice v Českých Budějovicích a. s ; Kazuistika byla přednesena na Třeboňských revmatologických dnech dne 4. 1. 2007
: Čes. Revmatol., 15, 2007, No. 4, p. 197-200.
: Case Report
Rabdomyolýza je syndrom charakterizovaný nekrózou buněk příčně pruhovaného svalstva a uvolněním jejich obsahu do krevního oběhu. Autor zdůrazňuje mezioborový charakter tohoto klinického syndromu a uvádí kazuistiku šestadvacetileté ženy, která byla po nezvyklé fyzické námaze (spinningu) léčena na interním oddělení. V komentáři k případu autor shrnuje základní fakta o patofyziologii, příčinách, klinickém obrazu a léčbě tohoto syndromu. V závěrečné diskusi se autor zamýšlí nad smyslem vyšetřování metabolických myopatií, které mohou být vzácnou, ale důležitou příčinou rabdomyolýzy. Význam případného odhalení vrozené myopatie spočívá v ovlivnění prognózy části nemocných preventivní léčbou.
Klíčová slova:
rabdomyolýza-myoglobin, metabolické myopatie, poruchy beta oxidace mastných kyselinÚvod
Rabdomyolýza je onemocnění či spíše syndrom, který bývá v učebnicích různých oborů zmiňován spíše stručně a rozptýleně ve více kapitolách. To svědčí o přesahu tohoto syndromu do různých medicínských odvětví. V literatuře bývá v poslední době toto onemocnění často citováno jednak autory z oblasti intenzivní medicíny a jednak autory z oborů jako je praktické a sportovní lékařství. Pokud jde o intenzivní medicínu, dle plzeňských autorů (1) se u souboru pacientů JIP signifikantní hypermyoglobinemie vyskytovala až v 70 % případů. V současné učebnici Intenzivní medicína autorů Ševčíka a spol. je užíván termín CINMA (critical illness myopathy) a dále termín akutní a chronická steroidní myopatie. Naproti tomu se rabdomyolýza po nadměrné fyzické zátěži někdy označuje jako syndrom netrénovaných sportovců. To jsou jen některé příklady až nepřehledné košatosti našeho tématu. Tradičně jsou pak myopatie častým chlebem revmatologů a pediatrů, opět s různým akcenty v tom kterém oboru. Navíc se rozvíjí diagnostika a to zejména v oblasti vrozených metabolických myopatií, o čemž bude pojednáno níže.
Popis případu
V naší kazuistice se jednalo o šestadvacetiletou ženu, která provozovala spinning, což je skupinové cvičení na stacionárních kolech. Poté pociťovala bolest nohou, která se stupňovala, všimla si tmavé moči. Nechala si na vlastním pracovišti (pracovala jako zdravotní sestra) vyšetřit sérum, kde byla zjištěna vysoká hodnota CK a myoglobinu, následovalo přijetí na interní oddělení.
Dle odebrané anamézy byla pacientka dosud zdráva, nemoci vnitřních orgánů negovala. V rodině se pouze jeden z prarodičů léčil s klouby, ale nejspíše se jednalo o osteoartrózu. Nemocná užívala pouze hormonální antikoncepci, byla kuřačka, údaj o požití alkoholu v době před cvičením nebyl v anamnéze odebrán. Objektivně při příjmu byla nemocná bez alterace, TK 140/80, TF 102 reg., na hrudníku a břiše byl normální interní nález, přítomno prosáknutí v okolí hlezenních kloubů.
Z vyšetření: EKG, UZ břicha a UZ srdce byly v mezích normy, pouze sonografista doporučil sledování parapelvické cysty pravé ledviny. V laboratorních vyšetřeních byla při příjmu elevace CK 1722 μkat/l, Ast 28 μkat/l, myoglobinu 16 000 μg/l, hodnota CRP byla 36,4, bilir. 4/9 μmol/l, krea 87 μmol/l, urea 3,23 mmol/l, při chemickém vyšetření moči jsme zjistili pH 5, bílkovinu na 1, krev na 4 kříže, v sedimentu pouze 0–4 ery, Leu 0–4, válce l–4. Vysoká „hematurie“ z chemického vyšetření moči byla falešně pozitivní při myoglobinurii.
Během pobytu se u pacientky rozvíjí otok měkkých tkání obou dolních končetin až do oblasti stehen, je přítomna výrazná bolestivost obou dolních končetin. Ošetřující lékařka zahájila energickou infuzní léčbu na interní JIP s dosažením hodinové diurézy 200–300 ml/h, do infuzí byl přidáván bikarbonát. Po jedenáctidenním pobytu dochází k poklesu CK z 1722 na 104 μkat/l, myoglobinu z 16 000 μg/l na 239 μg/l a AST z 28 μkat/l na 4,9 μkat/l. Dynamika poklesu hodnot CK a myoglobinu svědčila pro nepřítomnost další svalové destrukce a nepřímo potvrzovala prvotní názor, že se jednalo o ponámahové svalové poškození. Též klinický stav nemocné se výrazně zlepšil, po propuštění domů bylo pacientce doporučeno sledování renálních funkcí u praktického lékaře popř. nefrologa (clearance kreatininu byla před dimisí normální – 1,399 ml/s, tubulární resorpce snížena 0,933).
Komentář
Rabdomyolýza je definována jako syndrom charakterizovaný nekrózou buněk příčně pruhovaného svalstva a uvolněním jejich obsahu do cirkulace (1). Tíže onemocnění může kolísat od asymptomatických případů až po život ohrožující formy s akutním selháním ledvin a s minerálovým rozvratem. Typickou iontovou poruchou je hyperkalemie, dále hyperfosfatemie a hypokalcemie, která může být extrémní (1).
Připomeňme si, že je méně častý přímý inzult svalové buňky s jejím rozpadem. Klíčovým bodem pro poškození svalových buněk je i u crush syndromu narušení produkce energie ve svalu. Energetická deplece naruší funkci iontových pump (Na/K ATP-áza, výměnná Na/Ca pumpa a sarkoplazmatická kalcium sekvestrující pumpa) tak, že dojde k intracelulární kumulaci kalcia s aktivací proteáz a nakonec k rozpadu svalové buňky. Další destrukci svalu působí volné kyslíkové radikály (1). Co se dalších patofyziologických mechanismů týká, závažnost ledvinného selhání odpovídá objemovému množství poškozených svalů, k poškození ledvin dochází renální vasokonstrikcí, tubulární toxicitou rozpadových produktů myoglobinu a tubulární obstrukcí vysráženými bílkovinami, tento poslední faktor se však jeví podle posledních názorů méně důležitým (1, 7). Zásadním patofyziologickým mechanismem pro renální vasokonstrikci je fakt, že se kolující objem i rezerva tekutin přesunují do poškozených svalů, tento poznatek má své uplatnění v léčbě (1, 7).
Jaké jsou příčiny rabdomyolýzy? Jsou to všechny činitele, které vedou k výše uvedené přímé či nepřímé destrukci myocytu. Lze je jednoduše rozdělit na 2 velké skupiny, na přičiny traumatické a netraumatické. K traumatickým příčinám řadíme traumata se svalovou kompresí, crush syndrom, tyto případy lze ve velké míře sledovat ve válkách, při katastrofách apod. Zapomenout nemůžeme ani na traumata elektrickým proudem včetně zasažení bleskem, které vyvolají rabdomyolýzu asi v 10 % případů (7).
1. Příčiny rabdomyolýzy (zpracováno dle literatury uvedené v článku). 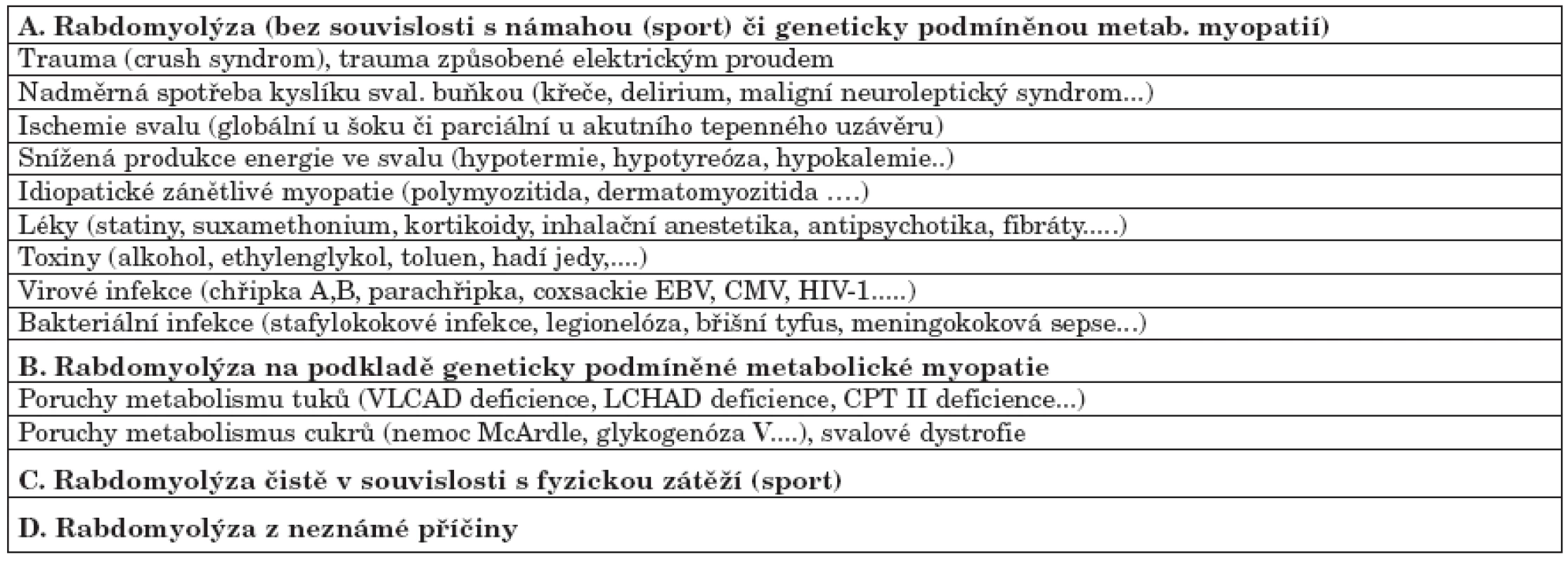
My se spíše budeme věnovat velké a nehomogenní skupině netraumatických přičin, kde určitý činitel naruší funkci iontových pump a produkci energie ve svalu. K nejčastějším netraumatickým příčinám rabdomyolýzy patří snížení dodávky kyslíku svalovým buňkám (globální hypoxie např. u šoku či lokální hypoxie u tepenného uzávěru končetiny), nadměrná spotřeba kyslíku svalovými buňkami (křeče, delirium, nadměrná fyzická aktivita, maligní hypertermie či maligní neuroleptický syndrom) či snížená produkce energie ve svalu z dalších příčin. K těm by patřila hypokalemie, hypotermie, hypotyreóza, metabolické myopatie atd.
Další širokou skupinou příčin netraumatické rabdomyolýzy jsou léky a toxické látky. Na prvním místě stojí alkohol, z nejdůležitějších léků jmenujme antipsychotika, fibráty, statiny, inhalační anestetika, kortikoidy, inhibitory MAO, propofol, suxametonium.
V praxi jsou významné nežádoucí účinky statinů a to zejména ve vyšších koncentracích. Léky, které inhibují cytochrom P-450 mohou zvyšovat sérové hladiny některých statinů a přispívat k zesílení jejich nežádoucích účinků. Proto se doporučuje v počátcích léčby statiny sledovat hladiny CK, jako významné se hodnotí zvýšení CK na 5–10násobek horní hranice normy. Dalšími rizikovými faktory pro vznik myopatie až rabdomyolýzy při terapii statiny jsou diabetes mellitus, hypotyreóza, ledvinné a jaterní postižení, věk nad 70 let, vysoké dávky statinů a kombinace statinů s fibráty (8).
Z toxinů jsou uváděny například hadí jedy (zmije, pakobra páskovaná – tiger snake) a toxiny některých ryb. Dle literatury existovala ve střední Evropě tzv. zátoková choroba (Haff disease) způsobená rybou burbot (mník), k příznakům nemoci patřily myalgie, svalová paralýza a selhání ledvin (7).
K rabdomyolýze může vést též infekce, ať už typičtěji infekce virová nebo bakteriální. Z virových onemocnění je nejčastěji do souvislosti se svalovým postižením uváděn virus chřipky A,B, ale i další: parachřipka, coxsackie, EBV, CMV atd. Z bakte-riálních onemocnění se uvádějí stafylokokové infekce, salmonelóza, břišní tyfus, legionelóza, listeróza, meningokoková sepse a další (2, 7).
Samostatnou kapitolou v etiologii svalových onemocnění, revmatologům důvěrně známou, jsou idiopatické zánětlivé myopatie, kdy je svalové poškození zprostředkováno imunologickými mechanismy. Patří sem polymyozitida, dermatomyozitida, myozitida asociovaná s jiným systémovým onemocněním či s malignitou a další (5).
Nutno podotknout, že existují jiné způsoby dělení příčin rabdomyolýzy než dělení na traumatické a netraumatické. V Cecil textbook of medicine z roku 2004 se uvádí dělení na tři kategorie, za prvé rabdomyolýza čistě po fyzické zátěži (pure exertional rhabdomyolysis), za druhé rabdomyolýza v souvislosti s dědičně podmíněnými defekty (genetically transmitted defect leading to rhabdomyolysis) a za třetí rabdomyolýza z příčin ostatních (nonhereditary nonexertional rabdomyolysis).
Pokud jde o diagnostiku tohoto syndromu, pak v klinickém obraze dominuje svalová bolest, slabost, ztuhlost a otok svalů, může být přítomno tmavé zbarvení moči, nicméně řada nemocných má minimální či žádné typické potíže. V séru je přítomna elevace myoglobinu, CK, AST a LDH, v moči lze stanovit myoglobin (respektive proteinurii a hematurii bez přítomnosti erytrocytů v močovém sedimentu). Klíčovou roli v rozlišení příčin rabdomyolýzy samozřejmě hraje anamnéza. Ve speciální diagnostice příčin rabdomyolýzy využíváme stanovení protilátek proti intracelulárním cytoplazmatickým nebo jaderným antigenům (vedle standardních imunologických vyšetření zejména MSA – pro myozitidu specifické protilátky), lze provést biopsii svalu či prokazovat multifokální elektromyografické změny při EMG. Dále je při pátrání po příčinách rabdomyolýzy vhodné vyšetřit sérologii virů chřipky, coxsackie a dalších a při pochybnostech provést kultivační vyšetření, abychom vyloučili aktivní bakteriální infekci.
U nemocných, u nichž máme podezření na metabolický podklad onemocnění, zajistíme ve specializované laboratoři nejen metabolické vyšetření krve a moči, ale též enzymatická a molekulární vyšetření v izolovaných lymfocytech nebo kultivovaných fibroblastech (3). Moderním způsobem diagnostiky CPT II deficience, zřejmě nejčastější poruchy lipidového metabolismu, je tandemová hmotnostní spektrofotometrie (4, 9).
V léčbě rabdomyolýzy stojí dle logiky věci na prvém místě kauzální opatření vedoucí k ostranění příčiny rozpadu svalových buněk. V závislosti na této příčině se může jednat o zprůchodnění cévy u akutního tepenného uzávěru, o fasciotomii při compartement syndromu, o léčbu infekce, o podání dantrolenu či bromokryptinu při maligním neuroleptickém syndromu či o vysazení léku (kortikoid, hypolipidemikum), který vedl k poškození svalu. Ne všude ovšem umíme kauzální příčinu odhalit či dostatečně ovlivnit.
Současně s kauzálními opatřeními přistupujeme co nejrychleji k volumexpanzi. Substituce tekutin je klíčovým postupem, doporučuje se dosažení hodinové diurézy cca 200–300 ml/h. Důležitost doplnění extracelulárního objemu tekutin lze ilustrovat na příkladu crush syndromu, kdy se doporučuje započetí infuzní léčby ještě před vyproštěním nemocného z trosek, jak je z výše uvedených patofyzologických poznámek zřejmé, jedná se o prevenci akutního renálního selhání.
Jako další opatření, ve kterém panuje shoda, lze uvést alkalizaci moči s dosažením pH 7,0, čehož lze dosáhnout přidáním bikarbonátu do infuzí. Jiná léčebná opatření, jako je například podání antioxidantů, nemají oporu v medicíně založené na důkazech. Pokud jde o vedení léčby, je doporučováno (1) raději sledovat sérové postupy myoglobinu než CK, neboť myoglobin má kratší eliminaci a rychleji reaguje na vývoj onemocnění. Hemodialýza je indikovaná u akutního selhání ledvin. Prognóza nemocných s rabdomyolýzou závisí na povaze základního onemocnění, mortalita nemocných s akutním selháním ledvin je významně vyšší. U nemocných, kteří přežijí, však dochází v naprosté většině případů do 3 měsíců k reparaci funkce ledvin, a to i u plně rozvinutého renálního selhání (1).
Korekce hypokalcemie by měla být uvážlivá, neboť může vést k významné depozici kalciových solí v poškozených svalech.
Diskuse
Diskuse nás může přivést k faktu, že přibývá fitness center i případů rabdomyolýzy diagnostikované po nepřiměřené fyzické zátěži. Ozývají se hlasy o syndromu netrénovaných sportovců, lektoři spinningu mají své klienty vést k pozvolné fyzické zátěži a k dostatečnému přísunu tekutin (6). Nabízí se otázka, proč nadměrná fyzická zátěž u některých jedinců vyvolává vážné svalové poškození. Odpovědí může být přítomnost dalších faktorů pro rozvoj rabdomyolýzy. Co se však skrývá pod pojmem „další faktory“? Vyloučíme-li infekty, požití alkoholu, léků či tiše probíhající idiopatické zánětlivé myopatie, dostáváme se do hájemství příčin vzácných, tj. zejména metabolických myopatií. Autoři Kabíček a kol. (3) doporučují již při prvé atace netraumatické rabdomyolýzy po fyzické zátěži pomýšlet u dětí a adolescentů na dosud asymptomatické či oligosymptomatické svalové onemocnění. Za všechny jmenujme poruchy metabolismu tuků: LCHAD deficience (long-chain 3-OH-Acyl-CoA dehydrogenase), VLCAD deficience (very long-chain Acyl-CoA dehydrogenase), CPT II deficience (cartnitin palmytoyl transferase II), poruchy metabolismu sacharidů: Mc Ardle disease, glykogenosa V..atd., svalové dystrofie (morbus Becker-Duchenne) a další. V léčbě u pacientů s poruchou v oblasti beta oxidace mastných kyselin se uplatňuje frekventní výživa se sníženým obsahem tuků. Tito nemocní by neměli dlouhodobě lačnit pro nebezpečí neketotické hypoglykemie. Supplementace tuků se podává podle toho, které tuky může dle typu metabolické poruchy nemocný utilizovat. Při akutní atace rabdomyolýzy nejasné etiologie, kde můžeme mít podezření na metabolickou myopatii, by měla být vždy podána infuze glukosy a ionty, aby byly pokryty energetické nároky organismu. K režimovým opatřením u nemocných s metabolickou myopatii patří též zákaz vyčerpávajícího svalového tréninku.
Naší nemocnou jsme seznámili s výše uvedenými možnostmi vyšetření a dodatečně jí nabídli vyšetření metabolických myopatií, pacientka se zatím rozhoduje, zda jej podstoupí.
Pokud bychom na závěr diagnostický a vyšetřovací postup v naší kazuistice srovnali s možnostmi uvedenými ve výše uvedeném přehledu, tak vidíme, že k diagnóze nás dovedla anamnéza, která v medicíně často již bez dalších sofistikovaných vyšetření vede k cíli. Průběh onemocnění a dobrá reakce na léčbu s rychlou eliminací CK a myoglobinu podpořily naše původní očekávání, že onemocnění bylo způsobeno enormní fyzickou námahou. V případě nedostatečné léčebné odpovědi bychom samozřejmě museli využít další ze škály výše uvedených vyšetření. Jak již uvádíme v diskusi, není dosud jednoty v tom, kdy u pacientů s rabdomyolýzou vyšetřovat vrozené metabolické myopatie. Vzhledem k možnosti příznivě ovlivnit prognózu skupiny nemocných s poruchou na úrovni beta oxidace mastných kyselin se přikláníme k doporučení vyšetřovat přítomnost metabolických myopatií u dětí a adolescentů s prvou atakou rabdomyolýzy po fyzické zátěži, tím spíše pak tam, kde by se svalové obtíže opakovaly. K důslednému vyšetřování zejména CPT II deficience se přiklání v současné literatuře také Bzdúch (4).
Na samém konci článku bych nám všem, často specialistům různých oborů, popřál, abychom při popisu a diagnostice méně častých a hůře zařaditelných nemocí mluvili společnou řečí a abychom naše nemocné dokázali léčit dobře.
MUDr. Martin Hrbek
Interní oddělení nemocnice v Českých Budějovicích a.s.
Ulice Boženy Němcové 54
370 87 České Budějovice
e-mail: martin.hrbek@centrum.cz
Sources
1. Kroužecký A, Matějovič M, Rokyta R jr., Novák I. Rabdomyolýza – mechanismy vzniku, příčiny, důsledky a léčba. Vnitř lék 2003; 49 : 668–72.
2. Ambrožová H, Hobstová J. Rhabdomyolýza – příčiny, klinický obraz a léčba, naše zkušenosti. Klin mikrobiol infec lek 2000; 6: l39–42.
3. Kabíček P, Chrastina P, Dvořáková L, Magner M, Zeman J. Rabdomyolýza po fyzické námaze – benigní nález nebo projev závažného onemocnění. Prakt lek 2006; 86 : 393–95.
4. Bzdúch V. Najčastejšia genetická príčina rabdomyolýzy. Vnitř lek 2004; 50 : 82.
5. Vencovský J, Jarošová K, Tomasová Studýnková J, et al. Polymyositida a dermatomyositida – projekt Národního registru revmatických chorob. Čes revmatol 2002; 10 : 98–l05.
6. Herle P, Krobová E, Elyjiwová O, Velebová P. Rabdomyolýza – syndrom netrénovaných sportovců? Prakt lek 2006; 86 : 90–92.
7. Holt SG. Rhabdomyolysis and acute renal failure. Causes and therapy. Intensive Care 2002; 9: l7–25.
8. Soška V. Hypolipidemika. In: Vítovec J, Špinar J a kol. Ed. Farmakoterapie kardiovaskulárních onemocnění, Praha, Avicenum 2004; l73–l82.
9. Hoffman GF Dědičné metabolické poruchy. Praha Grada 2006; 416 stran
10. Ševčík P, Černý V, Vítovec J, et al. Intenzivní medicína. Praha, Galén 2003; 422 stran.
Labels
Dermatology & STDs Paediatric rheumatology Rheumatology
Article was published inCzech Rheumatology

2007 Issue 4-
All articles in this issue
- Plasma cells as a marker predicting the outcome of anti-TNF therapy
- Procalcitonin in the diagnosis of bacterial infection in patients with autoimmune rheumatic diseases
- Musculoskeletal manifestations in celiac disease
- Rhabdomyolysis, a brief case report and commentary
- Hip joint destruction and secondary synovial chondromatosis in a patient with rheumatoid arthritis
- Czech Rheumatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Rhabdomyolysis, a brief case report and commentary
- Hip joint destruction and secondary synovial chondromatosis in a patient with rheumatoid arthritis
- Musculoskeletal manifestations in celiac disease
- Procalcitonin in the diagnosis of bacterial infection in patients with autoimmune rheumatic diseases
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

