-
Medical journals
- Career
Výskyt echokardiograficky detekovatelných kardiovaskulárních manifestací systémového lupus erythematodes
Authors: D. Tegzová; P. Jansa 1; D. Ambrož 1; T. Paleček 1; L. Dušek 2
Authors‘ workplace: Revmatologický ústav v Praze ; II. interní klinika kardiologie a angiologie Všeobecné fakultní nemocnice a 1. LF UK v Praze 1; Institut biostatistiky a analýz Masarykovy univerzity v Brně 2
Published in: Čes. Revmatol., 15, 2007, No. 2, p. 64-71.
Category: Original Papers
Overview
Cíl.
Cílem práce bylo zjistit výskyt jednotlivých kardiovaskulárních projevů systémového lupus erythematodes (SLE) detekovatelných echokardiograficky, popsat jejich typ, stupeň závažnosti a zjistit vztah k jednotlivým charakteristikám SLE.Metodika.
Bylo vyšetřeno 56 nemocných se SLE. Pacienti absolvovali echokardiografické vyšetření, které zahrnovalo posouzení struktury a funkce levé komory srdeční s hodnocením diastolické funkce pomocí tkáňové dopplerovské echokardiografie, posouzení struktury a funkce chlopenního aparátu, posouzení struktury a funkce pravé komory s hodnocením její systolické funkce a posouzení tlaků v plicnici a změn v perikardu (parametry: IVSd (šíře septa), ZSd (šíře zadní stěny), LKs/m² (systolický rozměr levé komory), LKd/m² (diastolický rozměr levé komory), EDV/m² (enddiastolický objem levé komory), ESV/m² (endsystolický objem levé komory), EF (ejekční frakce), velikost srdečních oddílů v jednorozměrném zobrazení, přítomnost významné trikuspidální regurgitace a její vrcholový gradient, dále Tei index). Při klinickém vyšetření byla hodnocena základní demografická data, typ imunosupresivní léčby a délka její aplikace, dávka kortikosteroidů, kterou nemocní užívali, přítomnost autoprotilátek (anti ds DNA, anti Ro, La, ACLA), přítomnost orgánových projevů a aktivita nemoci dle skóre SLEDAI. Byl zjišťován vztah mezi jednotlivými echokardiografickými patologiemi a parametry SLE.Výsledky.
Byly nalezeny různé typy chlopenních regurgitací u 13 pacientů a perikardiální výpotek u 8 pacientů Nebyly zjištěny známky přítomnosti plicní hypertenze. Pohlaví pacientů výskyt kardiologických patologií neovlivňovalo. Výskyt perikardiálního výpotku i chlopenních regurgitací souvisel s věkem pacienta. Vyšší výskyt byl u nemocných starších než 45 let. Doba trvání SLE není ve sledovaném souboru významně asociována s výskytem těchto patologií a totéž bylo prokázáno i pro všechny ostatní sledované parametry SLE. Byla zjištěna velmi silná korelace mezi výskytem perikarditidy a postižením plic, která není ovlivňována ani délkou trvání choroby ani věkem pacientů.Výskyt chlopenních regurgitací je statisticky významně zvýšený u pacientů s postižením vnitřních orgánů, a to specificky plic a CNS. Nebyla prokázána vazba k postižení ledvin. Bylo zjištěno statisticky méně chlopenních regurgitací u pacientů s kožním nebo kloubním postižením. Perikarditida koreluje pozitivně se zvýšenými hodnotami Tei indexu. Vyšší hodnoty PG max na trikuspidální regurgitaci korelují s plicní manifestací SLE a s vyšší aktivitou SLE (SLEDAI index > 5).Závěr.
SLE se manifestuje řadou kardiovaskulárních komplikací. V našem souboru se echokardiograficky detekovatelné patologie (zejména chlopenní regurgitace a perikardiální výpotek) kumulují u pacientů s přítomností orgánových projevů a u aktivního SLE (nejvíce při postižení plicního intersticia), bez ohledu na dobu jeho trvání. U starších pacientů s plicním postižením s dlouho trvajícím SLE byly zjištěny významně zvýšené hodnoty Tei indexu. U aktivního SLE s plicními projevy jsou zvýšeny hodnoty Pg max na trikuspidální chlopni. U ostatních echokardiografických parametrů nebyly v této analýze zjištěny žádné korelace ani vztahy k intenzitě a závažnosti SLE.Klíčová slova:
systémový lupus erythematodes, kardiovaskulární projevy, echokardiografie, perikarditida, plicní hypertenzeÚvod
Kardiovaskulární komplikace nejsou pro onemocnění systémovým lupus erythematodes (SLE) nejtypičtější komplikací, ale o to více jsou závažné, neboť se vyvíjejí často skrytě a ne vždy na ně ošetřující lékař včas myslí. Kardiologické projevy jsou typické pro druhou fázi onemocnění SLE, kdy se mimo ně projevují i jiné závažné, obvykle ireverzibilní orgánové změny (1, 2). Některé kardiální projevy, jako je např. perikarditida, jsou ale naopak časným projevem již v úvodu nemoci a jsou tak typické, že jsou začleněny mezi diagnostická kritéria (sérozitida, resp. perikarditida).
Ve srovnání se zdravou populací mají nemocní se SLE vyšší morbiditu i mortalitu, na níž mají významný podíl kardiovaskulární komplikace (3–5). Hlavní příčinou vyšší mortality z kardiologického hlediska jsou důsledky akcelerované aterosklerózy a plicní arteriální hypertenze (6, 7). Počet úmrtí v souvislosti s důsledky kardiovaskulárních komplikací pravděpodobně dokonce převyšuje počet úmrtí v souvislosti s vlastní aktivitou choroby. V současné době není jednoznačně jasné, co je predilekčním faktorem vývoje a závažnosti průběhu kardiovaskulárních komplikací u SLE. Proto není ani k dispozici jasně formulované doporučení pro metodiku preventivního vyšetřování a časného záchytu těchto komplikací (8, 4).
Z jednotlivých patologických nálezů kardio-vaskulárních projevů se nejčastěji vyskytuje perikarditida, která je udávána u 20–30 % nemocných (ale až u 60 %), endokarditida (18–74 %), myokarditida, vaskulitida (koronaritida), antifosfolipidový syndrom, plicní hypertenze (4–14 %), akcelerovaná ateroskleróza (13 %) (1, 8, 9). V této oblasti se jedná zejména o syndrom anginy pectoris, akutní infarkt myokardu a ischemii periferních cév, kdy úmrtnost je 9krát vyšší než u běžné populace. 53 % pacientů se SLE má více než tři rizikové faktory ischemické choroby srdeční. Roční incidence akutního infarktu myokardu je u běžných žen 0,001, u SLE 0,005 (9, 10). Hlavním rizikovým faktorem je nejspíše terapie kortikosteroidy a indukovaná hyperlipoproteinemie (11).
Cíl studie
V Revmatologickém ústavu jsme ve spolupráci s II. klinikou kardiologie a angiologie VFN a 1. LF UK realizovali grantový projekt zaměřený na včasnou detekci kardiovaskulárních komplikací u SLE. Jednou jeho částí bylo i hodnocení kardiovaskulárních patologií nalezených při screeningovém echokardiografickém vyšetření (2, 12). Cílem této práce bylo zjistit výskyt jednotlivých echokardiografických patologií, popsat jejich typ, stupeň závažnosti a zjisit vztah k vlastnímu základnímu onemocnění SLE, tedy popsat eventuální závislost na jednotlivých charakteristických vlastnostech SLE. Mezi ně patřila charakteristika nemocných, délka onemocnění, léčba a jednotlivé parametry aktivity SLE včetně eventuální závislosti na autoprotilátkovém spektru, které je typické pro SLE.
Metodika
Do studie byli zařazeni nemocní se SLE, jejichž diagnóza byla stanovena podle kritérií Americké revmatologické společnosti (ACR). Bylo vyšetřeno 56 nemocných se SLE. Pacienti absolvovali jednorázové echokardiografické vyšetření a dále podrobné vyšetření revmatologické, zaměřené na vlastní onemocnění SLE.
Provedené echokardiografické vyšetření zahrnovalo posouzení struktury a funkce levé komory srdeční s hodnocením diastolické funkce pomocí tkáňové dopplerovské echokardiografie, posouzení struktury a funkce chlopenního aparátu, posouzení struktury a funkce pravé komory s hodnocením její systolické funkce a posouzení tlaků v plicnici a změn v perikardu. Byly hodnoceny parametry: IVSd (šíře septa), ZSd (šíře zadní stěny), LKs/m2 (systolický rozměr levé komory), Lkd/m2 (diastolický rozměr levé komory), EDV/m2 (enddiastolický objem), ESV/m2 (endsystolický objem), EF (ejekční frakce), a dále rozměry srdečních oddílů hodnocené při jednorozměrném a dvourozměrném zobrazení, přítomnost významné regurgitace na trikuspidální chlopni hodnocené semikvantitativně, vrcholový gradient regurgitační trysky na trikuspidální chlopni a Tei index, vypočítávající funkci pravé komory srdeční dopplerovskou metodou dle průtokových charakteristik.
Při klinickém vyšetření byla hodnocena základní demografická data jako je pohlaví a věk nemocných, délka trvání nemoci, typ imunosupresivní léčby a délka její aplikace, dávka kortikosteroidů, kterou nemocní užívali, a aktivita nemoci hodnocená dle standardního skórovacího systému SLEDAI. Dále byly hodnoceny některé autoprotilátky, které jsou typické pro SLE, jako přítomnost anti ds DNA autoprotilátek a antikardiolipinových protilátek, a přítomnost eventuelních orgánových komplikací, které rovněž jsou pro SLE typické, jako je např. lupusová nefritida, neuropsychiatrické projevy nebo plicní postižení.
Při statistickém hodnocení byl zjišťován vztah mezi jednotlivými nalezenými echokardiografickými patologiemi a parametry SLE.
Statistické zpracování
Statistické zpracování dat bylo provedeno Institutem biostatistiky a analýz Masarykovy univerzity v Brně. Veškeré statistické testy byly aplikovány na celý soubor primárních dat bez předchozího vylučování hodnot a pacientů. Hodnota α < 0,05 byla aplikována jako hranice statistické významnosti změn a rozdílů ve všech použitých testech. Primární data všech proměnných byla hodnocena standardními robustními statistickými parametry (medián a percentily, hodnocení relativních četností). Vztahy mezi dvěma nebo více kategoriemi kategoriálních parametrů byly posuzovány ML testem dobré shody a Fisherovým exaktním testem. Srovnání dvou nebo více skupin pacientů v echokardiografických parametrech bylo provedeno pomocí standardního t-testu a analýzy rozptylu (ANOVA), model jednoduchého třídění (13, 14).
Výsledky
1. Charakteristika souboru (tab. 1)
Vstupní charakteristika souboru byla provedená robustní statistikou. Je viditelná převaha žen v souboru (84 %), což je pro onemocnění SLE naprosto typické. Z hlediska SLE je soubor dostatečně heterogenní (reprezentativní) a umožňuje analýzu jak málo aktivní choroby, tak i velmi vážných komplikací včetně poškození vnitřních orgánů. Průměrný věk nemocných při stanovení diagnózy SLE byl 38 let a v době vyšetření 46 let, průměrná délka trvání nemoci byla 6 let. Průměrná délka imunosupresivní terapie byla 6 let, přičemž většina byla léčena antimalariky (38 %) nebo azatioprinem (34 %). Aktivita nemoci dle skóre SLEDAI byla u 70 % nemocných vyšší než 5, výskyt autoprotilátek anti ds DNA byl u 43 %, anti Ro u 25 %, anti La u 23 % a ACLA u 23 %. Z projevů SLE byla nejčastěji přítomna manifestace kloubní (46 %), a kožní (43 %), závažné orgánové projevy jako lupusovou nefritidu mělo 30 %, postižení plic ve smyslu plicní intersticiální fibrózy mělo 18 % nemocných. Hypertenzi mělo 5,4 % pacientů. Veškeré údaje jsou podrobně uvedeny v tabulce 1.
Table 1. Charakteristika souboru. 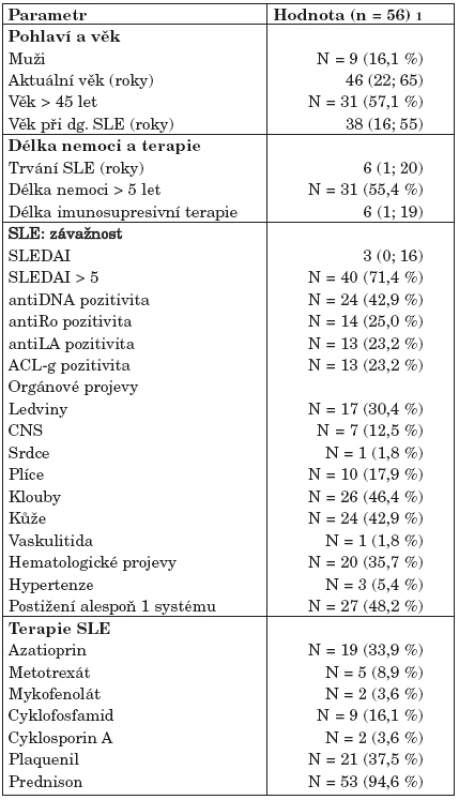
1Kontinuální proměnné jsou sumarizovány jako medián s 5 %–95 % percentily (v závorkách). Kategorie jsou vyjádřeny jako N a %. 2. Vstupní charakteristika vyšetřovaných kardiografických parametrů (tab. 2)
Z hlediska kardiologických patologií nebyly ve zhodnocených parametrech zjištěny žádné významné echokardiografické nálezy. Z jasně prokázaných patologií byly nalezeny různé typy chlopenních regurgitací (v databázovém součtu celkem u 13 pacientů) a perikardiální výpotek u 8 nemocných. U žádného pacienta nebyly zjištěny echokardiografické známky přítomnosti plicní hypertenze, ale parametr Pg max u celkem N = 3 pacientů dosahuje hraničních hodnot 36–38 mm Hg.
Table 2. Echokardiografie a kardiologické patologie. 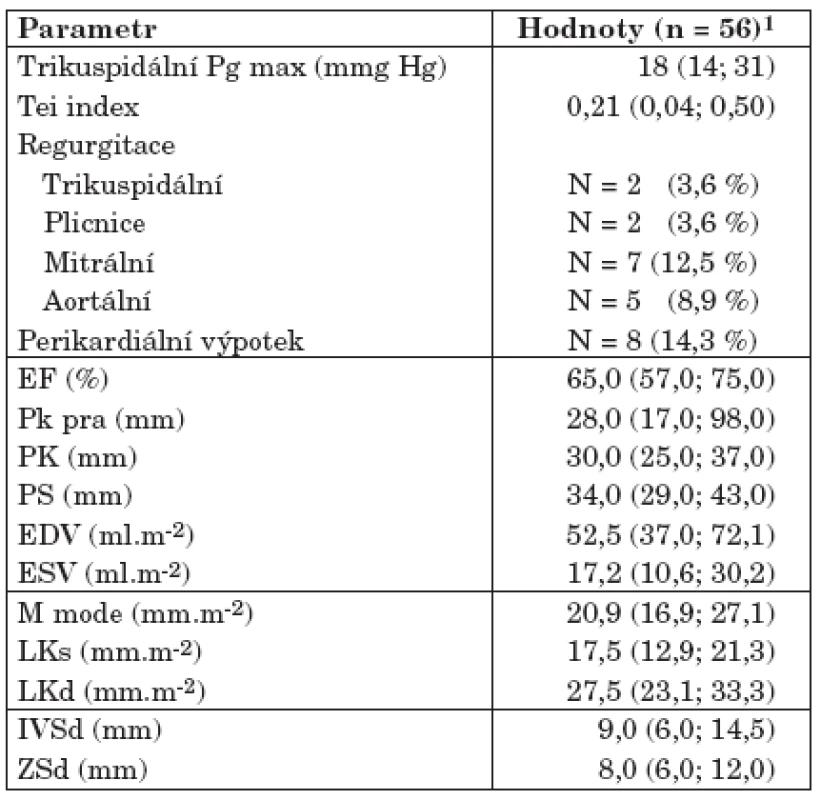
1Kontinuální proměnné jsou sumarizovány jako medián s 5 %–95 % percentily (v závorkách). Kategorie jsou vyjádřeny jako N a %. 3. Sumarizace vztahu mezi parametry pacientů a SLE a prokázanými kardiologickými patologiemi, tedy perikardiálními výpotky a chlopenními regurgitacemi (tab. 3)
Je evidentní, že soubor pacientů je kardiologicky spíše „zdravý“, všechny prokázané patologie se vyskytují v relativně nízkém procentu. Z důvodů hodnocení byl proveden databázový součet výskytů chlopenních regurgitací tak, aby bylo možné vůbec kalkulovat statistickou významnost, jednotlivé typy regurgitací nelze totiž odděleně vůbec hodnotit.
Table 3. Potenciální rizikové faktory dávané do souvislosti se SLE v korelaci s detekovanými kardiologickými patologiemi. 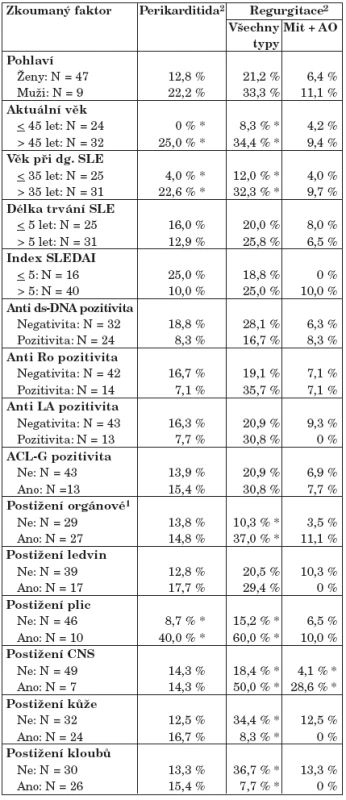
1Postižení aspoň jednoho důležitého orgánu (plíce, srdce, CNS nebo ledviny) 2Počet vyjádřených procent výskytu kardiologických patologií v daných řádcích *Známky statistické významnosti mezi kategoriemi uvedenými v řádcích (Fisherův exaktní test; p < 0,05) Pohlaví pacientů výskyt kardiologických patologií v našem souboru neovlivňuje. Výskyt perikardiálního výpotku i chlopenních regurgitací souvisel s věkem pacienta. Nemocní starší než 45 let měli signifikantně zvýšenou incidenci těchto patologií. Logicky se tento problém týká i věku při diagnostice SLE. Pacienti, u nichž se SLE projevil po 35. roce života, mají statisticky významně zvýšenou incidenci jak perikardiálního výpotku, tak i chlopenních regurgitací (počítáno pro všechny typy v součtu). Naopak doba trvání SLE není významně nijak asociována s výskytem těchto patologií a totéž bylo prokázáno i pro všechny markery aktivity lupusu (SLEDAI, anti ds DNA) i ostatní sledované parametry (anti Ro, anti LA. ACLG).
Velmi silná korelace byla prokázána mezi výskytem perikarditidy a postižením plic. Tato vazba je specificky statisticky významná a není ovlivňována ani délkou trvání choroby, ani věkem pacientů. Výskyt chlopenních regurgitací je statisticky významně zvýšený u pacientů s postižením vnitřních orgánů, a to specificky plic a CNS. Nebyla prokázána vazba k postižení ledvin.
Zcela opačný trend byl pro chlopenní regurgitace prokázán při sledování přítomnosti kožních a kloubních projevů, kdy bylo zjištěno statisticky méně chlopenních regurgitací u pacientů s tímto typem postižení. Vysvětlením může být, že pacienti s postižením kůže a/nebo kloubů nemívají často postižené vnitřní orgány, může tedy v našem souboru jít o příznivější průběh choroby než při postižení vnitřních orgánů, na jejichž přítomnost jsou právě chlopenní regurgitace vázány.
4. Návrh komplexní kategorizace pacientů se SLE ve vztahu ke kardiovaskulárním komplikacím (tab. 4)
Důvod k této analýze je ten, že SLE je charakterizovaný mnoha atributy a tyto spolu mohou, ale nemusejí souviset. Detailní pole parametrů (tak, jak s ním pracuje např. tab. 3) je pak redundantní a neodráží dostatečně ani terapeutickou, ani časovou charakteristiku choroby. Proto jsme provedli korelaci všech parametrů vážících se k SLE a dospěli jsme k definici tří skupin, se kterými jsme následně pracovali. Lze konstatovat, že tyto skupiny integrují různé ukazatele do homogenních celků.
Table 4. Komplexní hodnocení závažnosti SLE. 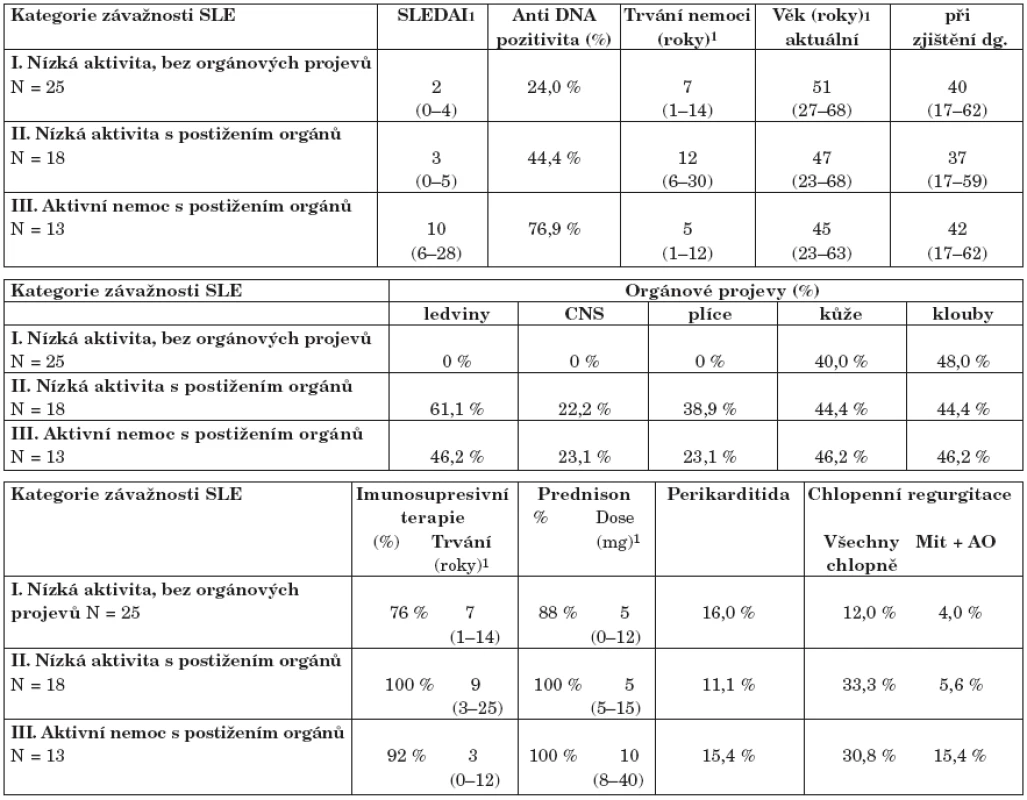
1Medián udávaný s 5 %–95 % percentily Skupina č. I.: minimální klinické projevy choroby, nízké hodnoty indexu SLEDAI i všech ostatních markerů aktivity choroby, bez přítomnosti orgánové manifestace. Je patrné, že jde o spíše krátce trvající chorobu, probíhající bez vážných komplikací s adekvátní léčbou. Nedochází ke kumulaci kardiologických potíží.
Skupina č. II.: mírně aktivní choroba, avšak s orgánovými projevy. Spíše dlouhotrvající choroba s terapeuticky udržovanou nízkou aktivitou, avšak s kumulací poškození vnitřních orgánů (hlavně ledviny, plíce) a se zvýšeným výskytem kardiologických komplikací, především chlopenních regurgitací.
Skupina č. III.: skupina evidentně s nejtěžším průběhem onemocnění, které, ačkoli probíhá relativně krátce (medián 5 let), je velmi aktivní a vede k výraznému poškození vnitřních orgánů. Léčba této skupiny je charakteristická vyššími dávkami prednisonu. Je v ní zvýšený výskyt chlopenních regurgitací, a to i na mitrální a na aortální chlopni.
Srovnání všech takto definovaných skupin pacientů dále ukazuje relativně nulovou korelaci mezi postižením kůže a kloubů a závažností nebo dobou trvání choroby. Kůže i klouby jsou v průměru postiženy u 45 % pacientů, a to napříč všemi skupinami. Dále je patrné, že zařazení pacienta do slabě nebo naopak silně „poškozené“ skupiny ne zcela souvisí s věkem. Ve všech třech skupinách se vyskytují pacienti všech věkových tříd a jejich současný věk kolísá v mediánu mezi 45 a 52 lety.
5. Kvantitativní analýza echokardiografických parametrů u skupin pacientů vytvořených dle závažnosti SLE, jak je uvedeno výše (tab. 5)
Analýza využívá komplexní kategorizace nemocných tak, jak byla definována v tabulce 4. Je patrné, že u většiny rozměrových a objemových parametrů neexistuje žádný prokázaný rozdíl mezi pacienty s mírným nebo vážným průběhem SLE. Tento závěr platí i pro detailní analýzu postižení jednotlivých orgánů nebo parametrů aktivity SLE (data nejsou ukázána). Jedinou výjimkou jsou parametry „Tei index“ (EA-ET)/ET) a „Pg max“ regurgitace na trikuspidální chlopni (gradient na trikuspidální chlopni). Oba parametry statisticky významně odlišují pacienty s těžším průběhem choroby od skupiny č. I, definované jako lehký průběh. Ačkoli ani Pg max, ani Tei nedosahují patologických hodnot, je patrné že jejich zhoršené hodnoty (= zvýšené Pg max i Tei index) souvisejí s těmi skupinami pacientů, které mají postiženy vnitřní orgány a mají i zjištěny echokardiografické patologie. Tato skutečnost byla tedy dále studována při dalších analýzách, jak jsou uvedeny v tabulkách 6 a 7.
Table 5. Echokardiografie ve vztahu ke třem skupinám SLE dle závažnosti. 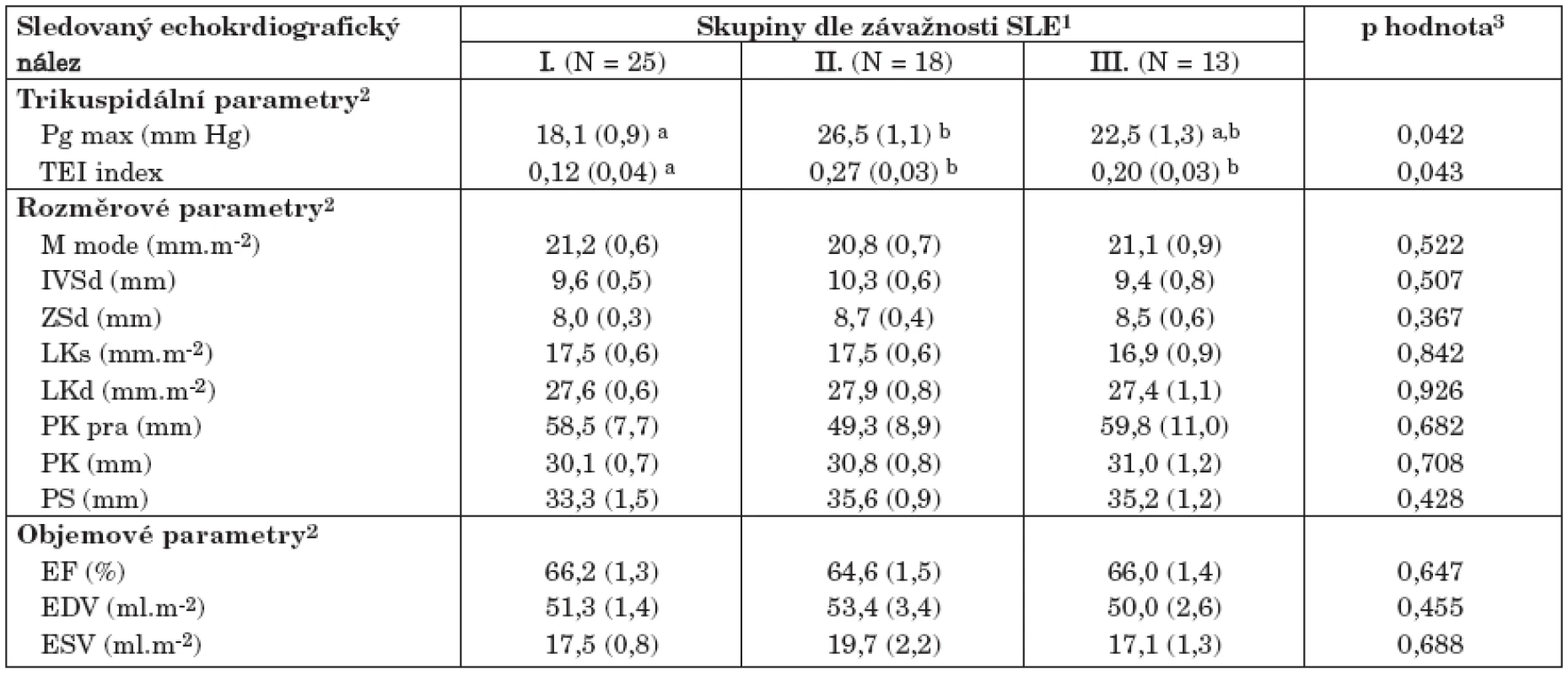
1Tři komplexní kategorie dle závažnosti SLE (viz též tab. 4): I. Nízká závažnost s nízkou aktivitou, bez orgánových projevů II. Nízká aktivita, ale s orgánovými projevy III. Aktivní nemoc s orgánovými projevy 2Čísla vyjadřují průměr doplněný standardní odchylkou (v závorkách) 3p hodnota rozdílu mezi skupinami pacientů I–III (jednosměrný test ANOVA; p < 0,05) a,bZnámky statistické významnosti mezi kategoriemi I–III v udávaných řádcích. Průměry značené odlišnými písmeny jsou navzájem statisticky významně odlišné (p < 0,05) 6. Kvantitativní analýza echokardiografických parametrů vybraných z tabulky č. 5 u pacientů s prokázanými kardiologickými patologiemi (tab. 6)
Výsledky dokazují, že zejména parametr Tei index významně souvisí s prokázanými kardiologickými patologiemi, specielně s chlopenními regurgitacemi a přítomností perikardiálního výpotku.
Table 6. Pg max a Tei index ve vztahu ke kardiologickým patologiím. 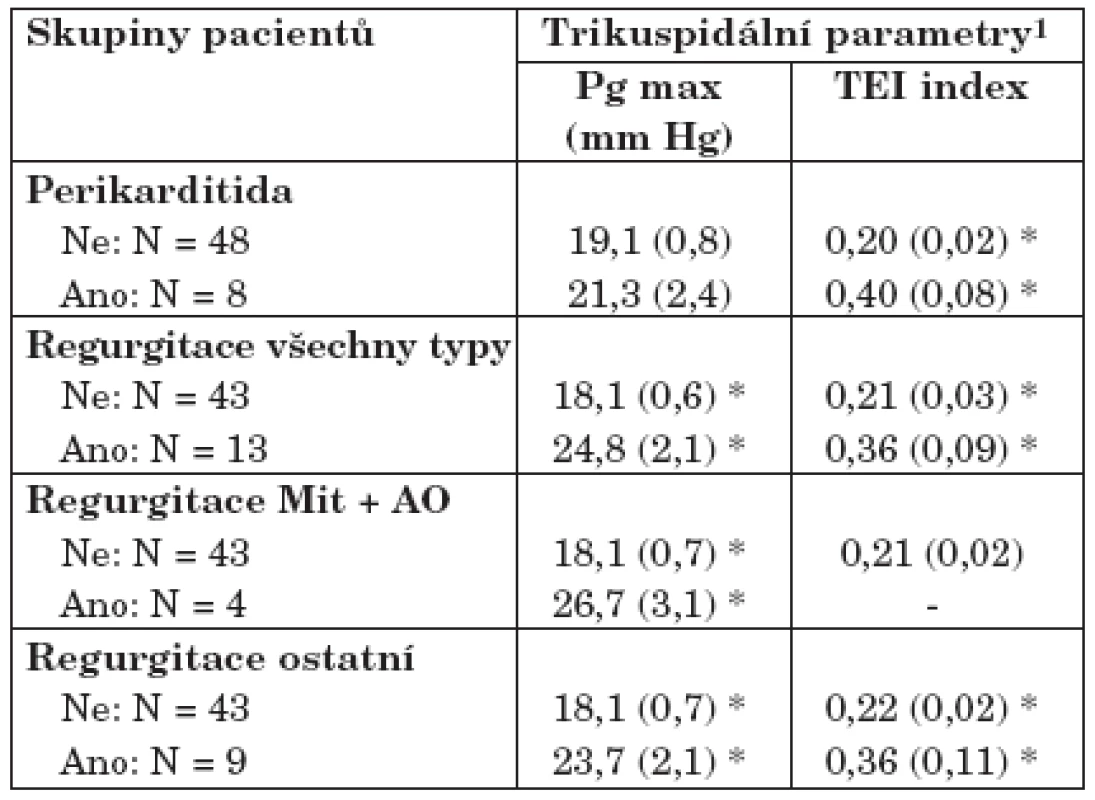
1Čísla vyjadřují průměr doplněný standardní odchylkou (v závorkách) *Označení statisticky významného rozdílu mezi uvedenými řádky (t-test; p < 0,05) 7. Kvantitativní analýza echokardiografických parametrů vybraných z tabulky č. 5 proti různým atributům SLE a charakteristikám pacientů (tab. 7)
Ani jeden z testovaných parametrů nesouvisí s pohlavím. Signifikantně zvýšené hodnoty Tei indexu byly zjištěny u spíše starších pacientů (> 45 let, kteří měli také SLE diagnostikován později, po 35. roce života). Pro tyto pacienty je typické, že nemoc u nich probíhá delší dobu (> 5 let) a i když zvýšené hodnoty Tei indexu nesouvisí s aktivitou nemoci a korelují s postižením vnitřních orgánů, specificky plic. Takto zvýšené hodnoty Tei indexu jsou tedy typické pro podskupinu č. II z tabulky 4, a to hlavně pro ty nemocné, u kterých déle trvající choroba je sice tlumena v aktivitě, ale má postižení plic s intersticiální plicní fibrózou. Rovněž zvýšené hodnoty Pg max na trikuspidální regurgitaci (nikoli ale průkazně patologické) souvisejí s plicní manifestací SLE a s vyšší aktivitou SLE (SLEDAI index > 5).
Table 7. Potenciální rizikové faktory SLE v korelaci k Pg max a Tei indexu. 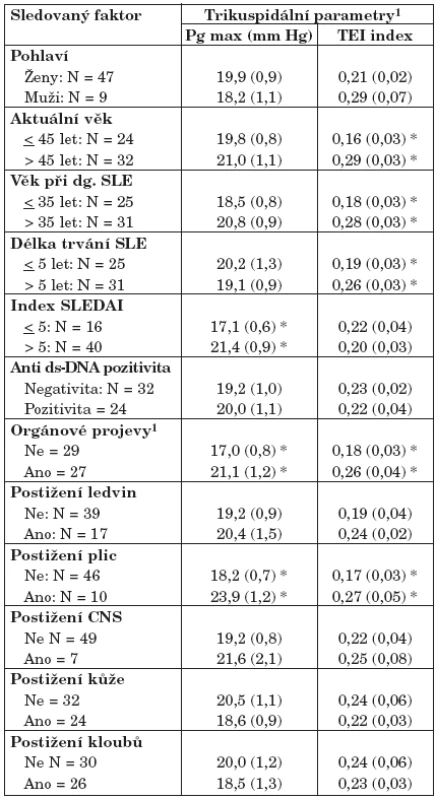
1Čísla vyjadřují průměr doplněný standardní odchylkou (v závorkách) *Označení statisticky významného rozdílu mezi uvedenými řádky (t-test; p < 0,05) Diskuse
Výskyt kardiovaskulárních projevů v našem souboru byl celkově velmi nízký. Vyskytly se pouze dva typy kardiovaskulárních patologií, a to přítomnost perikardiálního výpotku a chlopenní regurgitace. Výskyt perikardiálního výpotku v našem souboru byl výrazně nižší oproti údajům z literatury, u nás u 14 % nemocných, obecně je ale udáván od 20 % výše (1, 2). Výskyt chlopenních vad, zejména regurgitací, odpovídá výskytu v běžné populaci. Vůbec jsme nezjistili případy plicní hypertenze, která je udávána v průměru u 4–14 % nemocných se SLE (4, 8). Závislost nalezených kardiovaskulárních patologií na vzrůstajícím věku u sledovaných nemocných se SLE může souviset i s jejich přirozeným nárůstem u starších osob obecně. Vyšší výskyt kardiovaskulární manifestace u nemocných s aktivním SLE a s přítomností orgánových projevů, který jsme u našich nemocných zjistili, je pro SLE typický (1, 2), na druhé straně je ale udávána i závislost na délce trvání nemoci, což jsme v našem souboru prokázali jen částečně (15). V případě přítomnosti plicní manifestace SLE (zejména intersticiální plicní fibrózy) a u více aktivního onemocnění (SLEDAI index > 5) jsou patrny vyšší hodnoty vrcholového gradientu trikuspidální regurgitace, které mohou signalizovat riziko rozvoje plicní hypertenze. Patologické hodnoty však v našem souboru nalezeny nebyly (8, 16). Vysvětlením může být relativně malý počet probandů.
Závěr
SLE v různém stupni pokročilosti a závažnosti se manifestuje řadou kardiovaskulárních komplikací. V našem souboru jsme prokázali zejména výskyt chlopenních regurgitací a přítomnost perikardiálního výpotku. Tyto nálezy se kumulují u pacientů s přítomností orgánových projevů (bez ohledu na aktuální aktivitu SLE) a u agresivnějšího průběhu aktivní choroby (zde se zvýšeným indexem SLEDAI), a to bez ohledu na dobu trvání choroby. Všechny tyto nálezy souvisejí s přítomností orgánové manifestace, specificky nejvíce s postižením plic, resp. přítomností intersticiální plicní fibrózy. U starších pacientů s plicním postižením s dlouho trvajícím SLE byly zjištěny významně zvýšené hodnoty Tei indexu. Jsou-li u aktivní choroby SLE s indexem SLEDAI > 5 postiženy plíce, pozorujeme signifikantně vyšší gradient na trikuspidální chlopni. Tento nález může být perspektivně rizikový pro rozvoj plicní hypertenze. U ostatních echokardiografických parametrů nebyly v této analýze zjištěny žádné korelace ani vztahy k intenzitě a závažnosti SLE a nebyla zjištěna ani souvislost s absolvovanou imunosupresivní léčbou základního onemocnění.
Naše sledování mimo jiné upozorňuje na nutnost pečlivého sledování, které by mělo být zaměřeno nejen na obvyklé a častější projevy SLE, ale i na možné kardiovaskulární komplikace. Toto sledování by mimo běžné klinické vyšetření mělo obsahovat zejména cílenou anamnézu zaměřenou na obtíže, které by mohly být prvou známkou postižení srdce, jako je dušnost, palpitace, nevýkonnost, oprese na hrudi apod. Zejména je ale nutno zdůraznit význam preventivně a pravidelně prováděné echokardiografie, která nenáročnou, neinvazivní cestou přispívá k časné detekci možných kardiálních komplikací SLE, jež se vyvíjejí zpravidla pomalu, dlouho skrytě a v době klinické manifestace bývají často již pokročilé a tedy i hůře terapeuticky ovlivnitelné. Na základě našich pozorování se domníváme, že nemocní se SLE s intersticiální plicní fibrózou a s indexem SLEDAI > 5 by měli být pečlivě echokardiograficky sledováni, optimálně zřejmě každý rok i v nepřítomnosti symptomů podezřelých z plicní hypertenze.
MUDr. Dana Tegzová
Revmatologický ústav
Na Slupi 4
128 50 Praha 2
e-mail: tegz@revma.cz
Podporováno grantem IGA MZ ČR NR /7886-3
Sources
1. Dostál C, Vencovský J. Postižení srdce a cév, 93–93. Systémový lupus erythematodes, Medprint, 1997.
2. Gordon C. Long-term complications of systemic lupus erythematosus. Rheumatology 2002; 41 : 1095–1100.
3. Schattner A, Liang MH. The cardiovascular burden of lupus. Arch Intern Med 2003, 163(13): 1507–1510.
4. Petri M, Spence D, Bone RI, et al. Coronary artery disease risk factors in the John Hopkins lupus cohort Prevalence, recognition by patients and prevention practices. Medicina (Baltimore)1992; 71 : 91–302.
5. Urowitz MB, Gladman DD. How to improve morbidity and mortality in systemic lupus erythematosus. Rheumatology 2000; 39 : 238–244.
6. Manger K, Manger B, Repp R, et al. Definition of risk factors for death, and stage renal disease, and thromboembolic events in a monocentric cohort of 338 patients with systemic lupus erythematosus. Ann Rheum Dis 2002, 61 : 1065–1070.
7. Svenungsson E, Sensen-Urstad K, Heimbuerger M, et al. Risk factors for cardiovascular disease in systemic lupus erythematosus. Circulation 2001; 104 : 1887–1893.
8. Gaine SP. Pulmonary hypertension. JAMA 2000; 284 : 3160–3168.
9. Manzi S. Systemic lupus erythematosus: a model for atherogenesis? Rheumatology 2000; 39 : 353–359.
10. Selzer F, Sutton-Tyrrell K, Fitzgerald S, et al. Vascular stiffness in women with systemic lupus erythematosus. Hypertension 2001; 37 : 1075–1082.
11. Nuttall SL, Heaton S, Piper MK, et al. Cardiovascular risk in systemic lupus erythematosus – evidence of increased oxidative stress and dyslipidaemia. Rheumatology 2003; 42 : 758–762.
12. Nowak J, Nilsson T, Sylvén C, et al. Potential of carotid ultrasonography in the diagnosis of coronary artery disease. Stroke 1998; 29 : 439–446.
13. Altman DG. Practical Statistics for Medical Research. London: Chapman and Hall, 619p, 1991.
14. Zar JH. Biostatistical Methods. 2nd ed. London: Prentice Hall, 556p, 1984.
15. Cervera R, Font J, Peare C, et al. Cardiac disease in SLE. Prospective study od 70 pts. Ann Rheum 1991, 51“156–9.
16. Sturfelt G, Eskillson J, Nived O. Cardiovascular disease in SLE. A study of 75 pts from a defined population. Medicine (Baltimore), 1992 : 216–23.
Labels
Dermatology & STDs Paediatric rheumatology Rheumatology
Article was published inCzech Rheumatology

2007 Issue 2-
All articles in this issue
- Stanovení pentosidinu v moči a tkáních kloubního kompartmentu pacientů s pokročilou osteoartrózou
- Výskyt echokardiograficky detekovatelných kardiovaskulárních manifestací systémového lupus erythematodes
- Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Účinnost a strategie léčby
- Monitorování léčby osteoporózy
- Zobrazovací metody v hodnocení strukturální progrese u ankylozující spondylitidy
- Bezpečnost podání anti-TNF alfa léčby u revmatických pacientů s chronickou hepatitidou B nebo C
- Osteonekróza asociovaná se systémovou kortikoterapií
- Trombotická trombocytopenická purpura u nemocných se systémovým lupus erythematodes
- Czech Rheumatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Osteonekróza asociovaná se systémovou kortikoterapií
- Trombotická trombocytopenická purpura u nemocných se systémovým lupus erythematodes
- Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Účinnost a strategie léčby
- Zobrazovací metody v hodnocení strukturální progrese u ankylozující spondylitidy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

