-
Medical journals
- Career
Fertilitu zachovávající terapie gynekologických malignit
: Luboš Minář
: Gynekologicko-porodnická klinika LF MU a FN Brno, přednosta prof. MUDr. P. Ventruba, DrSc.
: Ceska Gynekol 2009; 74(6): 420-427
Cíl studie:
Informační přehled o konzervativní léčbě gynekologických malignit umožňující zachování reprodukčních funkcí.Typ studie:
Literární přehled s kazuistikou.Název a sídlo pracoviště:
Gynekologicko-porodnická klinika LF MU a FN Brno.Metodika:
Literární přehled o konzervativní léčbě gynekologických malignit umožňující zachování reprodukčních funkcí s ilustrativní kazuistikou.Závěr:
Podle údajů Národního onkologického registru představují z hlediska incidence gynekologických malignit určitou, početně ne zcela nevýznamnou skupinu, malignity vyskytující se u žen fertilního věku. Jedná se o značně citlivou oblast onkogynekologie, kde je žádoucí vysoce individualizovaný přístup, který vychází ze stadia onemocnění a současně reflektuje event. přání pacientky na zachování budoucí fertility. Zásadní je záchyt onemocnění v časných stadiích, který umožní fertilitu zachovávající konzervativní postup. Před zahájením konzervativní léčby je nutné provést obligatorní stagingová vyšetření, kdy je z pohledu onkogynekologa zásadní zejména expertní gynekologický ultrazvuk pánve a dutiny břišní, který se při adekvátní erudici vyšetřujícího jeví jako metoda s dostatečnou diagnostickou přesností vyjádřenou parametry senzitivity a specifity a současně i jako diagnostická metoda vysoce efektivní z hlediska ekonomického. Velice důležitou součástí týmu, který se podílí na realizaci této specializované péče v oblasti onkogynekologie je rovněž histopatolog specializující se na onkogynekologickou problematiku a jedním z důležitých předpokladů je rovněž možnost pracoviště provádět peroperační histopatologická vyšetření.Klíčová slova:
fertilita, gynekologické maligní tumory, hormonální terapie, chirurgická terapie, trachelektomie, expertní ultrasonografie.ÚVOD
Podle údajů Národního onkologického registru (NOR) byla v České republice v roce 2005 incidence karcinomu děložního hrdla 19,1. V absolutních číslech to znamená 1003 nových případů onemocnění, z toho jich bylo ve věkové kategorii do 35 let 151, od 35 do 40 let pak dalších 102 nových případů. U karcinomu endometria byla incidence 33,2, což je 1739 nových případů onemocnění. Karcinom děložního těla je však u žen ve fertilním věku spíše raritní záležitostí, ve věku do 35 let byly v roce 2005 hlášeny pouze 3 nové případy, ve věkové katerogii 35-40 let pak dalších 9 nových případů. U karcinomu ovaria byla incidence 21,4, což znamená 1129 nových případů onemocnění. Ve věkové kategorii do 35 let onemocnělo karcinomem ovaria 46 žen, ve věkovém rozmezí 35-40 let pak bylo postiženo touto diagnózou dalších 18 žen [18]. Vzhledem k výše uvedeným statistickým údajům, jednoznačnému trendu v plánovaném rodičovství kopírujícím západní civilizaci s posunem snahy o graviditu až k 3. decenniu, kdy narůstá incidence gynekologických malignit a současně i vzhledem k narůstajícímu počtu párů, které jsou odkázány ve snaze o úspěšnou graviditu na techniky asistované reprodukce (léčená sterilita je např. prokázaným rizikovým faktorem pro borderline ovariální tumory), je a zůstane problematika fertilitu zachovávající terapie gynekologických prekanceróz a malignit vysoce aktuální záležitostí.
KARCINOM ENDOMETRIA
Diagnóza karcinomu endometria v reprodukčním věku je velmi vzácná. Pacientky, u nichž je onemocnění diagnostikováno ve fertilním věku, většinou vykazují typické rizikové faktory pro vznik onemocnění I. typu. Typ I. je hormonálně dependentní, má vztah k absolutnímu nebo relativnímu hyperestrinismu, vzniká na terénu hyperplastického endometria a je spojen s klasickými rizikovými faktory. Jedním z nich je obezita, kdy riziko je závislé i na výši nadváhy. Obezita souvisí s vyšší koncentrací estrogenů, které vznikají aromatizací především z androgenů, na čemž se významně podílí právě tuková tkáň, navíc u obézních žen je redukována kapacita transportních globulinů, což způsobuje zvýšení hladin cirkulujících volných hormonů. Dalším rizikovým faktorem je diabetes mellitus, zejména I. typu, kde se udává relativní riziko stejné jako u obezity v rozmezí 2-4. Poruchy glycidového metabolismu jsou zjišťovány u asi 40 % pacientek s karcinomem endometria. Jak již bylo uvedeno výše, známým rizikovým faktorem karcinomu endometria jsou ovariální poruchy spojené se stavy hyperestrinismu. Tyto pacientky mají v anamnéze často sterilitu, která souvisí s poruchami cyklu, jako jsou anovulace či luteální insuficience, např. u syndromu polycystických ovarií je udáváno relativní riziko karcinomu endometria asi 3 [17]. Všechny nálezy karcinomu děložního těla v reprodukčním věku by měly být revidovány patologem specializujícím se na onkogynekologickou problematiku, neboť v mnoha případech může být diagnóza zaměněna s nálezem atypické hyperplazie endometria. Naprostá většina těchto malignit (asi 95 %) je typu I. a jsou zde velmi často přechody právě z atypické hyperplazie v dobře diferencovaný karcinom.
Pokud je histolopatologem potvrzen dobře diferencovaný endometroidní adenokarcinom omezený pouze na endometrium, je možno na základě přání pacientky zvolit konzervativní léčebný postup [2]. Stejný postup se týká i nálezu atypické hyperplazie endometria. Ve všech ostatních případech je jednoznačně indikována primární (definitivní) chirurgická léčba [27]. Před zahájením konzervativní léčby je nutné provést obligatorní stagingová vyšetření, kdy je zásadní zejména expertní gynekologický ultrazvuk pánve a dutiny břišní, který posuzuje jednak lokální rozsah nádoru, jednak i parenchymatózní orgány dutiny břišní (játra, ledviny) či uzliny v retroperitoneu. Při vaginálním pohledu hodnotíme integritu endomyometriální junkce a vylučujeme event. přítomnost invaze myometria (při vyšetření erudovaným ultrasonografistou je udávána specifita 80 %, která je srovnatelná s přesností peroperačního stanovení infiltrace myometria pomocí freez histologie) [7]. Další upřesnění suspektních nálezů je pak možné pomocí vyšetření selektivních. V literatuře je některými autory uváděna možnost využití nukleární magnetické rezonance (NMR) jako fakultativní vyšetřovací metody k vyloučení myometriální invaze právě před zahájením fertilitu šetřící léčby (dynamické NMR s kontrastem má podle některých literárních údajů přesnost 85-95 % v predikci myometriální invaze) [6].
Fertilitu zachovávající postup je založen na hormonální terapii vysokými dávkami gestagenů. Nejčastěji užívaným preparátem je medroxyprogesteron acetát v dávce 200-600 mg/den, event. megestrol acetát v dávce 160 320 mg/den. Medikamentózní terapie je indikována v kontinuálním režimu po dobu 3-6 měsíců s následným kontrolním vyšetřením a odběrem kontrolní biopsie. Ta se realizuje cíleně pod hysteroskopickou kontrolou s následnou kompletní kyretáží. V případě nálezu atypické hyperplazie endometria je postup identický, použijeme však redukovanou dávku hormonální terapie, většinou medroxyprogesteron acetát 100-200 mg/den rovněž v kontinuálním režimu [20]. Při negativním nálezu se doporučuje indukce ovulačních cyklů, event. ihned zařazení do programu asistované reprodukce.
KARCINOM DĚLOŽNÍHO HRDLA
Z hlediska incidence je u žen fertilního věku na prvním místě mezi gynekologickými malignitami karcinom děložního hrdla. Každý rok je diagnostikováno asi 150 nových případů v ženské populaci do 35 let, z toho se ve více než 60 % jedná o stadia splňující podmínky pro fertilitu zachovávající chirurgii. Jejím obecným principem je zachování děložního těla, adnex a alespoň části děložního hrdla. Rozsah výkonu závisí na stadiu onemocnění [22]. Vzhledem k diferenciaci léčby karcinomu děložního hrdla, kdy důležitou skupinu indikovaných operačních výkonů představují fertilitu zachovávající operace, je zcela zásadní přesný předoperační staging.
Většina onkogynekologických center využívá k zpřesnění stagingu nukleární magnetickou rezonanci (NMR), což je přesná metoda k určení stadia onemocnění, včetně zhodnocení regionálních lymfatických uzlin [31]. Limity této metody na druhou stranu představují cena vyšetření i erudice radiodiagnostika. Podle posledních publikovaných studií týkajících se stagingu časných stadií karcinomu děložního hrdla je rovněž vysoce spolehlivou metodou, současně snadno dostupnou a levnou ve srovnání s NMR, transrektální ultrazvukové vyšetření, které však vyžaduje vysoce erudovaného expertního ultrasonografistu v onkogynekologické problematice. Přítomnost a rozsah nádoru děložního hrdla lze stanovit na základě změny echogenity nádorové tkáně. Ta je hypoechogenní asi v 60 % případů, ve zbylých případech je izoechogenní s cervikálním stromatem nebo hyperechogenní, což se týká histologického typu adenokarcinomu. Obtížné je tedy hodnocení izoechogenních nádorů, kdy se jejich rozsah upřesňuje pomocí dopplerovského vyšetření s ozřejmením přítomnosti a uložení intratumorózních cév [7, 8]. Z hlediska rozsahu operačního výkonu nejjednodušší řešení umožňuje stadium IA1 bez přítomné angioinvaze, kdy je dostačujícím výkonem konizace. Ve stadiu IA1 s angioinvazí a IA2 je indikována pánevní lymfadenektomie, vč. biopsie sentinelové lymfatické uzliny a prostá vaginální trachelektomie (konizace), ve stadiu IB1 pak pánevní lymfadenektomie, vč. biopsie sentinelové lymfatické uzliny s radikální trachelektomií, kdy je cílem dosáhnout standardního rozsahu výkonu na parametriích a poševní manžetě jako u hysterektomie II. stupně radikality [23, 25]. V předoperačním stagingu u stadia IB1 má zásadní úlohu vyšetření magnetickou rezonancí nebo expertním ultrazvukovým transrektálním vyšetřením k upřesnění rozsahu tumoru (léze v největším rozměru nesmí přesahovat 2 cm) a ke stanovení kraniálního dosahu nádoru.
O rozvoj konzervativního chirurgického řešení časných stadií karcinomu děložního hrdla u žen fertilního věku se zasloužil především Dargent, který zpočátku prováděl laparoskopickou pánevní lymfadenektomii následovanou radikální vaginální trachelektomií [5], první soubor abdominálně operovaných pacientek referoval Ungár [3].
Z hlediska operačního přístupu je v praxi nejužívanější variantou od stadia IA1 s angioinvazí výše kombinace laparoskopické pánevní lymfadenektomie, vč. biopsie sentinelové uzliny s trachelektomií provedenou vaginálně nebo kombinovanou laparoskopicko-vaginální technikou s různým rozsahem výkonu jednotlivými přístupy podle erudice operatéra a zvyklosti centra. Laparoskopický přístup je s výhodou využíván kromě provedení pánevní lymfadenektomie k disekci ureterů, močového měchýře, resekci uterinních cév, postranního a zadního parametria, ve vaginální části se pak zpravidla provádí kolpotomie, oddělení děložního hrdla a závěrečná sutura pochvy a děložního těla [21].
Kombinace těchto dvou přístupů se jeví pro pacientku jako nejpříznivější zejména pro miniinvazivitu s redukcí rizika adhezivního procesu v dutině břišní za předpokladu adekvátní erudice onkogynekologického operatéra.
Zásadní pro fertilitu zachovávající výkon je dodržení kritérií dostatečného výkonu. Je to negativita pánevních lymfatických uzlin, kdy vzhledem k nemožnosti peroperačního zpracování celého materiálu z pánevní lymfadenektomie má velký význam biopsie a freez histologie sentinelové uzliny. Detekce sentinelové lymfatické uzliny je založena na peritumorózní aplikaci kombinace vitálního barviva a radiokoloidu s následnou detekcí barvivem označené lymfatické uzliny s adekvátní radiační aktivitou. Jsou stanoveny určité predilekční lokalizace výskytu sentinelové mízní uzliny a sice před odstupem a.uterina z a. iliaca interna, podél vasa iliaca externa a v oblasti fossa obturatoria [15, 16]. V případě detekované pozitivity pánevních mízních uzlin je fertilitu zachovávající výkon kontraindikován a je nutné provedení systematické paraaortální lymfadenektomie a radikální hysterektomie v rozsahu typu III. Druhou alternativou je ukončení výkonu a následná neoperační léčba kurativní konkomitantní chemoradioterapií. V případě, že pracoviště nemá možnost provedení peroperační histologie sentinelové uzliny, je možné event. provedení výkonu ve dvou sezeních, kdy výkon na děložním hrdle je indikován při negativitě pánevních lymfatických uzlin dle definitivní histologie. Dalším zásadním kritériem je dostatečná vzdálenost nádoru od kraniálního řezu na děložním hrdle. Ta by měla být alespoň 10 mm, podle některých autorů postačuje 5 mm, při zachování 5 mm délky reziduálního cervikálního kanálu. Při nedodržení podmínky je nutná radikalizace výkonu. Optimální je rovněž provedení peroperačního vyšetření kraniálního okraje hrdla po oddělení od děložního těla, někteří autoři považují za rozhodující adekvátní předoperační staging. Dalšími podmínkami jsou odpovídající resekce poševní manžety a parametrií [1, 24]. Na druhou stranu přibývá studií, které signalizují minimální riziko postižení parametrií u nádorů s nízkým rizikem při intaktních lymfatických uzlinách. Diskutuje se tedy o kritériích pro event. snížení radikality výkonů nejen v rámci fertility zachovávající chirurgie [4]. Po provedené radikální trachelektomii se na začátku následné gravidity doporučuje založení cerclage a gravidita se ukončuje primárním císařským řezem, počet otěhotnění po tomto výkonu se uvádí v 30-35 % případů.
KARCINOM OVARIA
U karcinomu ovaria se podle posledních údajů NOR setkáváme s mírným poklesem incidence, tento trend lze předpokládat i v dalším období, kdy by se měl začít projevovat efekt plošnějšího užívání hormonální kontracepce od devadesátých let minulého století. Na druhou stranu riziko představuje nárůst procenta neplodných párů v populaci, kdy sterilita léčená indukcí ovulace nebo přímo v kontrolovaných IVF cyklech stimulací gonadotropiny je prokázaným rizikovým faktorem pro borderline ovariální nádory [9, 10, 11]. Ovaria musí být jednoznačným středem zájmu vzhledem k limitovaným možnostem detekce časných asymptomatických stadií maligních nádorů, problémem zůstává neexistující efektivní screening těchto onemocnění s vysokým maligním potenciálem. Přihlédneme-li k základnímu histopatologickému dělení ovariálních malignit na nádory epiteliální a neepiteliální, nemá smysl, vzhledem k poměrně velmi nízkému počtu neepiteliálních malignit, o screeningu této skupiny nádorů uvažovat.
U nádorů epiteliálních není k dispozici metoda, která by splňovala kritéria screeningové metody. Tumor marker Ca 125 je produkován především serózními karcinomy a bývá zvýšen asi u 80 % pokročilých ovariálních nádorů a stanovení jeho hladiny patří mezi obligatorní stagingová vyšetření. Na druhou stranu však může být falešně negativně elevován i u celé řady dalších gynekologických i negynekologických patologií, tj. u benigních ovariálních nádorů, endometriózy, myomatózní dělohy, zánětů, u hepatopatie, autoimunitních onemocnění, rovněž tak i v těhotenství nebo při menstruaci. U mucinózních karcinomů bývá zvýšen asi v 50 % případů a je nutné doplnit odběr dalších nádorových markerů (Ca 19-9, Ca 72-4, CEA). U mladších žen s ovariální rezistencí se doporučuje vyšetření dalších typů tumor markerů k vyloučení event. neepiteliálních nádorů, tj. hCG, LDH, AFP. Žádný z uvedených tumor markerů však nelze využít v rámci screeningu.
Totéž platí i pro ultrazvukové vyšetření vzhledem k nepoměru nákladů a efektivitě screeningu. Na druhou stranu má ultrazvukové vyšetření jednoznačně vyšší specifitu a je v rukou zkušeného ultrasonografisty suverénně nejpřesnější diagnostickou metodou v diferenciální diagnostice benigních a maligních ovariálních nádorů [7]. Souhrnnou informaci o rozsahu a povaze nádoru získáme kombinací transvaginálního vyšetření (s popisem morfologie nádoru a jeho cévního zásobení) s transabdominálním vyšetřením.
Ultrazvukový nález na ovariu lze u žen ve fertilním věku rozdělit na 3 základní skupiny. Za normální nález se považuje velikost ovarií 3 x 3,5 x 4 cm, homogenní struktura tkáně s event. přítomností folikulů do průměru maximálně 30 mm. Za onkologicky nesuspektní nález podle USG kritérií se považuje rovněž nález polycystických ovarií s hyperechogenním stromatem a vícečetnými subkapsulárně uloženými folikuly průměru do 8 mm, rovněž tak za normální nález lze považovat i stav, kdy při adekvátní erudici vyšetřujícího nelze vizualizovat ovarium při jinak dobrých akustických podmínkách. Za nález suspektní považujeme velikost ovarií větší, než odpovídá normálnímu nálezu, přítomnost hladkostěnné cysty nebo větší množství volné tekutiny v Douglasově prostoru. Za nález patologický se jednoznačně považuje přítomnost nehomogenní ovariální rezistence, která má složku solidní i cystickou, typická pro cystickou složku je multilokularita s přítomností sept, nepravidelnost vnitřní výstelky cyst s papilárními prominencemi nebo nález zevních exkrescencí. Za patologii považujeme rovněž přetrvávající přítomnost volné tekutiny v Douglasově prostoru nad 3–3,5 cm, tj. nad 20 ml [29, 32].
Kromě posouzení morfologie se v diagnostice ovariálních patologií rutinně využívá hodnocení cévního toku při dopplerovském vyšetření, které významným způsobem doplní informaci o biologickém chování nádoru. Sledují se kvantitativní i kvalitativní kritéria vyšetření. Mezi kvantitativní charakteristiky patří index rezistence, pulsatilní index, nově se hodnotí i další kvantitativní markery, např. vrchol systolické rychlosti nebo průměrný čas k dosažení maximální rychlosti. Důležité jsou rovněž markery kvalitativní, které zahrnují uspořádání novotvořených cév centrálně v solidní složce nádoru, v papilárních prominencích a septech a střední až vysokou hustotu cévní sítě. Udává se, že kombinací morfologických a dopplerovských kritérií dosahuje expertní ultrasonografické vyšetření senzitivity až 95 % a specifity asi 90% v diferenciální diagnostice benigních a maligních ovariálních lézí. Mělo by se tedy jednat o postup, který by měl snižovat počet neindikovaných chirurgických intervencí a současně zvyšovat časnou detekci ovariálních malignit [30, 32].
Co nejpřesnější předoperační diagnóza umožňuje adekvátně informovat pacientku před výkonem o možných variantách řešení patologického nálezu a naplánovat optimální chirurgický výkon, jehož nezbytnou součástí je peroperační vyšetření nádoru patologem erudovaným v onkogynekologické problematice. Předoperační ultrazvuková informace o suspektním nádoru snižuje riziko peroperační perforace pouzdra nádoru [19] a pečlivé předoperační zhodnocení kontralaterálního ovaria umožňuje provedení fertilitu zachovávajícího, ale současně adekvátně radikálního stagingového chirurgického výkonu [28].
Principem fertilitu zachovávajícího výkonu je ponechání dělohy a alespoň části jednoho ovaria, fertilita je zachována rovněž i po bilaterální adnexektomii, ale tato žena je již odkázána na techniky asistované reprodukce s využitím programu dárcovství ovocytů. Konzervativní výkon je možné provádět jen při splnění přísných indikačních kritérií. Zachování jednoho vaječníku je možné, pokud se jedná o stadium IA s intaktním pouzdrem ovaria a bez přítomnosti maligního ascitu a současně se jedná o příznivý histologický typ nádoru (tj. varianta serózní, mucinózní nebo endometroidní) a příznivý grading nádoru, tj. dobře nebo maximálně středně diferencovaný. Pokud makroskopický pohled potvrdí nesuspektní předoperační ultrazvukový nález na kontralaterálním ovariu, pak není biopsie druhostranného ovaria indikována. V případě stadia IB s postižením obou ovarií pak ponecháváme na žádost pacientky pouze dělohu, stejně jako v předchozím případě není nutnost adjuvantní chemoterapie. V případě, že se jedná o nepříznivý grading (tj. špatně diferencovaný nádor) nebo iatrogenně o stadium IC, je prognóza rovněž příznivá a na základě přání pacientky je možné event. zvolit rovněž konzervativní postup, již se však nevyhneme nutnosti podat adjuvantní chemoterapii [4]. Vzhledem k výrazné gonadotoxicitě rutinně užívané kombinace taxanů s platinovým preparátem je možným postupem odběr tkáně z kontralaterálního ovaria za účelem kryoprezervace tkáně s následným získáním oocytů v rámci technik asistované reprodukce [12, 13, 14]. Námětem k diskusi je fertilitu zachovávající chirurgický výkon s následnou chemoterapií v případě stadia IC se spontánní rupturou pouzdra či pozitivitou laváže nebo přítomností maligního ascitu. Kompletní stagingový, ale zároveň fertilitu zachovávající výkon zahrnuje odběr peritoneální tekutiny nebo laváž ve standardních lokalitách, event. brániční stěry, biopsii z peritonea přední exkavace, pánevních stěn a parakolických prostor, současně i biopsii ze všech suspektních ložisek nebo adhezí v oblasti pánve a dutiny břišní, infrakolickou omentektomii, apendektomii, pánevní a paraaortální lymfadenektomii a jednostrannou nebo oboustrannou adnexektomii podle stadia onemocnění [26]. Po operaci se doporučuje snaha o co nejčasnější graviditu a po dokončení reprodukčních plánů odstranění ponechaných adnex. V případě, že žena graviditu bezprostředně neplánuje, je indikována hormonální kontracepce a důsledná dispenzární péče.
Častěji se u mladších žen setkáváme s borderline ovariálními tumory, které se vyskytují v průměru ve věkové kategorii o 10-15 let nižší než karcinomy, mají podstatně lepší prognózu a nižší riziko recidiv. Nejčastější variantou borderline tumoru u žen fertilního věku je endocervikální typ mucinózního nádoru, který má vrchol výskytu kolem 35. roku. Ve srovnání s invazivním karcinomem jsou příznivější podmínky pro zachování ovaria nebo jeho části, je možné zachovat část vaječníku i v případě oboustranného postižení za předpokladu, že jsme schopni s dostatečnou přesností identifikovat nepostiženou ovariální tkáň. Rozsah fertilitu zachovávajícího výkonu je menší než u invazivního karcinomu, kromě adekvátního výkonu na adnexech se provádí odběr peritoneální tekutiny nebo laváž ve standardních lokalitách, random biopsie, současně i exstirpace všech suspektních ložisek nebo adhezí a zvětšených lymfatických uzlin v retroperitoneu a infrakolická omentektomie, naopak systematická lymfadenektomie nepatří do standardu výkonu. Po dokončení reprodukčních plánů není jednoznačně indikováno odstranění ponechaných adnex, pacientka je však srozuměna s vyšším rizikem recidivy onemocnění. To je podle literárních údajů při zachování makroskopicky nepostižených druhostranných adnex asi 10-15 %, při resekčním výkonu na postiženém ovariu a ponechání jeho části 20-35 %. Z tohoto důvodu je racionální provádět resekční výkony pouze při bilaterálním postižení nebo při jednostranné adnexektomii v anamnéze [4].
VLASTNÍ POZOROVÁNÍ
Na našem pracovišti jsme v období leden – srpen 2009 zaznamenali 4 případy časných stadií invazivního karcinomu ovaria u žen fertilního věku (věkové rozmezí 32 36 let), které splňovaly indikační kritéria fertilitu zachovávajícího chirurgického výkonu. Ve všech případech se jednalo o stadium IA a nádory příznivého histologického typu a gradingu.
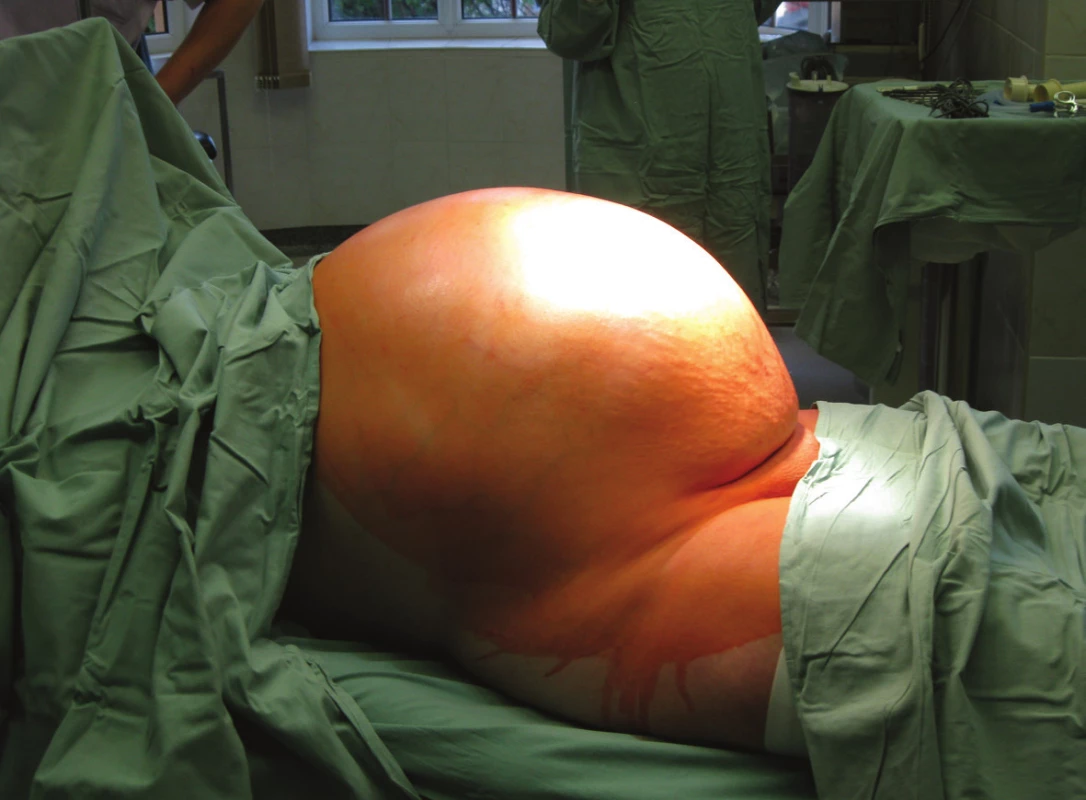
V rámci kazuistiky je prezentována 36letá pacientka, která byla na naše pracoviště referována pro nález rozsáhlé cystické rezistence pánve a dutiny břišní, pravděpodobně ovariálního orriga. Její rodinná i osobní anamnéza, včetně onkologické, byla negativní. Z hlediska gynekologické anamnézy rodila dvakrát císařským řezem, v obou případech byla indikací intrapartální hypoxie. Jinak neudávála žádné gynekologické onemocnění, hormonální antikoncepci nikdy nemedikovala. Profesí byla administrativní pracovnice. Z pohledu aktuálního objektivního nálezu udávala anamnesticky asi 18 měsíců trvající zvětšování obvodu břicha a váhový přírůstek 20 kg, což dávala do souvislosti „s rodinným výskytem obezity“. Menstruační cyklus byl celé období pravidelný, poslední 3 měsíce si stěžovala na obstipaci. Objektivní nález byl charakterizován výrazným vyklenutím břišní stěny nad niveau až k processus xyphoideus, pacientka měla v době diagnózy hmotnost 115 kg při tělesné výšce 169 cm. Při zevním pohledu nález imponoval jako donošená vícečetná gravidita u obézní ženy [obr. 1].
Při gynekologickém vyšetření vzhledem k habitu a výraznému edematóznímu prosáknutí břišní stěny nebyla jednoznačně možná diferenciace nálezu, jevila se naznačená undulace ascitu, vaginálně bylo patrné hladké děložní hrdlo a palpačně výrazné snížení kleneb poševních s nemožností palpační diferenciace dělohy.
Při vaginálním ultrasonografickém vyšetření byla patrna drobná děloha utlačená masivní cystickou rezistencí bez přítomných sept, s částečně vizualizovatelnou, nerovnou spodinou. Při abdominálním pohledu bylo viditelné v dutině břišní velké množství tekutiny zasahující do všech břišních kvadrantů. To podmiňovalo vysoké uložení jater, paraaortální oblast byla zcela nepřehledná (mimo hloubkový dosah sondy). Při okrajích tekutiny, zejména v pravém mezo - a hypogastriu, byla popisována četná, smíšeně echogenní kulovitá ložiska průměru až 60 mm, některá cystického vzhledu. Játra byla přístupná pouze interkostálně, bez jednoznačných ložisek. Oboustranně byla popisována vs. tlakově podmíněná dilatace vývodných cest močových podmiňující hydronefrózu II. stupně.
Závěr expertního ultrasonografického vyšetření nebyl zcela jednoznačný a popisoval dvě varianty nálezu. První byla objemný cystický útvar, jednokomorový, anechogenního obsahu, ale v určitém úseku s výrazně nerovnou, prominující spodinou. Parametry dopplerovského vyšetření signalizovaly zvýšené riziko malignity. Druhou popisovanou variantou byl obraz karcinomatózy peritonea se zahuštěním ascitu, v USG obraze nebylo možné jednoznačné rozlišení, protože některé oblasti se nacházely mimo hloubkový dosah sondy. Nádorové markery byly negativní, pouze hraniční hodnota Ca 125, RTG plic bez nálezu fluidothoraxu.
Pacientka byla indikována k probatorní laparotomii a po seznámení se všemi variantami potenciálních histopatologických nálezů preferovala fertilitu zachovávající operační výkon v případě nálezu malignity časného stadia.
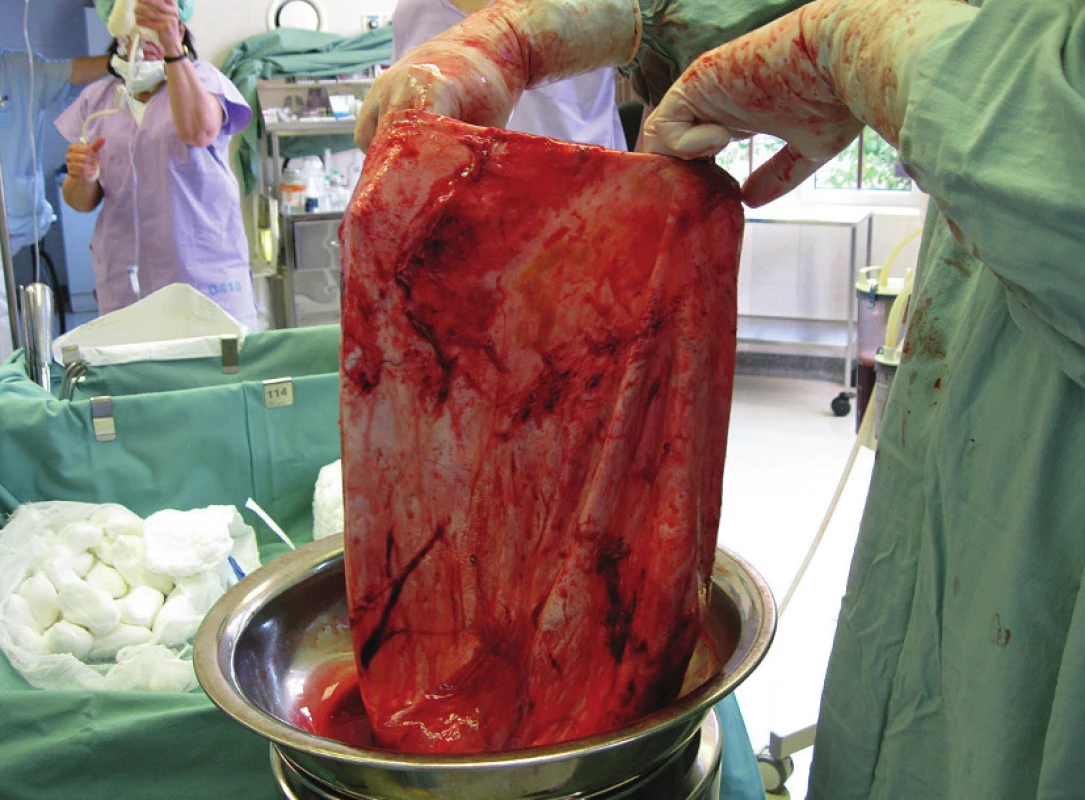
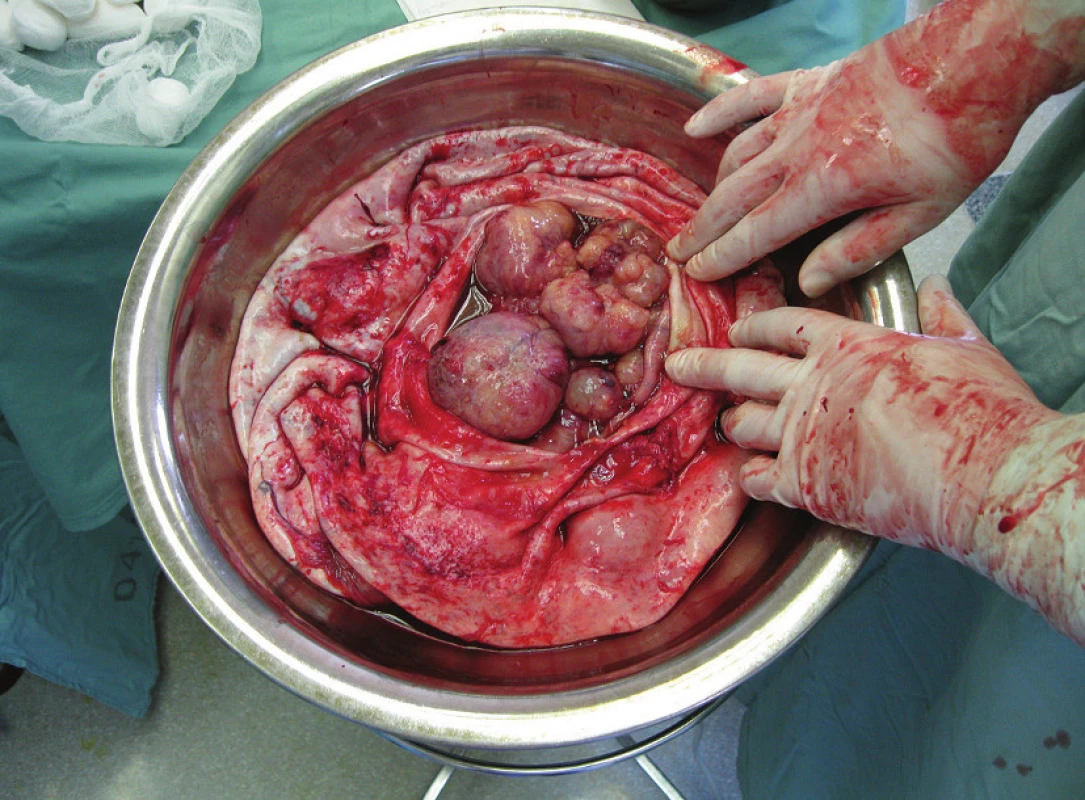
Výkon byl proveden z dolní střední laparotomie s následným prodloužením nad pupek vzhledem k peroperační detekci velkoobjemového ovariálního kystomu. Po provedení laváže se podařilo vyluxovat hladkostěnný kystom bez perforace pouzdra před břišní stěnu a po podvazu závěsného aparátu in toto oddělit. Z dutiny kystomu bylo odsáto 24 litrů zelenavě zkalené, viskózní tekutiny. Na rozdíl od zcela hladkého zevního povrchu kystomu byly na vnitřním povrchu patrné kulovité, hladce opouzdřené, objemné prominence, na řezu tvořené jemně granulární, bělavou nádorovou tkání s drobnými dutinkami s hlenovitým obsahem [obr. 2, 3]. Z peroperační histologie byl referován dobře diferencovaný mucinózní cystadenokarcinom. Po revizi pánve a dutiny břišní, kde nebyly shledány makroskopické projevy diseminace nádoru, jsme se rozhodli na základě předoperační konzultace s pacientkou pro provedení fertilitu zachovávajícího výkonu. Byly provedeny brániční stěry a biopsie ve standardních lokalitách, infrakolická omentektomie, apendektomie, pánevní a paraaortální lymfadenektomie. Kontralaterální adnexa byla makroskopicky zcela normálního vzhledu, biopsie tedy nebyla provedena a rovněž byla ponechána děloha, v rámci výkonu jsme ještě doplnili frakcionovanou kyretáž. Všechny další odebrané tkáně byly podle definitivní histologie již bez nálezu nádorových změn (včetně cytologie laváže), bylo získáno celkem 47 lymfatických uzlin (31 pánevních a 16 paraaortálních). Definitivní histologie potvrdila původní příznivý histotyp i grading nádoru, rozsah nemoci byl tedy uzavřen jako stadium IA podle FIGO. Pacientka byla po náležitém poučení převedena do pravidelné dispenzární péče (s redukcí hmotnosti o 23 kg ve srovnání s bezprostředním předoperačním obdobím).
ZÁVĚR
Podle údajů NOR představují z hlediska incidence gynekologických malignit určitou, početně ne zcela nevýznamnou skupinu, malignity vyskytující se u žen fertilního věku. Jedná se o značně citlivou oblast onkogynekologie, kde je žádoucí vysoce individualizovaný přístup, který vychází ze stadia onemocnění a současně reflektuje event. přání pacientky na zachování budoucí fertility. Zásadní je záchyt onemocnění v časných stadiích, který umožní fertilitu zachovávající konzervativní postup, pro což je nutná nejen adekvátní erudice zainteresovaného lékařského personálu v jednotlivých používaných diagnostických a terapeutických postupech, ale samozřejmě i disciplinovanost pacientek z hlediska absolvování prevence nebo vyhledání včasné odborné pomoci v případě klinických potíží.
Vzhledem k jednoznačné diferenciaci léčby gynekologických malignit, kdy určitou skupinu indikovaných operačních výkonů představují právě fertilitu zachovávající operace, je pak zcela zásadní přesný předoperační staging. V něm by z pohledu onkogynekologa mělo hrát dominující úlohu expertní ultrasonografické vyšetření, které se při adekvátní erudici vyšetřujícího jeví jako metoda s největší diagnostickou přesností vyjádřenou parametry senzitivity a specifity a současně i jako diagnostická metoda vysoce efektivní z hlediska ekonomického ve srovnání s dalšími dostupnými vyšetřovacími metodami (CT, NMR, PET).
Neméně důležitou roli pak sehrává i důsledná dispenzární péče probíhající na úrovni specializovaných ambulancí onkologynekologických center.
MUDr. Luboš Minář
Gynekologicko-porodnická klinika
LF MU a FN Brno
Obilní trh 11
625 00 Brno
e-mail: lubosminar@seznam.cz
Sources
1. Bartoš, P. Radikální trachelektomie v léčbě časného cervikálního karcinomu. Čes Gynek, 2000, 65, 437.
2. Benedet, JL., et al. FIGO staging classifications and clinical practise guidelines in the management of gynecologic cancers. FIGO Committee on Gynecologic Oncology. Int J Gynecol Obstet, 2000, 70, 207.
3. Cibula, D., et al. Abdominální radikální trachelektomie - technika a zkušenosti. Čes Gynek, 2005, 70, 117.
4. Cibula, D. Chirurgická léčba v onkogynekologii. Mod Gynek Porod, 2007, 16, 533.
5. Dargent, D., et al. Laparoscopic assesment of the sentinel lymph node in early stage of cervical cancer. Gynec Oncol, 2000, 79, 411.
6. DelMachio, A. Estimating the depth of myometrial involvement by endometrial carcinoma: efficacy of transvaginal sonography vs. MRI. Amer J Roentgenol, 1993, 160, 533.
7. Fischerová, D. Využití ultrazvuku v onkogynekologii. Mod Gynek Porod, 2007, 16, 719.
8. Fischerová, D., et al. Transrectal ultrasound and magnetic resonanc imaging in staging of aerly cervical cancer. IJGC, 2007, 17.
9. Hudeček, R., Ventruba, P., Tsompsos, J., et al. Incidence of malignancy occurance in patients treated for infertility with assisted reproduction techniques. Helen J Obstet Gynecol, 2006, 5, 79.
10. Hudeček, R., Ventruba, P., Huser, M., et al. Zhoubné novotvary ovaria v populaci infertilních pacientek České republiky - I. část. Prakt Gyn, 2006, 3, 100.
11. Hudeček, R., Ventruba, P., Huser, M., et al. Zhoubné novotvary ovaria v populaci infertilních pacientek České republiky - II. část. Prakt Gyn, 2006, 4, 136.
12. Huser, M., Juránková, E., Crha, I., et al. Kryokonzervace ovariální tkáně - šance na záchranu fertility žen s rakovinou. Čes Gynek, 2007, 72, 68.
13. Huser, M., Crha, I., Ventruba, P., et al. Prevention of ovarian function damage by a GnRH analogus during chemotherapy in Hodgkin lymphoma patiens. Hum Rep, 2008, 23, 863.
14. Huser, I. Crha, R. Hudecek, R., et al. Ovarian tissue cryopreservation – new oportunity to preserve fertility in female cancer patients. Eur J Gynaec Oncol, 2007, 28, 249.
15. Holub, Z., Kužel, D., et al. Minimálně invazivní operace v gynekologii. Praha: Grada 2005, s. 231.
16. Holub, Z. Laparoskopické operace. Mod Gynek Porod, 2006, 15, 273.
17. Homesley, HD., Zaino, R. Endometrial cancer: prognostic factors. Seminars in Oncology. 21, 71, 1994. 18. Novotvary 2005 ČR, ÚZIS ČR, NOR ČR.
19. Petrenko, M. Adnexální laparoskopická chirurgie. In: Holub, Z., Kužel, D., et al. Minimálně invazivní operace v gynekologii. Praha: Grada 2005, s. 67.
20. Pluta, M. Patogeneze a management prekanceróz endometria. Prakt Gyn, 2004, 2, 6.
21. Querleu, D., et al. Laparoscopic pelvic lymphadenectomy in the staging of early cancer of the cervix. Amer J Obstet Gynec, 1991, 164, 579.
22. Rob, L., et al. Fertilitu zachovávající operace u časného stadia karcinomu děložního hrdla dnes a zítra. Čes Gynek, 2006, 71, 302.
23. Rob, L. Současné trendy v léčbě gynekologických nádorů. Gynek po promoci, 2006, 2, 47.
24. Rob, L. (komentář): Dargent, D. Radikální trachelektomie jako metoda zachovávající fertilitu u časných stadií zhoubných nádorů hrdla děložního hrdla. Gynek po promoci, 2001, 1, 28.
25. Rob, L., Svoboda, B., Robová, H., et al. Guideline gynekologických zhoubných nádorů - Komplexní léčba operabilních stadií zhoubných nádorů děložního hrdla. Mod Gynek Porod, 2007, 16, 226.
26. Robová, H., Rob, L., Svoboda, B., et al. Guideline gynekologických zhoubných nádorů. - Komplexní léčba ovariálních epiteliálních zhoubných nádorů. Čes Gynek, 2006, 71, 237.
27. Svoboda, B., Kubecová, M., Rob, L., et al. Guideline gynekologických zhoubných nádorů - Komplexní léčba zhoubných nádorů děložního těla. Mod Gynek Porod, 2007, 16, 237.
28. Timmermann, D., et al. Ultrasound et endoscopic surgery in obstetrics and gynaecology. London: Springer 2003.
29. Timmermann, D., et al. Subjective assessment of adnexal masses with the use of ultrasonography: an analysis of interobserver variability and experience. UOG, 1999, 13, 11.
30. Valentin, L., et al. Ultrasound characteristics of different types of adnexal malignancies. UOG, 2006, 41, 102.
31. Yang, W. Transrectal ultrasound in the evaluation of cervical carcinoma and comparison with spiral computed tomography and magnetic resonance imaging. Br J Radiol, 1996, 69, 610.
32. Yazbek, J., et al. A comparative study of the risk of malignancy index and ovarian crescent sign for the diagnosis of invasive ovarian cancer. UOG, 2006, 28, 320.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2009 Issue 6-
All articles in this issue
- Comparison of reactive oxygen species production in neat semen and washed spermatozoa
- Amniotic fluid interleukin 6 levels in preterm premature rupture of membranes
- Densitometry findings in women using gestagen contraception
- Combination therapy with anticholinergics and alpha-blockers for the treatment of overactive bladder in female patients – pilot study
- Fertility preserving treatment of gynecological malignant tumors
- Molecular characterization of epithelial ovarian borderline tumors with respect to clinical management and prognosis
- Reproductive outcome after laparoscopic myomectomy – retrospective analysis 1994-2007
- Ovarian torsion in the first trimester gravidity after stimulation in vitro fertilization – case report
- Prenatal intracranial hemorrhagie – diagnosis and follow-up
- Analysis of perinatal indicators of the Olomouc region in the period 1994-2008
- Effect of cranberry extract capsules taken during the perioperative period upon the post-surgical urinary infection in gynecology
- Complications of laparoscopic and laparotomic treatment of endometrial cancer
- Treatment of recurrent ovarian cancer
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Amniotic fluid interleukin 6 levels in preterm premature rupture of membranes
- Prenatal intracranial hemorrhagie – diagnosis and follow-up
- Ovarian torsion in the first trimester gravidity after stimulation in vitro fertilization – case report
- Fertility preserving treatment of gynecological malignant tumors
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career