-
Medical journals
- Career
Léčba idiopatické choroidální neovaskulární membrány ranibizumabem – naše zkušenosti
Authors: O. Chrapek; Z. Vostrovská; I. Šínová; B. Chrapková
Authors‘ workplace: Oční klinika FN a LF UP v Olomouci, I. P. Pavlova 6, Olomouc, 779 00, Přednosta: prof. MUDr. Jiří Řehák, CSc., FEBO
Published in: Čes. a slov. Oftal., 75, 2019, No. 1, p. 25-28
Category: Original Article
doi: https://doi.org/10.31348/2019/1/3Overview
Cíl: Zhodnotit anatomický a funkční výsledek terapie ranibizumabem u pacientů, u nichž byla diagnostikována idiopatická choroidální neovaskularizace.
Soubor a metodika: Soubor tvoří 6 pacientů. Pacienti byli starší 18 a mladší 50 let. Sledovací doba trvala 12 měsíců. Fluorescenční angiografií a optickou koherenční tomografií byla u pacientů prokázána aktivní idiopatická choroidální neovaskularizace v subfoveolární lokalizaci. Za známku aktivity choroidální neovaskularizace byl při fluorescenční angiografii považován průsak barviva do zóny makulárního edému. Za známku aktivity choroidální neovaskularizace při vyšetření optickou koherenční tomografií byla považována přítomnost serózní ablace pigmentového listu sítnice a/nebo subretinální tekutina a/nebo intraretinální edém v podobě intraretinálních cyst. Na ETDRS (Early Treatment Diabetic Retinopathy Study) optotypu byl pozorován pokles zrakové ostrosti na úroveň < 85 písmen. Po úvodní aplikaci ranibizumabu byl uplatněn režim pro re nata, kdy k reaplikaci ranibizumabu bylo přistoupeno při známkách aktivity choroidální neovaskularizace při vyšetření optickou koherenční tomografií, fluorescenční angiografií a nebo při poklesu zrakové ostrosti ve spojení s aktivitou choroidální neovaskularizace na optické koherenční tomografii či fluoroangiogramu.
Výsledky: V průměru jsme u pacientů souboru pozorovali po 12 měsících léčby zisk +11 písmen ETDRS optotypu. V průměru jsme pozorovali redukci centrální makulární tloušťky o -233µm. U všech pacientů souboru byla ve 12. měsíci sledování konstatována při optické koherenční tomografii klidová submakulární jizva bez exsudace a tedy bez přítomnosti serózní ablace pigmentového listu sítnice, subretinální tekutiny a intraretinálního edému v podobě intraretinálních cyst. V průběhu 12 měsíců léčby byly každému pacientovi v průměru aplikovány 3 injekce ranibizumabu.
Závěr: V našem souboru jsme pozorovali pozitivní vliv ranibizumabu na průběh idiopatické choroidální neovaskularizace. Ranibizumab u všech pacientů souboru dosáhl regrese choroidální neovaskularizace s vymizením makulárního edému. S ústupem aktivity choroidální neovaskularizace dává ranibizumab reálnou naději na zlepšení zrakové ostrosti.
Klíčová slova:
idiopatická choroidální neovaskulární membrána – anti-VEGF léčba – ranibizumab
ÚVOD
Choroidální neovaskularizace (CNV) je formace novotvořených cév, které vyrůstají z choriokapilaris, prorážejí Bruchovu membránu, rostou pod pigmentový list sítnice a později případně až do subretinálního prostoru. U dospělých pacientů bývá v pozadí formování CNV především vlhká forma věkem podmíněné makulární degenerace (VPMD) a vysoká myopie. Ze vzácnějších příčin patří vzpomenout uveitidy, centrální serózní chorioretinopatie (CSCHR), angioidní pruhy, úrazy, nádory a makulární dystrofie. CNV může být označena rovněž jako idiopatická, pokud její vznik není možné spojit se zjevnou příčinou či klinicky prokazatelnou predispoziční abnormalitou [2,4,10,13]. Udává se, že 17 % CNV u pacientů mladších 50 let je idiopatických [3].
Důležitou roli v patogenezi CNV hraje vaskulární endoteliální růstový faktor (VEGF), jehož blokáda je současným standardem léčby. V České republice můžeme pro blokování molekul VEGF použít dva anti-VEGF preparáty: ranibizumab (Lucentis; Novartis Pharma AG, Basel, Switzerland) a aflibercept (Eylea; Bayer AG, Leverkusen, Germany). Ranibizumab v klinických studiích prokázal svou účinnost a bezpečnost v léčbě CNV spojených s vlhkou formou VPMD, patologickou myopií a CNV vznikajících bez ohledu na jejich etiologii [1,6,11,14,15,16].
V naší práci hodnotíme anatomický a funkční výsledek terapie ranibizumabem u pacientů, u nichž byla diagnostikována idiopatická CNV.
METODIKA
Soubor tvoří retrospektivně hodnocení pacienti, kteří byli léčeni ranibizumabem na Oční klinice FN a LF UP v Olomouci v letech 2012 – 2017 pro idiopatickou CNV. Pacienti byli starší 18 a mladší 50 let, fluorescenční angiografií (FAg) a optickou koherenční tomografií (OCT) byla u nich prokázána aktivní CNV v subfoveolární lokalizaci. Za známku aktivity CNV byl při FAg vyšetření považován průsak barviva do zóny makulárního edému. Za známku aktivity CNV při OCT vyšetření byla považována přítomnost serózní ablace pigmentového listu sítnice (RPE) a/nebo subretinální tekutina a/nebo intraretinální edém v podobě intraretinálních cyst. Na ETDRS (Early Treatment Diabetic Retinopathy Study) optotypu byl pozorován pokles zrakové ostrosti (ZO) na úroveň < 85 písmen (P). CNV nebyla spojena s VPMD (věk < 50 let) či patologickou myopií (refrakční vada pod -6 Dpt), nebyla prokázána polypoidální choroidální vaskulopatie ani retinální angiomatózní proliferace. U pacientů byla vyloučena aktivní diabetická retinopatie, netrpěli oční či periokulární infekcí ani nitroočním zánětem. V minulosti neprodělali laserové ošetření v oblasti makuly, nepodstoupili fotodynamickou léčbu ani pars plana vitrektomii. Pacienti měli negativní anamnézu stran CSCHR, očního úrazu, očního nádoru, makulární dystrofie a nebyly u nich diagnostikovány angioidní pruhy. V minulosti u nich nebyly intravitreálně aplikovány anti-VEGF preparáty, kortikosteroidy či depotní implantáty. Netrpěli systémovým zánětlivým či infekčním onemocněním ani jinou zjevnou příčinou či klinicky prokazatelnou predispoziční abnormalitou, které by mohly souviset se vznikem CNV.
Do souboru bylo zařazeno 6 pacientů (4 ženy a 2 muži) průměrného věku 38 let, (medián 41,5, směrodatná odchylka σ = 8,9582), kdy nejmladšímu pacientovi bylo v době zahájení léčby 23, nejstaršímu 48 let. 1x bylo léčeno oko pravé, 5x oko levé. Sledovací doba trvala 12 měsíců. U všech pacientů jsme pomocí ETDRS optotypu hodnotili nejlépe korigovanou vstupní ZO a po 12 měsících výslednou ZO. Porovnáním vstupní a výsledné zrakové ostrosti jsme hodnotili zlepšení, stabilizaci či zhoršení ZO. Zisk > 5 písmen ETDRS optotypu byl hodnocen jako zlepšení ZO, ztráta > 5 písmen ETDRS optotypu byla hodnocena jako zhoršení ZO. Změna zrakové ostrosti +/-5 P ETDRS optotypu byla hodnocena jako stabilizace ZO. Anatomické změny v makule a makulární tloušťku jsme hodnotili při zahájení terapie a po 12 měsících pomocí OCT, kdy byl použit OCT přístroj Cirrus (Zeiss, Jena), nebo Spectralis (Heidelberg). U každého pacienta byl při vstupu do léčby a po 12 měsících použit tentýž OCT přístroj, s jehož pomocí jsme při vstupu do léčby a na konci 12-ti měsíčního sledovacího období měřili centrální makulární tloušťku (CMT) a vyhodnocovali míru její změny. CMT byla definována jako průměrná retinální tloušťka kruhové zóny o průměru 1 mm kolem centra foveoly. Posledním hodnoceným parametrem byl počet intravitreálních injekcí, který byl každému jednotlivému pacientovi souboru v průběhu 12-ti měsíčního sledovacího období aplikován. Po úvodní aplikaci ranibizumabu byl uplatněn režim pro re nata (PRN), kdy k reaplikaci ranibizumabu bylo přistoupeno při známkách aktivity CNV na OCT/FAg a nebo při poklesu ZO ve spojení s aktivitou CNV na OCT/FAg.
VÝSLEDKY
U všech pacientů souboru byla diagnostikována klasická CNV, která u žádného pacienta souboru nepřekročila svou velikostí rozsah dvou ploch disku.
ZO a CMT během prvních 3 měsíců léčby, během reaplikací a na konci dvanáctiměsíčního sledovacího období vyjadřuje spolu s počty intravitreálních aplikací ranibizumabu u jednotlivých pacientů souboru. Tabulka 1.
Table 1. ZO a CMT během prvních 3 měsíců léčby, během reaplikací a na konci dvanáctiměsíčního sledovacího období vyjádřeno spolu s počty intravitreálních aplikací ranibizumabu u jednotlivých pacientů souboru 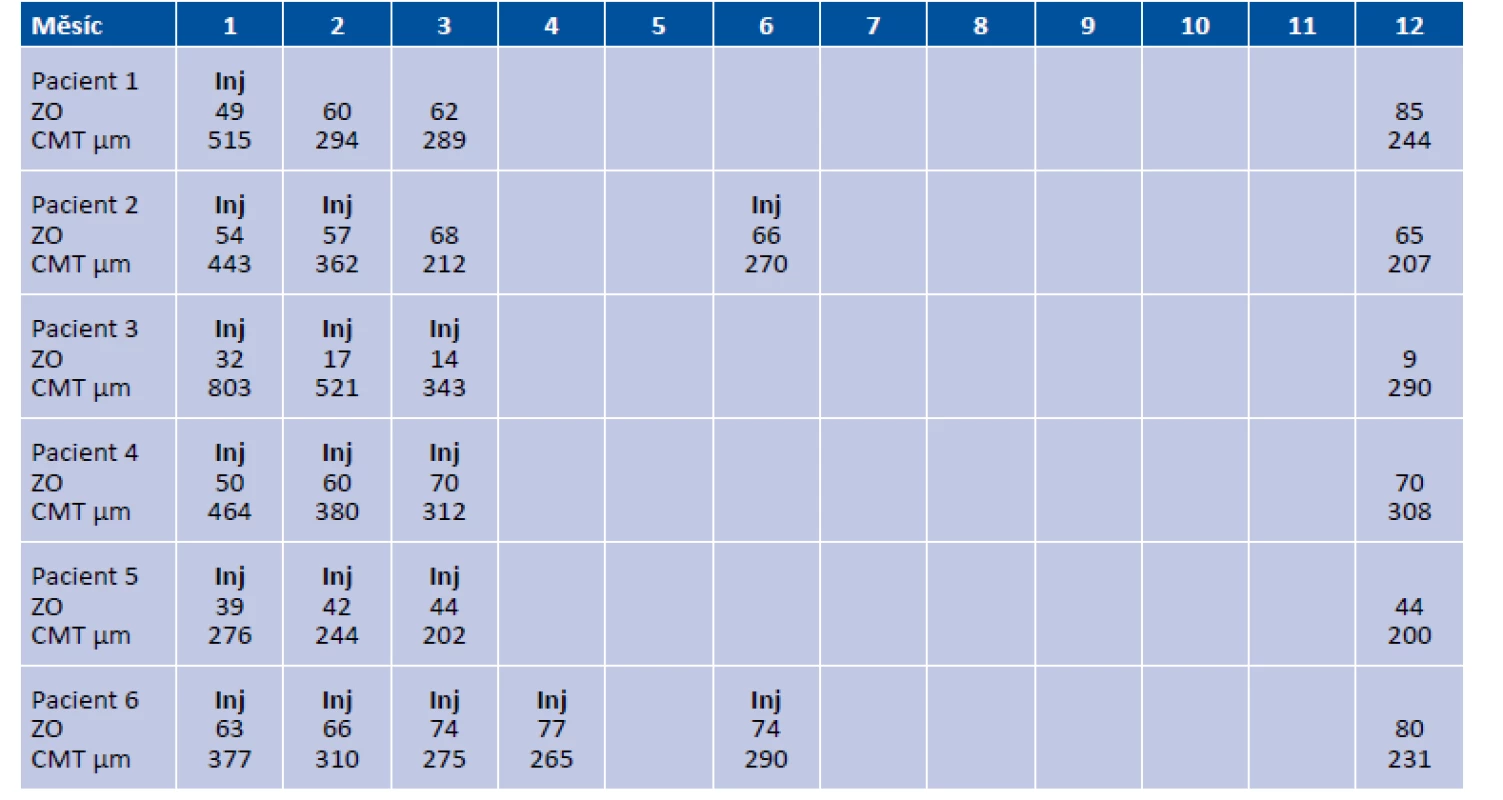
Průměrná vstupní ZO pacientů souboru byla 48 P ETDRS optotypu (medián 49P, σ = 10,0235), průměrná výsledná ZO pacientů souboru byla 59 P ETDRS optotypu (medián 67P, σ = 25,8161).
V průměru jsme u pacientů souboru pozorovali po 12 měsících léčby zisk +11 P ETDRS optotypu (medián 14P, σ = 17,9536). U 4 pacientů souboru jsme pozorovali zlepšení ZO s průměrným ziskem +21 P ETDRS optotypu (medián 18P, σ = 9,2466), u 1 pacienta stabilizaci ZO se ziskem +5 P ETDRS optotypu a u 1 pacienta zhoršení ZO se ztrátou -23 P ETDRS optotypu.
Průměrná vstupní CMT pacientů souboru byla 480 µm (medián 453,5 µm, σ = 162,9945), průměrná výsledná CMT pacientů souboru byla 247 µm (medián 237,5 µm, σ = 40,0901). CMT se u všech pacientů souboru zlepšila. V průměru jsme pozorovali redukci CMT o -233 µm (medián 196 µm, σ = 140,2379).
U všech pacientů souboru byla ve 12. měsíci sledování konstatována na OCT klidová submakulární jizva bez exsudace a tedy bez přítomnosti serózní ablace RPE, subretinální tekutiny a intraretinálního edému v podobě intraretinálních cyst.
V průběhu 12 měsíců léčby byly každému pacientovi v průměru aplikovány 3 injekce ranibizumabu (medián 3, σ = 1,1547). Jen u jednoho pacienta souboru byla aplikována jediná injekce ranibizumabu na začátku léčby. U jednoho pacienta souboru byla léčba zahájena dvěmi injekcemi ranibizumabu v odstupu jednoho měsíce a pro reaktivaci CNV po 6 měsících musela být jedna reaplikace ranibizumabu opakována. U tří pacientů souboru byla léčba zahájena třemi po sobě jdoucími injekcemi v odstupu jednoho měsíce a v průběhu celého dalšího sledovacího období nemuselo být přistoupeno k žádné reaplikaci. U jediného pacienta souboru byla léčba zahájena 4 po sobě jdoucími aplikacemi ranibizumabu a pro reaktivaci CNV na 6. měsíci sledování byla na této kontrole ještě jedna injekce ranibizumabu reaplikována. Je možné si povšimnout, že u všech pacientů souboru byly aplikace ranibizumabu provedeny v průběhu prvních 6 měsíců sledovacího období.
DISKUSE
Idiopatická CNV je onemocnění postihující osoby mladší 50 let a může zapříčinit těžkou ztrátu zraku. Přesná etiopatogeneze zůstává nejasná, uvažuje se o abnormitách v úrovni choroidey, jako je fokální choroiditida, choroidální ischémie, abnormity choroidálních cév, narušená funkční aktivita cirkulujících hematopoetických kmenových buněk [3,7,9,12].
Houfa na souboru 39 idiopatických CNV potvrdil přínos ranibizumabu pro zrakovou ostrost léčených očí. Na vstupu do léčby a na 12. měsíci sledování byla průměrná nejlépe korigovaná ZO 0.67 ± 0.45 logaritmu minimálního úhlu rozlišení (logMAR) a 0.16 ± 0.21 logMAR, kdy tento rozdíl byl hodnocen jako statisticky signifikantní (P < 0.001) [7].
V klinické studii MINERVA, hodnotící účinnost a bezpečnost ranibizumabu u CNV vznikajících bez ohledu na jejich etiologii, ale nesouvisejících s vlhkou formou VPMD a patologickou myopií, byl prokázán statisticky signifikantně lepší efekt ranibizumabu oproti placebu. Pacienti léčení ranibizumabem měli již na 2. měsíci léčby průměrný zisk +9,5 P ETDRS optotypu oproti pacientům na placebo terapii, kteří v průměru ztráceli -0,4 P ETDRS optotypu. Právě idiopatické CNV byly jednou z etiologických CNV skupin, u nichž činil rozdíl v zisku písmen na 2. měsíci léčby mezi skupinou léčenou ranibizumabem a placebem > 10 P ETDRS optotypu. Na 12. měsíci pak byl u pacientů léčených ve studii MINERVA ranibizumabem zaznamenán průměrný zisk +11 P ETDRS optotypu [11].
I v našem malém souboru jsme sledovali pozitivní vliv ranibizumabu na ZO léčených pacientů, kdy pacienti souboru získali v průměru po 12 měsících terapie +11 P ETDRS optotypu.
V referovaných souborech je spolu s pozitivním vlivem ranibizumabu na ZO zmiňován i pozitivní dopad léčby na CMT. Houfa prokázal redukci makulární tloušťky na souboru 39 pacientů s idiopatickou CNV, kdy vstupní průměrná makulární tloušťka 354,05 ± 86,52 μm byla po 12 měsících léčby redukována na hodnotu 219,15 ± 19,11 μm a tato změna byla hodnocena jako statisticky signifikantní (P < 0,001) [7]. V klinické studii MINERVA pacienti léčení ranibizumabem měli na vstupu průměrnou CMT 392,5µm (SD 145,20), po 12 měsících terapie ranibizumabem došlo ke snížení CMT v průměru o 102,7 µm [11].
I my jsme na našem souboru pozorovali u všech pacientů redukci CMT v průměru o -233 µm. U všech pacientů po 12 měsících vymizely známky aktivity CNV s ústupem intraretinálního edému, subretinální tekutiny a serózní ablace RPE. Nicméně jen u 4 pacientů (66 %) byl tento anatomický úspěch provázen funkčním zlepšením a vzestupem ZO. U jednoho pacienta se přes anatomický úspěch léčby ZO nezměnila a u jednoho pacienta dokonce zhoršila. Příčinu vidíme v kombinaci atrofických a degenerativních změn makuly po proběhlém onemocnění s fibrotickou přestavbou původně aktivní CNV s pravděpodobným poškozením fotoreceptorů foveoly při původně subfoveolární lokalizaci CNV.
Klinické studie hodnotící efektivitu a bezpečnost ranibizumabu v léčbě CNV zapříčiněných vlhkou formou VPMD udávají poměrně vysokou potřebu reaplikací pro dosažení terapeutického efektu. Ve studii PrONTO, v níž byli pacienti s vlhkou formou VPMD léčeni v PRN režimu, byl průměrný počet injekcí ranibizumabu 5,6 za prvních 12 měsíců léčby [5].
Houfa při 12 měsíců trvající léčbě 39 pacientů s idiopatickou CNV potřeboval k dosažení terapeutického efektu v průměru 2,1 ± 1,1 injekcí [7]. Chuangfeng Fan aplikoval ranibizumab u 44 pacientů s idiopatickou CNV. Za 12 měsíců léčby potřeboval u pacientů, u nichž byla doba trvání obtíží kratší než 3 měsíce, v průměru 1,22 ± 1,01 injekce, u pacientů s dobou obtíží 3–6 měsíců pak 2,53 ± 1,76 injekcí [8]. V našem souboru jsme za 12 měsíců léčby aplikovali v průměru 3 injekce ranibizumabu s velmi dobrým anatomickým i funkčním efektem.
ZÁVĚR
V našem souboru jsme pozorovali pozitivní vliv ranibizumabu na průběh idiopatické CNV. Ranibizumab u všech pacientů souboru dosáhl regrese CNV s vymizením makulárního edému. S ústupem aktivity CNV dává ranibizumab reálnou naději na zlepšení ZO. Z naší zkušenosti i zkušenosti jiných autorů [7,8] se jeví, že idiopatická CNV reaguje na ranibizumab lépe než CNV u pacientů s vlhkou formou VPMD a k dosažení terapeutického efektu je zapotřebí nižšího počtu reaplikací ranibizumabu. K ověření tohoto faktu však bude zapotřebí větší prospektivní studie.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou.
doc. MUDr. Oldřich Chrapek, Ph.D.
Oční klinika FN a LF UP v Olomouci, I.P. Pavlova 6, Olomouc, 779 00
Do redakce doručeno dne: 30. 7. 2018
Do tisku přijato dne: 3. 1. 2019
Sources
1. Brown, D.M., Michels, M., Kaiser, P.K. et al.: Ranibizumab versus verteporfin photodynamic therapy for neovascular age-related macular degeneration: two-year results of the ANCHOR study. Ophthalmology, 116, 2009; 1 : 57–65.e5.
2. Carneiro, A.M., Silva, R.M., Veludo, M.J. et al.: Ranibizumab treatment for choroidal neovascularization from causes other than age-related macular degeneration and pathological myopia. Ophthalmologica, 225, 2011; 2 : 81–88.
3. Cohen, S.Y., Laroche, A., Leguen, Y. et al.: Etiology of choroidal neovascularization in young patients. Ophthalmology, 103,1996; 8 : 1241-1244.
4. Derosa, J.T., Yannuzzi, L.A., Marmor, M. et al.: Risk factors for choroidal neovascularization in young patients: a case-control study. Doc Ophthalmol, 91,1995; 3 : 207–222.
5. Fung, A.E., Lalwani, G.A., Rosenfeld, P.J. et al.: An Optical Coherence Tomography-Guided, Variable Dosing Regimen with Intravitreal Ranibizumab (Lucentis) for Neovascular Age-related Macular Degeneration. Am J Ophthalmol, 143, 2007; 4 : 566-583.
6. Holz, F.G., Amoaku, W., Donate, J. et al.: Safety and efficacy of a flexible dosing regimen of ranibizumab in neovascular age related macular degeneration: the SUSTAIN study. Ophthalmology, 118, 2011; 4 : 663–671.
7. Houfa, Y., Xiaoyun, F., Jian, M. et al.: Idiopathic Choroidal Neovascularization: Intraocular Inflammatory Cytokines and the Effect of Intravitreal Rinibizumab Treatment. Scientific Reports, 6, 2016, Article number: 31880. Doi:10.1038/srep31880., Dostupné na: https://www.nature.com/articles/srep31880
8. Chuanfeng, F., Qiang, J., Yu, W. et al.: Clinical Efficacy of Intravitreal Ranibizumab in Early and Mid-Idiopathic Choroidal Neovascularization. Journal of Ophthalmology, Volume 2014, Article ID 382702, Dostupné na http://dx.doi.org/10.1155/2014/382702.
9. Inagaki, M., Harada, T., Kiribuchi, T. et al.: Subfoveal choroidal neovascularization in uveitid. Ophthalmologica, 2010, 1996; 4 : 229 – 233.
10. Klein, R., Peto, T., Bird, A., et al.: The epidemiology of age-related macular degeneration. Am J Ophthalmol, 137, 2004; 3 : 486 – 495.
11. Lai, T.Y.Y., Staurenghi, G., Lanzetta, P. et al.: Efficacy and safety of ranibizumab for the treatment of choroval neovascularization due to uncommon cause. Twelve-Month Results of the Minerva Study. Retina, 0, 2017; 1-14.
12. Sasahara, M., Otani, A., Yodoi, Y. et al.: Circulating hematopoietic stem cells in patients with idiopathic choroidal neovascularization. Invest Ophthalmol Vis Sci, 50, 2009; 4 : 1575–1579.
13. Spaide, R.F.: Choroidal neovascularization in younger patients. Curr Opin Ophthalmol, 10, 1999; 3 : 177–181.
14. Tufail, A., Narendran, N., Patel, P.J. et al.: Ranibizumab in myopic choroidal neovascularization: the 12-month results from the REPAIR study. Ophthalmology, 120, 2013; 9 : 1944–1945.e1.
15. Tufail, A., Patel, P.J., Sivaprasad, S. et al.: Ranibizumab for the treatment of choroidal neovascularisation secondary to pathological myopia: interim analysis of the REPAIR study. Eye (Lond), 27, 2013; 6 : 709–715.
16. Wolf, S., Balciuniene, V.J., Laganovska, G. et al.: RADIANCE: a randomized controlled study of ranibizumab in patients with choroidal neovascularization secondary to pathologic myopia. Ophthalmology, 121, 2014; 3 : 682–692.e2.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2019 Issue 1-
All articles in this issue
- Využití shear waves elastografie k diagnostice změn okohybných svalů u pacientů s endokrinní orbitopatií
- Léčba idiopatické choroidální neovaskulární membrány ranibizumabem – naše zkušenosti
- Postradiačná makulopatia u pacientov s malígnym melanómom corpus ciliare a chorioidey po stereotaktickej rádiochirurgii
- Efektivní separace tkáňových vrstev dárcovské rohovky pro DMEK injekcí tekutiny mezi Descemetskou membránu a rohovkové stroma: Výsledky prvního souboru operací
- Primární orbitální teratom
- Pozdní pooperační syndrom distenze pouzdra
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Pozdní pooperační syndrom distenze pouzdra
- Primární orbitální teratom
- Léčba idiopatické choroidální neovaskulární membrány ranibizumabem – naše zkušenosti
- Postradiačná makulopatia u pacientov s malígnym melanómom corpus ciliare a chorioidey po stereotaktickej rádiochirurgii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

