-
Medical journals
- Career
Pars plana vitrektómia a kombinovaná liečba pars plana vitrektómia, triamcinolon acetonid intravitreálne a laserkoagulácia makuly pri diabetickom edéme makuly – ročné výsledky
: J. Štefaničková 1; P. Strmeň 1; K. Vavrová 1; L. Mrózová 2; V. Krásnik 1
: Klinika oftalmológie LFUK a UNB Bratislava, prednosta doc. MUDr. Vladimír Krásnik, PhD. 1; Caldera, s. r. o., vedúci Mgr. Miroslav Helbich, PhD. 2
: Čes. a slov. Oftal., 68, 2012, No. 5, p. 180-188
: Original Article
Cieľ:
V prospektívnom sledovaní porovnať anatomické a funkčné výsledky pars plana vitrektómie (PPV) so zlúpnutím vnútornej hraničnej membrány (MLI) (súbor PPV) a pars plana vitrektómie so zlúpnutím MLI, aplikáciou triamcinolonu acetonid 4 mg intravitreálne (TRIAM) a laserkoaguláciu makuly (súbor PPV + TRIAM) u očí s difúznym diabetickým edémom makuly (DEM).Metódy:
V súbore PPV bola vykonaná PPV so zlúpnutím MLI a v súbore PPV + TRIAM bola vykonaná PPV so zlúpnutím MLI, triamcinolon acetonid 4 mg bol aplikovaný intravitreálne na konci operácie a laserkoagulácia makuly 3 týždne od operácie. Centrálna ostrosť zraku (COZ), centrálna hrúbka makuly (CMT) a objem makuly boli zaznamenané pred operáciou, 1., 3., 6. a 12. mesiac po PPV.Výsledky:
Zaradených bolo 68 očí u 59 pacientov s DEM nereagujúcim na laserkoaguláciu alebo s vitreomakulárnou trakciou, v súbore PPV 35 očí a v súbore PPV + TRIAM 33 očí. V súbore PPV bola pred operáciou, v 1., 3., 6. a 12. mesiaci po operácii priemerná COZ 0,22; 0,21; 0,28; 0,32; 0,30, priemerná CMT 497,69 μm; 400,89 μm; 356,46 μm; 346,89 μm; 319,49 μm a priemerný objem makuly 11,48 mm3; 9,82 mm3; 9,28 mm3; 9,07 mm3, 8,83 mm3. V súbore PPV + TRIAM bola priemerná COZ 0,18; 0,16; 0,23; 0,26; 0,26, priemerná CMT 447,82 μm; 276,03 μm; 266,27 μm; 268,36 μm; 251,15 μm, priemerný objem makuly 10,71 mm3; 8,03 mm3; 8,28 mm3; 7,96 mm3; 7,66 mm3. Štatisticky významné zlepšenie COZ bolo sledované v obidvoch súboroch od 3. mesiaca (p = 0,0013), pri CMT a hrúbke makuly od 1. pooperačného mesiaca (< 0,001). Porovnaním obidvoch súborov, v súbore PPV + TRIAM pri kombinovanej liečbe sme zistili štatisticky významnú zmenu CMT a hrúbky makuly v 1. mesiaci oproti hodnotám pred operáciou (p = 0,002), čo však nebolo spojené so štatisticky významnou zmenou v COZ (p = 0,229). Najčastejšou pooperačnou komplikáciou bolo zvýšenie vnútroočného tlaku a operácia šošovky, častejšie v súbore PPV + TRIAM (p = 0,153, p = 0,056).Záver:
Obidva operačné postupy sú efektívne v liečbe DEM. Kombinovaná liečba PPV, triamincinolon acetonid 4 mg a laserkoagulácia makuly je spojená s vyšším výskytom pooperačných komplikácií (zvýšenie vnútroočného tlaku a operácie šošovky).Kľúčové slová:
diabetický edém makuly, pars plana vitrektómia, kombinovaná liečba
Diabetes mellitus je závažný zdravotný problém a jeho prevalencia stále stúpa. Starnutie populácie, zmeny stravovacích návykov a nárast obezity spôsobilo, že je stále viac jednotlivcov postihnutých týmto ochorením a komplikáciami s ním spojenými.
Diabetická retinopatia je jedna z najdiskutovanejších mikrovaskulárnych komplikácií ochorenia DM. Vo vekovej skupine 25–74 rokov je najčastejšou príčinou slepoty v rozvinutých krajinách. Štandardnou liečbou diabetickej retinopatie do dnešných dní je laserkoagulácia. V štúdii Early Treatment Diabetic Retinopathy Study (ETDRS) (8) sa potvrdilo, že laserkoagulácia pri diabetickom edéme makuly (DEM) redukuje stredne ťažkú stratu centrálnej ostrosti zraku (COZ) o 50 %, ale aj napriek tejto intenzívnej liečbe u niektorých pacientov dochádza k zhoršeniu COZ. Jednou z liečebných možností u pacientov s DEM, najmä difúznym, je aj pars plana vitrektómia (PPV). Predpokladá sa, že uvoľnením všetkých trakčných síl na sietnicu a zlepšením oxygenácie sietnice po PPV môžeme zmenšiť opuch sietnice (29).
Kortikosteroidy aplikované do dutiny sklovca môžu spôsobiť redukciu opuchu sietnice a v závislosti od rozsahu ischémie makuly aj zlepšenie COZ (15). Počas PPV sa používajú na vizualizáciu sklovca, napomáhajú jeho kompletnému odstráneniu, uľahčujú zlúpnutie vnútornej hraničnej membrány (MLI) a v pooperačnom období sa využíva ich protizápalový a antiedematózny účinok. V oftalmológii sa najčastejšie používa látka triamcinolon acetonid (TRIAM) (15).
Cieľom tejto prospektívnej štúdie u očí s DEM nereagujúcim na laserkoaguláciu alebo s prítomnosťou vitreomakulárnej trakcie je porovnať funkčné a anatomické výsledky operácii PPV so zlúpnutím MLI a PPV so zlúpnutím MLI doplnenej o aplikáciu TRIAM na konci operácie a laserkoaguláciu makuly 3 týždne po operácii.
MATERIÁL A METODIKA
Do prospektívneho nerandomizovaného sledovania boli zaradené oči po splnení uvedených kritérií: dĺžka trvania DEM menej ako 2 roky (24 mesiacov); doba sledovania minimálne 12 mesiacov a dodržiavanie pravidelných kontrol podľa objednania; HbA1c menej ako 10 % metódou DCCT za posledný rok pred operáciou; podrobné interné vyšetrenie s údajmi o prítomnej hypertenzii, poruche metabolizmu lipidov a proteinúrii; COZ menej ako 0,6 na Snellenových optotypoch; nález DEM s vitreomakulárnou trakciou potvrdenou OCT alebo DEM nereagujúci na laserkoaguláciu; centrálna hrúbka makuly (CMT) > 300 μm na OCT; PPV bez operácie šošovky v jednom sedení; číre optické média v 1., 3., 6. a 12. mesiaci po operácii, aby bolo možné urobiť OCT vyšetrenie (neprítomnosť krvi, exsudátu, silikónového oleja alebo plynu v dutine sklovca). Kritéria pre vylúčenie očí zo sledovania boli nasledovné: laserkoagulácia makuly menej ako 3 mesiace pred operáciou, panretinálna laserkoagulácia menej ako 4 mesiace pred operáciou, intravitreálna aplikácia kortikosteroidov alebo inhibítorov cievneho endotelového rastového faktoru (VEGF) menej ako 3 mesiace pred operáciou, predchádzajúca PPV, iná operácia oka menej ako 6 mesiacov pred operáciou (napríklad operácia šošovky alebo trabekulektómia), nepriehľadné optické médiá v pooperačnom období.
V súbore PPV bola u všetkých očí uskutočnená PPV so zlúpnutím MLI. Laserkoagulácia bola možná najskôr 3 mesiace od operácie. V súbore PPV + TRIAM boli všetky oči liečené PPV so zlúpnutím MLI a aplikáciou TRIAM 4mg do dutiny sklovca na konci operácie a laserkoaguláciou makuly 3 týždne po operácii.
Po operácii boli oči vyšetrené v 1., 3., 6. a 12. mesiaci v obidvoch súboroch. Pri každej kontrole boli urobené nasledovné vyšetrenia: COZ, CMT a objem makuly na OCT (Stratus 3.0 Zeiss Humphrey, San Leonardo, California, USA), zmeraný vnútroočný tlak (VOT) a sledovaný výskyt pooperačných komplikácií. Centrálna ostrosť zraku bola vyšetrená na Snellenových optotypoch a uvádzaná v decimálnom skóre. Za zlepšenie COZ sme považovali zlepšenie o 2 a viac riadkov Snellenových optotypov, za zhoršenie pokles COZ o 2 a viac riadkov Snellenových optotypov a za stabilizáciu COZ ± 1 riadok Snellenových optotypov.
V pooperačnom období boli sledované skoré komplikácie, ktoré sa vyskytli do 1. mesiaca od operácie a neskoré komplikácie.
Doplňujúca laserkoagulácia v súbore PPV bola možná podľa rozhodnutia operatéra po 3 mesiacoch od operácie. V súbore PPV + TRIAM doplňujúca laserkoagulácia pri pretrvávaní DEM bola možná 3 mesiace od laserkoagulácie prevedenej 3 týždne po operácii. Intravitreálna aplikácia liečiv v pooperačnom období nebola možná u žiadneho pacienta.
Na štatistické spracovanie údajov sme použili Wilcoxonov neparametrický test. Pri zisťovaní rozdielu nutnosti operácie šošovky v pooperačnom období medzi skupinami PPV a PPV+TRIAM bol použitý Fisherov exaktný test. Za štatisticky významnú hladinu sme považovali p < 0,05. Koreláciu medzi jednotlivými sledovanými parametrami alebo ich zmenu sme merali Pearsonovým koeficientom korelácie.
VÝSLEDKY
Do prospektívneho nerandomizovaného sledovania bolo zaradených 68 očí u 59 pacientov, 27 mužov a 32 žien. V súbore PPV sme sledovali 35 očí u 28 pacientov, z toho 14 mužov (50 %) a 14 žien (50 %). V súbore PPV + TRIAM bolo sledovaných 33 očí u 31 pacientov, 13 mužov (42 %) a 18 žien (58 %). Priemerný vek zaradených pacientov v skupine PPV bol 59,71 ± 10,0 roka, od 37 do 80 rokov. V skupine PPV + TRIAM bol priemerný vek 62,36 ± 6,39 roka, od 52 do 76 rokov.
V skupine PPV bolo zaradených 27 pacientov (96,43 %) s DM typ 2 a jedna pacientka (3,57 %) s DM typ 1. Priemerná dĺžka trvania DM v čase operácie bola 15,34 ± 9,44 roka. Priemerná hodnota HbA1c pred operáciou bola v tejto skupine 8,40 ± 0,78 %. Do skupiny PPV + TRIAM bolo zaradených 29 pacientov (93,55 %) s DM typ 2 a dvaja pacienti (6,45 %) s DM typ 1. Priemerná dĺžka trvania DM v čase operácie bola 16,15 ± 8,73 roka a priemerná hodnota HbA1c pred operáciou bola 8,33 ± 0,89 %. Doba sledovania bola v obidvoch súboroch 12 mesiacov. Doba zhoršovania COZ zaznamenaná subjektívne pacientom bola v súbore PPV 12,97 ± 7,93 mesiaca a v súbore PPV + TRIAM 14,94 ± 6,27 mesiaca (tab. 1).
1. Charakteristika vyšetrovaných súborov pacientov 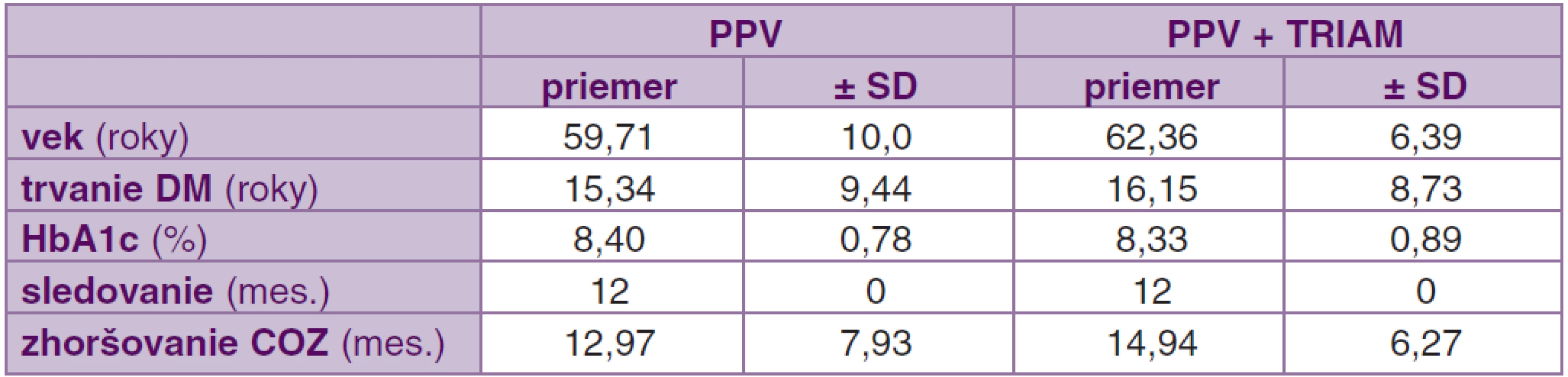
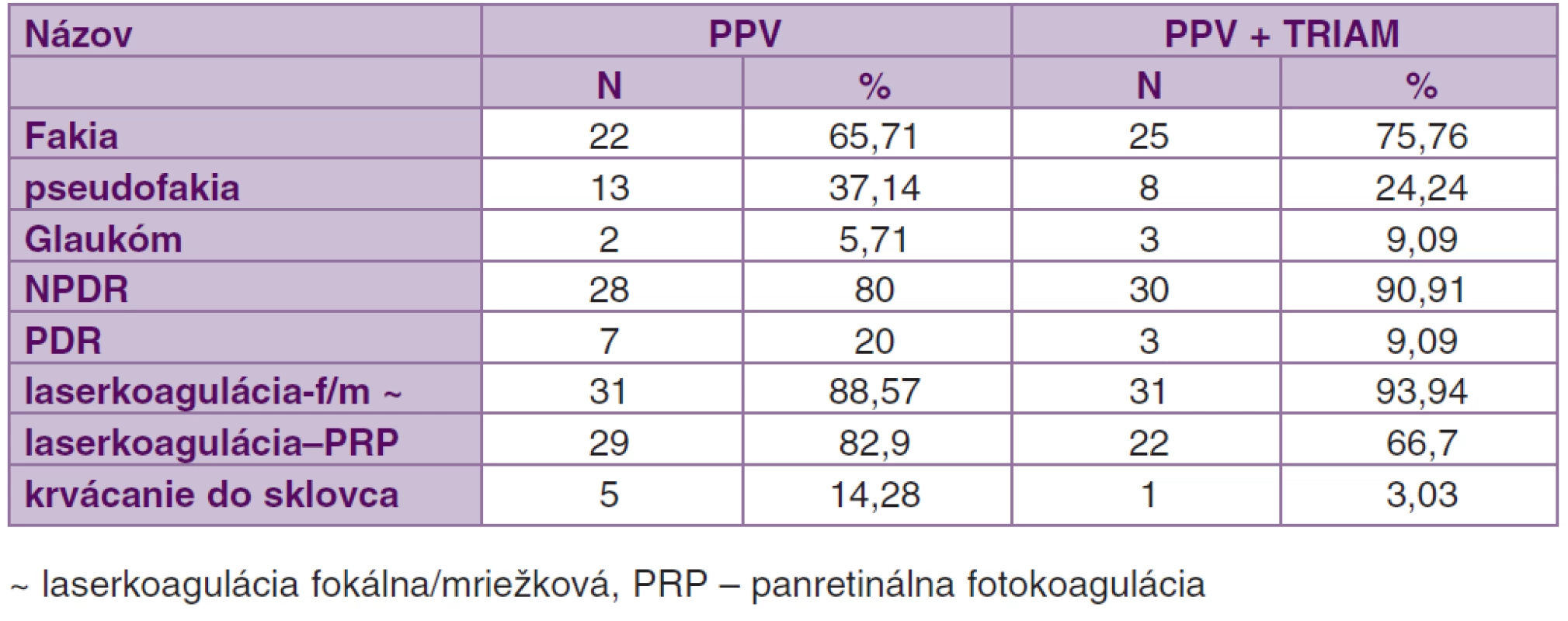
V súbore PPV bola NPDR u 28 (80 %), PDR u 7 očí (20 %). V súbore PPV + TRIAM NPDR u 30 očí (90,91 %) a PDR u troch očí (9,09 %). U očí s PDR boli zistené len malé neovaskularizácie na TZN bez trakcie na okolitú sietnicu. Diabetický edém makuly bol na všetkých očiach v obidvoch súboroch. Vitreomakulárna trakcia bola indikáciou k operácii v súbore PPV u 26 očí (74,29 %), v súbore PPV + TRIAM u 28 očí (84,85 %). Krvácanie do sklovca malého rozsahu bolo pozorované u 5 očí (14,28 %) v skupine PPV a u jedného oka (3,03 %) v skupine PPV + TRIAM (tab. 2).
Všetci pacienti podstúpili štandardnú 3-bránovú PPV. V súbore PPV bola 23G PPV vykonaná u 14 očí (40 %) a v súbore PPV + TRIAM u 30 očí (90,91 %). Pred operáciou bola epiretinálna membrána (ERM) diagnostikovaná u 12 očí (34,29 %) v súbore PPV a v súbore PPV + TRIAM u 7 očí (21,21 %). Peroperačne bola ERM zistená v súbore PPV u 17 očí (48,57 %) a v súbore PPV + TRIAM u 13 očí (39,39 %). U 25 očí (71,43 %) v súbore PPV a u 29 očí (87,88 %) v súbore PPV + TRIAM nebola nutná žiadna tamponáda dutiny sklovca na konci operácie. Zlúpnutie MLI po predchádzajúcom ofarbení trypánovou modrou a kryokoaguláciu za sklerotómie na konci operácie sme robili na všetkých očiach (tab. 3).
3. Charakteristika operačných postupov. 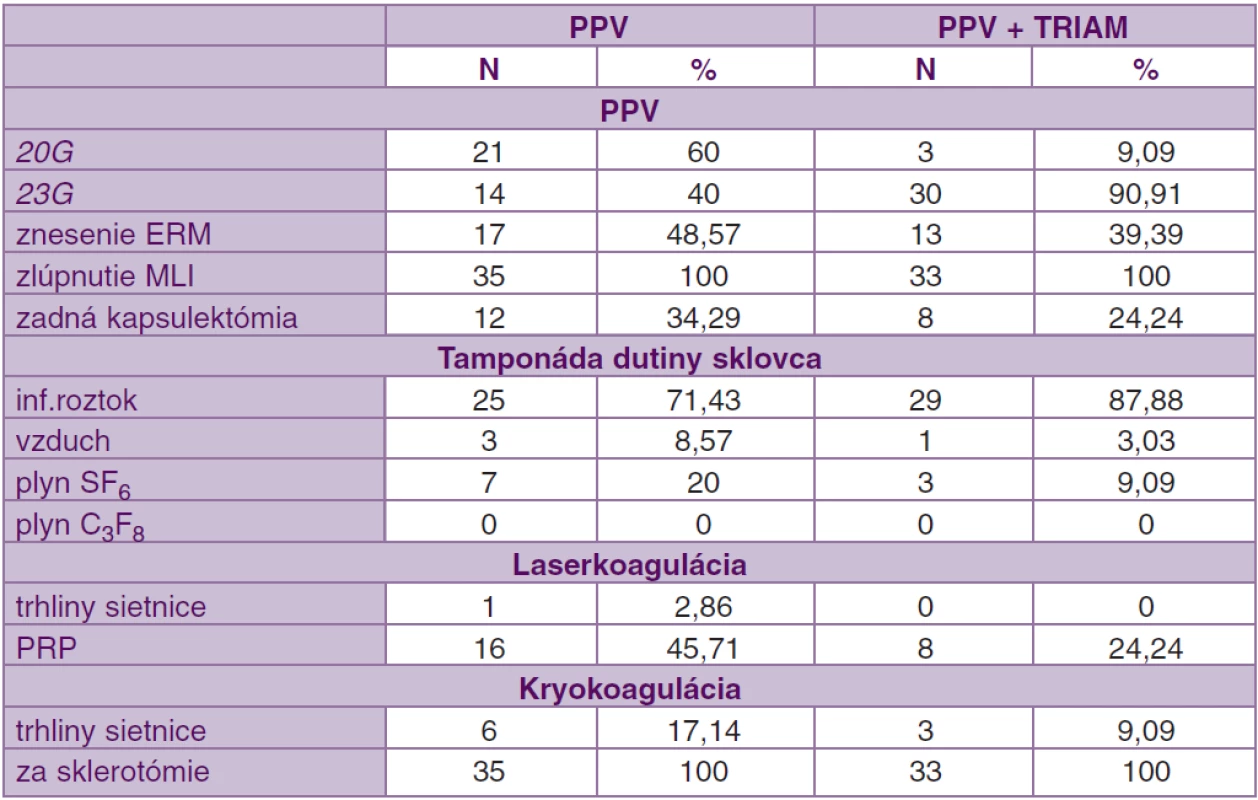
Centrálna ostrosť zraku
Priemerná COZ v 12. mesiaci po operácii v súbore PPV bola 0,30 a v súbore PPV + TRIAM 0,26. V súbore PPV sa u 10 očí (28,57 %) COZ zlepšila o 2 a viac riadkov, u 2 očí (5,72 %) klesla COZ o 2 a viac riadkov a stabilizáciu sme dosiahli u 23 očí (65,71 %). V súbore PPV + TRIAM sme v 12. mesiaci pozorovali zlepšenie COZ o 2 a viac riadkov u 7 očí (21,21 %), zhoršenie o 2 a viac riadkov u jedného oka (3,03 %) a stabilizáciu sme dosiahli u 25 očí (75,76 %) (tab. 4).
4. Priemerné hodnoty centrálnej ostrosti zraku 
Priemerná zmena COZ v súbore PPV v 12. mesiaci bola 0,11 (CI 95 %; 0,05, 0,16, p = 0,0013),v súbore PPV + TRIAM 0,08 (CI 95 %; 0,03, 0,13, p < 0,001). Štatisticky významný rozdiel v sledovanej hodnote COZ medzi súbormi PPV a PPV + TRIAM sa v 12. mesiaci nepotvrdil, p = 0,375 (tab. 5, graf. 1).
5. Porovnanie súbor PPV vs. PPV + TRIAM. Priemerné hodnoty zmeny centrálnej ostrosti zraku pred operáciou až 12. mesiac 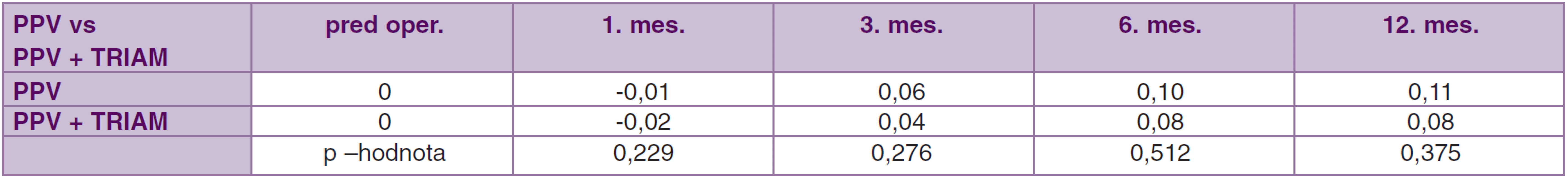
1. Priemerná zmena centrálnej ostrosti zraku 
Centrálna hrúbka makuly
Priemerná CMT pred operáciou v súbore PPV bola 497,69 ± 168,92 μm a v súbore PPV + TRIAM 447,82 ± 119,53 μm (tab. 6). V súbore PPV malo v 12. mesiaci 20 z 35 očí (57,14 %) CMT < 300 μm, pričom CMT < 250 μm malo 16 z 35 očí (45,71 %). Ďalším 6 z 35 očí (17,14 %) sa CMT znížila o viac ako 20 %. Centrálnu hrúbku makuly < 300 μm v súbore PPV + TRIAM malo v 12. mesiaci 30 z 33 očí (90,90 %), z toho CMT < 250 μm malo 16 z 33 očí (48,48 %). Dvom očiam z 35 (5,71 %) v súbore PPV a dvom očiam z 33 očí (6,06 %) v súbore PPV + TRIAM sa v 12. mesiaci zvýšila CMT o viac ako 20 % a tento trend pokračuje aj v ďalších mesiacoch sledovania. V 12. mesiaci bola v súbore PPV priemerná zmena CMT -178 μm (CI 95 %; -50, -144 μm, p < 0,001) a v súbore PPV + TRIAM -197 μm (CI 95 %; -142, -252 μm,( p < 0,001) (tab. 6, 7, graf 2).
6. Priemerné hodnoty centrálnej hrúbky makuly (μm) 
7. Porovnanie súbor PPV vs. PPV + TRIAM. Priemerné hodnoty zmeny centrálnej hrúbky makuly (μm) pred operáciou až 12. mesiac 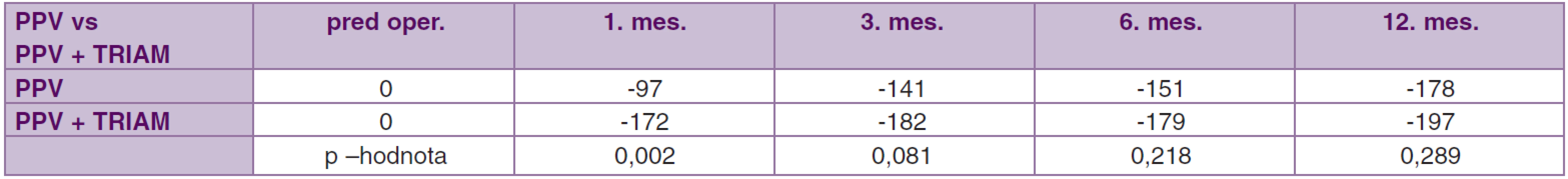
2. Priemerná zmena centrálnej hrúbky makuly (μm) 
V obidvoch súboroch vo všetkých sledovaných mesiacoch po operácii nastalo štatisticky významné zníženie CMT (p < 0,001), pričom neboli zaznamenané výraznejšie rozdiely v jednotlivých mesiacoch medzi súbormi okrem prvého mesiaca. V prvom mesiaci po operácii v skupine PPV + TRIAM bolo zistené až dvojnásobne zníženie CMT oproti súboru PPV, čo je spôsobené použitím TRIAM na konci operácie (p = 0,002) (tab. 7, graf. 2).
Objem makuly
V súbore PPV bol priemerný objem makuly pred operáciou 11,48 ± 2,39 mm3 a v súbore PPV + TRIAM 10,71 ± 2,62 mm3. Priemerný objem makuly v 12. mesiaci po operácii sa zmenšil na 8,83 mm3 resp. 7,66 mm3 (tab. 8).
8. Priemerné hodnoty objemu makuly (mm<sup>3</sup>) 
V 12. mesiaci po operácii bola v súbore PPV priemerná zmena objemu makuly -2,65 mm3 (CI 95 %; -1,57, -3,73, p < 0,001). V súbore PPV + TRIAM bola priemerná zmena objemu makuly v 12. mesiaci -3,05 mm3 (CI 95 %; -2,18, -3,92 mm3, p < 0,001). Vo všetkých mesiacoch v obidvoch súboroch nastalo zníženie objemu makuly (p < 0,001) bez výraznejších rozdielov v jednotlivých mesiacoch okrem prvého mesiaca. V prvom mesiaci po operácii v súbore PPV + TRIAM sme zaznamenali výraznejšie zníženie objemu makuly oproti súboru PPV, čo je tiež ako pri CMT spôsobené použitím TRIAM na konci operácie (p = 0,027) (tab. 8, 9, graf. 3).
9. Porovnanie súbor PPV vs. PPV + TRIAM. Priemerné hodnoty zmeny objemu makuly (mm<sup>3</sup>) pred operáciou až 12. mesiac 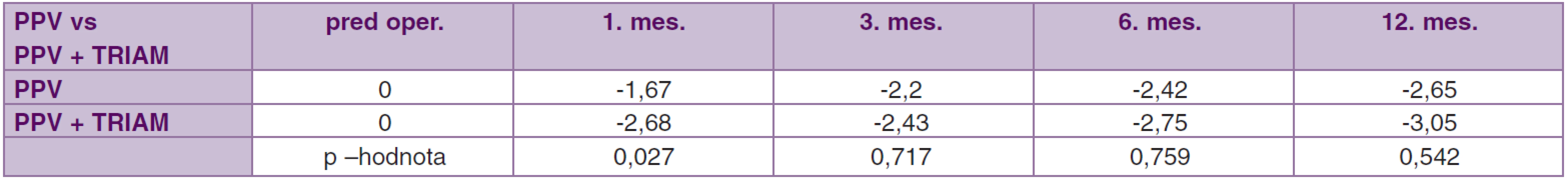
3. Priemerná zmena objemu makuly (mm<sup>3</sup>) 
Na grafoch znázorňujúcich vzťahy medzi vstupnými hodnotami – závislosť COZ od CMT vidíme, že v súbore PPV bolo zaradených viac očí s vyššími hodnotami CMT ako v súbore PPV + TRIAM. Výskyt očí s nižšími vstupnými hodnotami COZ bol približne rovnaký v obidvoch súboroch (graf. 4, 5).
Graf 4, 5. Súbor PPV a súbor PPV + TRIAM. Vstupné hodnoty - grafická závislosť hodnôt centrálnej ostrosti zraku od centrálnej hrúbky makuly (μm) 
Na výsledných grafoch vidíme výsledný posun k nižším hodnotám CMT a vyšším hodnotám COZ (graf. 6, 7).
Graf. 6, 7. Súbor PPV a súbor PPV + TRIAM. Grafická závislosť hodnôt centrálnej ostrosti zraku od centrálnej hrúbky makuly (μm) v 12. mesiaci 
Pre porovnanie závislosti medzi jednotlivými súbormi sme porovnávali vstupné hodnoty COZ, CMT, objem makuly a zmenu v 12. mesiaci. Koreláciu sme vyjadrili pomocou Pearsonovho koeficientu korelácie.
V súbore PPV sme dokázali štatistickú závislosť medzi vstupnou hodnotou CMT a objemom makuly so zmenou v 12. mesiaci (p < 0,001). To znamená, že čím väčšia CMT pred operáciou, tým väčšia zmena (pokles) po operácii. Tie isté závery sme potvrdili aj pre objem makuly (tab. 10).
10. Korelácie (závislosť) medzi jednotlivými parametrami pred operáciou a ich zmenou počas 12 mesiacov po operácii v súbore PPV 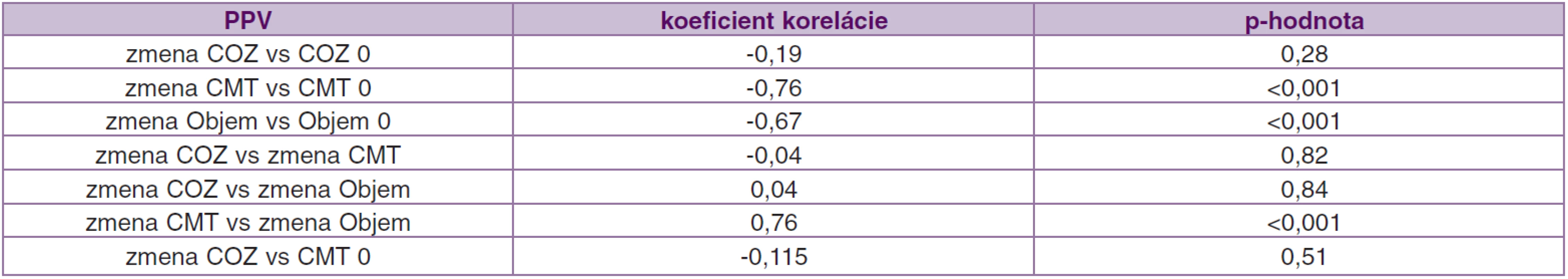
V súbore PPV + TRIAM sme dokázali podobné výsledky. Štatisticky významnú hladinu sme potvrdili pri meraniach CMT a objem makuly (v oboch meraniach p < 0,001). V tomto súbore výsledky CMT aj objemu makuly potvrdzujú významnosť štatistických rozdielov na hladine p = 0,05 (tab. 11).
11. Korelácie (závislosť) medzi jednotlivými parametrami pred operáciou a ich zmenou počas 12 mesiacov po operácii v súbore PPV + TRIAM 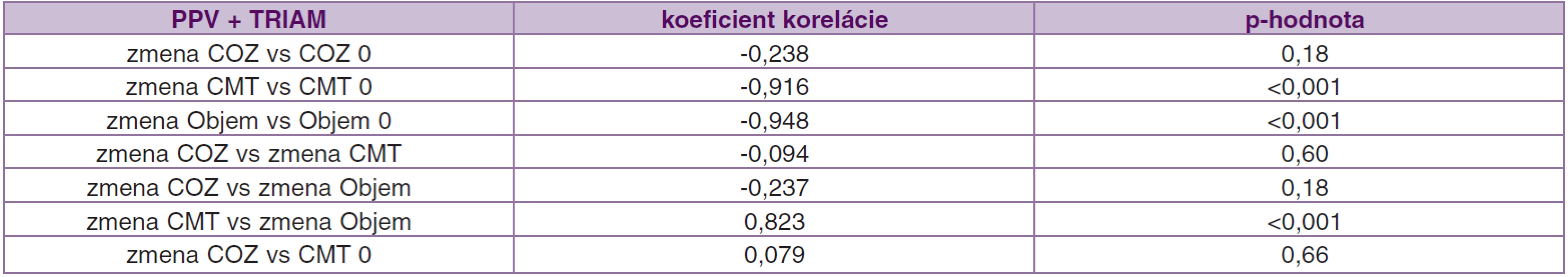
Komplikácie
Najčastejšou peroperačnou komplikáciou boli trhliny sietnice. V súbore PPV sme trhlinu na jednom oku (2,86 %) ošetrili laserkoaguláciou a na 6 očiach (17,14 %) sme použili kryokoaguláciu. V súbore PPV + TRIAM sme peroperačne vzniknuté trhliny ošetrili pomocou kryokoagulácie na 3 očiach (9,09 %). U všetkých týchto očí bol aplikovaný na konci operácie expanzný plyn SF6.
V prvom roku sledovania sme zvýšenie VOT nad 25 mmHg pozorovali u 5 očí (14,29 %) v súbore PPV a u 9 očí (27,27 %) v súbore PPV + TRIAM. U všetkých očí so zvýšeným VOT bola nasadená monoterapia. U jedného oka (2,86 %) v súbore PPV a troch očí (9,09 %) v súbore PPV + TRIAM, ktoré boli pred operáciou sledované pre primárny glaukóm s otvoreným uhlom a liečené monoterapiou, bolo nutné pridať do liečby ďalšie antiglaukomatikum. Fibrínová reakcia v PK bola na 5 očiach (14,29 %) v súbore PPV a na 4 očiach (12,12 %) v súbore PPV + TRIAM. Vo všetkých prípadoch reakcia vymizla do jedného týždňa od operácie. Krvácanie do dutiny sklovca bolo na dvoch očiach (5,71 %) v súbore PPV a na jednom oku (3,03 %) v súbore PPV + TRIAM. Vo všetkých prípadoch sa vstrebalo spontánne bez nutnosti chirurgickej intervencie. Hypotónia 1. deň po operácii bola zistená na jednom oku po 23G PPV. Odlúčenie sietnice a endoftalmitídu sme nezaznamenali ani na jednom oku.
V obidvoch súboroch sme prospektívne sledovali nutnosť operácie šošovky v pooperačnom období a priemernú dobu do operácie šošovky. V súbore PPV sme operáciu šošovky uskutočnili u 4 z 22 fakických očí (18,18 %). Trinásť očí (37,14 %) bolo v čase operácie PPV pseudofakických. Priemerná doba do operácie šošovky bola 8,56 ± 3,11 mesiaca. V súbore PPV + TRIAM bolo hodnotených 25 fakických očí. Umelú vnútroočnú šošovku malo pred operáciou 8 očí (24,24 %). Operácia šošovky bola nutná u 11 očí (44,0 %), priemerná doba do operácie bola 6,25 ± 3,65 mesiaca. V súbore PPV + TRIAM bol vyšší výskyt následných operácií šošovky ako v súbore PPV (p = 0,056) (tab. 12).
12. Operácie šošovky v súboroch PPV a PPV + TRIAM 
DISKUSIA
Diabetický edém makuly (DEM) predstavuje závažnú príčinu zhoršenia COZ u pacientov s cukrovkou. Prísna kontrola hladiny glukózy a hodnôt krvného tlaku takisto ako fokálna/mriežková laserokoagulácia sú efektívne postupy u mnohých pacientov, ale aj tak existuje skupina pacientov, u ktorej dochádza k zhoršeniu COZ (22).
V našom sledovaní sme hodnotili vplyv PPV so zlúpnutím MLI na vstrebanie DEM a výslednú COZ. Ďalej sme sledovali, či doplnenie tejto operačnej procedúry o aplikáciu triamcinolon acetonidu 4 mg na konci operácie a laserkoaguláciu makuly 3 týždne po operácii, má signifikantný vplyv na nami sledované veličiny. Sledovaných bolo 68 očí u 59 pacientov, ktorí boli rozdelení do 2 súborov: súbor PPV 35 očí, u ktorých sme previedli PPV so zlúpnutím MLI, súbor PPV + TRIAM 33 očí, u ktorých sme previedli PPV so zlúpnutím MLI, aplikáciou TRIAM a laserkoaguláciou makuly 3 týždne po operácii.
Jednu z najdôležitejších úloh pri vzniku a trvaní difúzneho DEM hrá sklovec (25, 26). Dôkazy o úlohe sklovca pri vzniku a trvaní DEM vychádzajú z početných štúdií. Od roku 1992, keď Lewis et al. (20) popísali benefit PPV u 10 očí so zhrubnutou a natiahnutou zadnou kôrou sklovca (ZKS) pred makulou pri DEM, nastal zvýšený záujem vo vitreoretinálnej chirurgii o chirurgickú liečbu DEM. V ich sledovaní PPV spojená s odstránením ZKS viedla k vstrebaniu edému u všetkých 10 očí a zlepšenie COZ nastalo u 8 z 10 očí. Následne ďalší autori potvrdili pozitívny efekt PPV pri liečbe DEM so zhrubnutou a natiahnutou ZKS (12, 14, 24). V ďalšom období bolo publikovaných viacero retrospektívnych klinických štúdií, ktoré ukázali, že PPV s odstránením ZKS pri DEM s trakciou môže viesť k zmenšeniu edému a zlepšeniu zrakových funkcií (30, 32). Na druhej strane PPV môže viesť k zmenšeniu edému makuly u očí s DR aj bez prítomnosti zjavnej vitreomakulárnej trakcie (6, 17, 31). La Heij et al. (17) publikovali prácu, kde opísali vstrebanie DEM po PPV na 19 očiach bez prítomnosti vitreomakulárnej trakcie pred operáciou. Tachi a Ogino (31) pozorovali efekt PPV pri difúznom DEM u 58 očí s priloženou ZKS. Po 12 mesiacoch sledovania nastalo vstrebanie edému u 92 % očí a zlepšenie COZ u 53 % očí.
Vstrebanie edému u pacientov s difúznym DEM nie je podmienené len uvoľnením všetkých trakčných síl z povrchu sietnice, ale pravdepodobne aj elimináciou faktorov zvyšujúcich priepustnosť, ako napríklad VEGF, a pravdepodobne aj lepším transportom a penetráciou kyslíka a výživových látok cez dutinu sklovca k makule. Počas PPV viskózny gél nahrádzame málo viskóznym infúznym roztokom, čo má za následok zvýšený transport molekúl v dutine sklovca. Na základe týchto zmien, môže byť napríklad kyslík presunutý z dobre zásobených oblastí sietnice do hypoxických (28, 29). Holekamp et al. (11), Maeda a Tano (21) a Steffanson et al. (29) dokázali, že PPV redukuje hypoxiu sietnice u experimentálnych zvierat aj ľudí. Niektorí dokazujú, že kyslíková liečba znižuje rozsah DEM a pôsobením kyslíka dochádza k redukcii VEGF (23). Spotrebu kyslíka sietnicou znižujeme aj pri laserkoagulácii, čím vysvetľujeme jej účinok v liečbe DR (29). Antonetti et al. (1) ukázali, že zvýšenie hladiny VEGF v sklovci je spojené so znížením hladiny okludínu a poškodením pevných endoteliálnych spojení. Tieto zmeny tiež prispievajú k zvýšeniu permeability ciev u pacientov s DEM. Predpokladá sa, že účinok PPV pri vstrebaní DEM vzniká kombináciou oboch mechanizmov a) uvoľnením všetkých trakčných síl z povrchu sietnice; b) zlepšením zásobenia sietnice kyslíkom a znížením koncentrácie faktorov zvyšujúcich permeabilitu ciev (11).
Stolba et al. (30) v prospektívnej randomizovanej štúdii dokázali, že PPV so zlúpnutím MLI je spojená s lepšími funkčnými a anatomickými výsledkami ako naturálny priebeh ochorenia. Yanyali et al. (33) sledovali lepší efekt PPV so zlúpnutím MLI na vstrebanie DEM a COZ v porovnaní s jedným sedením mriežkovej laserkoagulácie. Gandorfer et al. (9) vo svojej malej štúdii u 12 pacientov po PPV so zlúpnutím MLI dosiahli zlepšenie COZ o 2 a viac riadkov Snellenových optotypov u 92 % pacientov 4–12 týždňov po operácii. Vznik nového alebo zhoršenie existujúceho edému nepozorovali ani u jedného pacienta počas priemernej doby sledovania 16 mesiacov (8–31 mesiacov). Peroperačne zistili zhrubnutú a priloženú ZKS k makule u 10 pacientov. U dvoch pacientov po PPV pozorovali patologický reflex na povrchu sietnice, ale žiadnu membránu pred makulou. Pars plana vitrektómia so zlúpnutím MLI viedla k zlepšeniu COZ a vstrebaniu edému bez vzniku nových epiretinálnych membrán v pooperačnom období. Preto kompletné uvoľnenie tangenciálnej trakcie a inhibícia reproliferácie fibróznych astrocytov je dobre uváženou voľbou v liečbe pacientov s DEM a pokročilých ochorení vitreomakulárneho rozhrania (9). Mechanizmus, ktorý vedie k vstrebaniu edému po zlúpnutí MLI, je pravdepodobne spôsobený kompletným uvoľnením trakčných síl, zvýšením výmeny látok medzi sietnicou a priestorom sklovca (zhrubnutá MLI pôsobí ako bariéra pre difúziu) a tým lepšou oxygenáciou makuly (6, 7).
Vstrebanie edému rok po operácii, CMT < 250 μm, sme zistili u 45,7 % očí v súbore PPV a u 48,55 % v súbore PPV + TRIAM. Centrálnu hrúbku makuly menej ako 300 μm sme dosiahli u 65,71 % očí v súbore PPV a u 90,9 % očí v súbore PPV + TRIAM, čo je štatisticky významný rozdiel (p < 0,001). Väčší počet očí s CMT < 300 μm takisto ako dvojnásobne zníženie CMT a objemu makuly v prvom mesiaci po operácii v súbore PPV + TRIAM si vysvetľujeme aplikáciou TRIAM na konci operácie a laserkoaguláciou makuly 3 týždne po operácii. Z množstva štúdii vieme, že TRIAM je účinný v liečbe DEM, zlepšuje COZ, znižuje CMT aj objem makuly, ale jeho účinok trvá len 3 až 6 mesiacov po podaní v dávke 4 mg (5, 15). Doplňujúce terapeutické zásahy, ako napríklad laserkoagulácia, môžu ešte zvýrazniť jeho účinok (16). Najvýraznejšie zníženie hrúbky makuly u očí po aplikácii TRIAM je dosiahnuté u očí so sklovcom v 4. týždni po podaní (4). Priemerný polčas vstrebania TRIAM 4 mg z oka so sklovcom je 18,6 dňa a u oka po PPV je to 3,2 dňa (3). Keďže táto doba je po vitrektómii kratšia, rozhodli sme sa pre laserkoaguláciu makuly 3 týždne po operácii u všetkých očí v danom súbore. Takto sme sa snažili byť čo najšetrnejší k očným tkanivám, najmä k sietnici počas laserkoagulácie a minimalizovať riziko rozvoja edému po laserkoagulácii. Myslíme si, že po 3 týždňoch od operácie je už predný segment stabilizovaný a pacient lepšie spolupracuje počas zákroku.
Tak ako v iných publikáciách (11, 18, 27), ani my sme nezistili koreláciu medzi zmenou COZ a redukciou hrúbky makuly, v 12. mesiaci po operácii, v súbore PPV r = -0,04, p = 0,82, a v súbore PPV + TRIAM r = -0,094, p = 0,60. Koreláciu sme potvrdili len medzi zmenou CMT a zmenou objemu makuly v 12. mesiaci, v súbore PPV r = 0,76, p < 0,001 a v súbore PPV + TRIAM r = 0,823, p < 0,001. Shah et al. (27) odporúčajú pristupovať k hodnoteniu vzťahu medzi výslednou COZ a redukciou CMT s opatrnosťou. Podobne ako my nedokázali signifikantný vzťah medzi hodnotami vstupnej COZ a redukciou CMT po operácii (p = 0,63). Predpokladajú, že príčinou môže byť dysfunkcia fotoreceptorov pri chronickom edéme, poškodenie sietnice vyvolané opakovanými laserkoaguláciami alebo poruchy perfúzie makuly. Stolba et al. (30) pozorovali stabilizáciu COZ od 6. mesiaca po operácii. My sme sledovali štatisticky významnú zmenu COZ od 3. mesiaca po operácii v obidvoch súboroch a stabilizáciu sme dosiahli tiež od 6. mesiaca. Zhodné výsledky s našimi dosiahli aj Pendergast et al. (24) u očí po PPV s natiahnutou a zhrubnutou ZKS na OCT. Stabilizáciu ± 1 riadok dosiahli u 91 % očí a zhoršenie COZ o 2 a viac riadkov u 9 % očí. U 45 očí (81,8 %) pozorovali kompletné vstrebanie edému priemerne 4,5 mesiaca od operácie. Podľa očakávania výsledky u očí s ischemickou makulopatiou boli horšie. Kang et al. (16) sledovali oči po kombinovanej liečbe PPV + TRIAM a laserkoagulácii makuly 2 týždne po operácii. U všetkých očí sa COZ štatisticky zlepšila v 3. mesiaci a zostala zlepšená aj v 6. a 12. mesiaci. Významné zlepšenie COZ zistili aj medzi 6. a 12. mesiacom. My sme pozorovali najvýraznejšie zlepšenie COZ v 3. a 6. mesiaci po operácii (v súbore PPV zmena COZ 0,06 a 0,10; v súbore PPV + TRIAM 0,04 a 0,08).
Dillinger a Mester (6) sledovali 60 očí po PPV so zlúpnutím MLI a referovali o zlepšení COZ o 2 a viac riadkov u 46 % z nich a zhoršení o 2 a viac riadkov u 7 %. Priemerná doba sledovania však bola len 3 mesiace. My sme v súbore PPV v 12. mesiaci dosiahli zlepšenie COZ o 2 a viac riadkov Snellenových optotypov u 28,57 % očí a stabilizáciu ± 1 riadok u 65,71 %, spolu stabilizáciu a zlepšenie u 94,29 %. V súbore PPV + TRIAM sme v 12. mesiaci zlepšenie o 2 a viac riadkov dosiahli u 21,21 % očí a stabilizáciu u 75,76 %. Stabilizáciu a zlepšenie COZ sme dosiahli u 96,27 % očí. V 12. mesiaci od operácie sme nezaznamenali štatisticky významný rozdiel v COZ medzi obidvoma súbormi (p=0,375). Lee et al. (19) tiež sledovali 2 súbory pacientov, u ktorých bola prevedená PPV alebo PPV + TRIAM pre rôzne cievne ochorenia sietnice. V skorom pooperačnom období (doba sledovania 2 mesiace) pozorovali štatisticky významné zlepšenie COZ v obidvoch súboroch, pričom rozdiel medzi skupinami nebol štatisticky významný (p = 0,19) takisto ako v našich súboroch. Triamcinolon acetonid indikovali na konci operácie pri náleze klinicky signifikantného edému makuly, fibrovaskulárnych tkanív a u pacientov mladších ako 40 rokov.
V našom súbore sme zaznamenali štatisticky významné zmenšenie CMT aj objemu makuly už od 1. mesiaca po operácii, ktoré pretrvávalo až do poslednej kontroly. Podobný pozitívny vplyv PPV so zlúpnutím MLI bol pozorovaný aj v iných štúdiách (9, 33). Avci et al. (2) pozorovali vstrebanie alebo zníženie edému u 81 % očí s DEM a u 92 % očí s edémom inej etiológie. Kang et al. (16) po kombinovanej liečbe (PPV + TRIAM a laserkoagulácia makuly) zistili CMT ≤ 250 μm u 67 % očí počas šesťmesačného sledovania. Tachi a Ogino (31) pozorovali vstrebanie edému v prvých 3 mesiacoch po operácii u 46,1 % očí, medzi 3 a 6 mesiacom u 20,7 % očí a medzi 6. až 12. mesiacom u 31 % očí. Tieto výsledky ukazujú, že aj po pol roku od operácie je stále šanca na vstrebanie edému.
Nepozorovali sme závažné očné komplikácie ako endoftalmitídu alebo odlúčenie sietnice. Najčastejšími komplikáciami v pooperačnom období bolo zvýšenie VOT a nutnosť operácie šošovky. Toto sú najčastejšie vedľajšie účinky po aplikácii kortikosteroidov do dutiny sklovca. V retrospektívnej štúdii Beer a Bakri (3) sledovali 43 očí a zistili zvýšenie VOT 24 mmHg a viac u 48,8 % očí a 27,5 % očí malo zvýšenie VOT viac ako 10 mmHg. Jonas et al. (15) u 75 očí 71 pacientov tiež zaznamenali zvýšenie VOT nad 21 mmHg u 52 % očí po aplikácii TRIAM. Táto štúdia má však menší dopad na prax, keďže použili dávku 25 mg, ktorá sa používa oveľa menej často ako bežná dávka 4 mg. My sme zistili zvýšenie VOT 25mmHg a viac u 14,29 % očí v súbore PPV a u 27,27 % očí v súbore PPV + TRIAM. Limitáciou tohto sledovania je, že hodnota VOT bola stanovaná na základe jedného merania pred operáciou. Ďalej u pacientov s glaukómovým ochorením je každé zvýšenie VOT závažné a zvýšenie VOT na 25 mmHg a viac môže u nich spôsobiť vážne komplikácie.
Kang et al. (16) pozorovali vznik sivého zákalu u 8 z 12 očí (66,7 %) a operácia šošovky bola prevedená u 7 z týchto očí. My sme sa zamerali len na výskyt operácii šošovky. Ani u jedného oka sme nezrealizovali operáciu šošovky spolu s operáciou na zadnom segmente naraz, aby sme sa vyhli prípadnemu negatívnemu ovplyvneniu výsledkov operáciou šošovky. Počas sledovania však bola operácia šošovky nutná u 4 očí (18,18 %) v súbore PPV a u 11 očí (44 %) v súbore PPV + TRIAM. Zistili sme častejší výskyt operácii šošovky v pooperačnom období v súbore PPV + TRIAM, p = 0,056 na hranici štatistickej významnosti. Väčšina operácii bola realizovaná medzi 6. a 12. mesiacom sledovania.
ZÁVER
Výsledky nášho sledovania demonštrujú, že obidva nami sledované operačné postupy, pars plana vitrektómia so zlúpnutím vnútornej hraničnej membrány a pars plana vitrektómia so zlúpnutím vnútornej hraničnej membrány doplnená o aplikáciu triamcinolon acetonidu 4mg na konci operácie a laserkoaguláciu makuly 3 týždne po operácii, sú efektívne v liečbe DEM. Nezistili sme štatisticky významný rozdiel medzi jednotlivými súbormi v 12. mesiaci po operácii v centrálnej ostrosti zraku, centrálnej hrúbke makuly a objeme makuly. Operácia pars plana vitrektómia so zlúpnutím vnútornej hraničnej membrány doplnená o aplikáciu triamcinolon acetonidu 4 mg na konci operácie a laserkoaguláciu makuly 3 týždne po operácii je spojená s vyšším výskytom pooperačných komplikácií (zvýšenie VOT a operácie šošovky).
Do redakce doručeno dne 9. 7. 2012
Do tisku přijato dne 16. 11. 2012
MUDr. Jana Štefaničková, PhD.
Klinika oftalmológie LFUK a UNB
Ružinovská 6
826 06 Bratislava
e-mail: jstefanicka@gmail.com
Sources
1. Antonetti, DA., Barbera, AJ., Hollinger, LA. et al.: Vascular endothelial growth factor induces rapid phosphorylation of tight junction proteins occludin and zonula occluden 1. A potential mechanismus for vascular permeability in diabetic retinopathy and tumors. J Biol Chem., 274, 1999; 33 : 23463–7.
2. Avci, R., Kaderli, B., Avci, B., et al: Pars plana vitrectomy and removal of the internal limitng membrane in the treatment of chronic macular edema. Graefes Arch Clin Exp Ophthalmol, 242; 2004 : 845–852.
3. Beer, PM., Bakri, SJ., Singh, RJ. et al.: Intraocular concentrations and pharmacocinetics of triamcinolone acetonide after a single intravitreal injections. Ophthalmology, 110; 2003 : 681–686.
4. Bonini–Filho, MA., Jorge, R., Barbosa, JC. et al.: Intravitreal injection versus sub–Tenons infusion of triamcinolone acetonide for refractory diabetic macular edema: a randomized clinical trial. Invest Ophthalmol Vis Sci, 46; 2005 : 3845–3849.
5. Chieh, JJ., Roth, DB., Liu, M. et al.: Intravitreal triamcinolone acetonide for diabetic macular edema. Retina 25; 2005 : 828–834.
6. Dillinger, P., Mester, U.: Vitrectomy with removal of the internal limiting membrane in chronic diabetic macular oedema. Graefes Arch Clin Exp Ophthalmol, 242, 2004, 630–637.
7. Ducournau, D., Ducournau, Y.: A closer look at the ILM. Retinal Physician supplementum, July/August, 2008 : 4–15.
8. Early Treatment of Diabetic Retinopathy Study Research Group. Photocoagulation for diabetic macular edema. Early Treatment Diabetic Retinopathy Study report number 1. Graefes Arch Clin Exp Ophthalmol, 103; 1985 : 1796–1806.
9. Gandorfer, A., Messmer, E., Ulbig, MW. et al.: Resolution of diabetic macular edema after surgical removal of the posterior hyaloid and the inner limiting membrane. Retina, 20, 2000, 123–133.
10. Gaucher, D., Tadayoni, R., Erginay, A. et al.: Optical coherence tomography assessment of the vitreoretinal relationship in diabetic macular edema. Am J Ophthalmol, 139; 2005 : 807–813.
11. Haller JA., Qin H., Apte RS. et al.: Vitrectomy outcomes in eyes with diabetic macular edema and vitreomacular traction. Ophthalmology, 117; 2010 : 1087–1093.
12. Harbour, JW., Smiddy, WE., Flynn, Jr. HW. et al.: Vitrectomy for diabetic associated with a thickened and taut posterior hyaloid membrane. Am J Ophthalmol, 121; 1996 : 405–413.
13. Holekamp, NM., Shui, YB., Beebe, DC. et al.: Vitrectomy surgery increases oxygen exposure to the lens: a possible mechanism for nuclear cataract formation. Am J Ophthalmol, 139; 2005 : 302–310.
14. Jahn, CE., Topfner, L., von Schutz, K.et al.: Improvement of visual acuity in eyes with diabetic macular edema after treatment with pars plana vitrectomy. Ophthalmologica, 218; 2004 : 378–384.
15. Jonas, JB.: Intravitreal triamcinolone acetonide for diabetic retinopathy. Dev Ophthalmol. Basel, Karger, 2007; vol. 39 : 96–110.
16. Kang SW., Park SC., Kang JH.: Triple therapy of vitrectomy intravitreal triamcinolone and macular laser photocoagulation for intractible diabetic macular edema. Am J Ophthalmol 144; 2007 : 878–885.
17. La Heij, EC., Hendrikse, F., Kessels, AG. et al.: Vitrectomy results in diabetic macular edema without evident vitreomacular traction. Graefes Arch Clin Exp Ophthalmol, 239; 2001 : 264–270.
18. Larrson, J., Zhu, M., Sutter, F. et al.: Relation between reduction of foveal thickness and visual acuity in diabetic macular edema treated with intravitreal triamcinolone. Am J Ophthalmol, 139; 2005 : 802–806.
19. Lee, GW., Ahn, AK., Park, YG.: Intravitreal triamcinolone reduces the morphologic changes of ciliary body after pars plana vitrectomy for retinal vascular diseases. Am J Ophthalmol, 145; 2008 : 1037–1044.
20. Lewis, H., Abrams, GW., Blumenkraz, MS. et al.: Vitrectomy for diabetic macular traction and edema associated with posterior hyaloid traction. Ophthalmology, 99; 1992 : 753–759.
21. Maeda, N., Tano, Y.: Intraocular oxygen tension in eyes with proliferative diabetic retinopathy with and without vitreous. Graefes. Arch. Clin. Exp. Ophthalmol., 234 (Suppl I); 1996: S66–S69.
22. Mayer, C.: Current treatment approaches in diabetic macular edema. Ophthalmologica, 221; 2007 : 118–131.
23. Nguyen, QD., Shah, SM., Van Anden, E. et al.: Supplemental oxygen improves diabetic macular edema: a pilot study. Invest Opthalmol Vis Sci, 45; 2004 : 617–624.
24. Pendergast, SD., Hassan, TS., Williams, GA. et al.: Vitrectomy for diffuse diabetic macular edema associated with a taut premacular posterior hyaloid. Am J Opthalmol, 130; 2000 : 178–186.
25. Sebag, J., Buckingham, B., Charles, MA. et al.: Biochemical abnormalities of vitreous in humans with proliferative diabetic retinopathy. Graefes Arch Clin Exp Ophthalmol, 110; 1992 : 1472–1476.
26. Sebag, J.: Vitreous anatomy and vitreomacular interface. Boston, Butterworth–Heinemann, 1998: s. 1–23.
27. Shah, SP., Patel, M., Thomas, D., et al.: Factors predicting outcome of vitrectomy for diabetic maculatr edema: results of prospective study. Br J Ophthalmol, 90; 2006 : 33–36.
28. Steffanson, E.: Physiology of vitreous surgery. Graefes Arch Clin. Exp. Opthalmol., 247; 2009 : 147–163.
29. Steffanson, E.: The therapeutic effects of retinal laser treatment and vitrectomy: a theory based on oxygen and vascular physiology. Acta Ophthalmol Scand, 79; 2001 : 435–440.
30. Stolba, U., Binder, S., Gruber, D. et al.: Vitrectomy for persistent diffuse diabetic macular edema. Am J Ophthalmol, 140; 2005 : 295–301.
31. Tachi, N., Ogino, N.: Vitrectomy for diffuse macular edema in cases of diabetic retinopathy. Am J Ophthalmol, 122; 1996 : 258–260.
32. Yamamoto, T., Akabane, N., Takeuchi, S.: Vitrectomy for diabetic macular edema: The role of posterior vitreous detachment and epimacular membrane. Am J Ophthalmol, 132; 2001 : 369–377.
33. Yanyali, A., Nohatcu, AG., Horozoglu, F. et al.: Modified grid laser photocoagulation versus pars plana vitrectomy with internal limiting membrane removal in diabetic macular edema. Am J Ophthalmol, 139; 2005 : 795–801.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2012 Issue 5-
All articles in this issue
- Ranibizumab in the ARMD Wet Form Treatment – Two Years Results Obtained from the AMADEuS Registry
- Pars Plana Vitrectomy and Combination Therapy Pars Plana Vitrectomy, Intravitreal Triamcinolon Acetonid and Macular Lasercoagulation – One Year Results
- Clinical Variability of Best’s Disease
- The Current State of the Evidence of Malignant Tumors of the Eye and its Adnexa (dg. C69) in the Slovak Republic and in the Czech Republic
- Adjustable Versus Non-adjustable Sutures in Strabismus Surgery in Patients with Thyroid Ophthalmopathy
- The Application of Dysport® – the Possibilities of the Side Effect on the Eyelids Position (a Clinical – Histological study)
- Transnasal Endoscopic Surgery Approach in Intraorbital Tumors
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Clinical Variability of Best’s Disease
- The Application of Dysport® – the Possibilities of the Side Effect on the Eyelids Position (a Clinical – Histological study)
- Pars Plana Vitrectomy and Combination Therapy Pars Plana Vitrectomy, Intravitreal Triamcinolon Acetonid and Macular Lasercoagulation – One Year Results
- Adjustable Versus Non-adjustable Sutures in Strabismus Surgery in Patients with Thyroid Ophthalmopathy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career