-
Medical journals
- Career
Neurosarkoidóza: zriedkavý prípad sarkoidózy krčnej miechy – kazuistika
Authors: E. Kantorová 1; E. Kurča 1; J. De Riggo 2; J. Šutovský 2; J. Michalik 1; V. Nosáľ 1; E. Rozborilová 3; J. Hamžík 4; M. Hladká 5; J. Plank 6
Authors‘ workplace: Neurologická klinika JLF UK a MFN 1; Neurochirurgické oddelenie MFN 2; Klinika tuberkulózy a pľúcnych chorôb JLF UK a MFN 3; Chirurgická klinika JLF UK a MFN 4; Rádiodiagnostická klinika JLF UK a MFN 5; Ústav patologickej anatómie JLF UK a MFN 6
Published in: Cesk Slov Neurol N 2008; 71/104(5): 588-591
Category: Case Report
Overview
Sarkoidóza je granulomatózne ochorenie nie presne známej etiológie. Najčastejšie postihuje pľúca a lymfatické uzliny, zriedkavejšie oko, kostnú dreň, centrálny a periférny nervový systém, obličky, pečeň, srdce a svaly. Patomorfologicky ide o ložiská zložené z lymfocytov a mononukleárnych fagocytujúcich buniek obkolesujúcich nekazeózne epiteloidné bunky granulómov. Postihnutie nervového systému sa vyskytuje v 5–15 % prípadov sarkoidózy. Sarkoidóza krčnej miechy je zriedkavá a predstavuje podľa dostupných údajov 0,3–0,4 % prípadov. Stanovenie diagnózy neurosarkoidózy nie je obyčajne jednoduché. Ochorenie je terapeuticky dobre ovplyvniteľné steroidmi prípadne v kombinácii s inými imunosupresívnymi liekmi. Prognóza quoad vitam je dobrá, ale výsledný neurologický stav závisí od lokalizácie a veľkosti jazvy po prebehnutom granulomatóznom zápale. V práci autori opisujú kazuistiku pacienta s pravdepodobnou až istou diagnózou neurosarkoidózy krčnej miechy.
Kľúčové slová:
granulomatózne ochorenia – sarkoidóza – miechová lokalizácia sarkoidózyÚvod
Prevalencia sarkoidózy v Európe sa pohybuje medzi 3 až 60 prípadmi na 100 tis. obyvateľov. Najvyššia je v škandinávskych krajinách, kde je podľa rádiologických štúdií prevalencia udávaná nad 64 na 100 tis. obyvateľov, podľa autoptických nálezov je to až 641 na 100 tis. obyvateľov. V južnej Európe je najnižšia, 3–5/100 tis. obyvateľov. V USA je priemerná prevalencia 40 na 100 tis. obyvateľov, pričom Afroameričania majú 2–3-násobne vyššiu prevahu nad europoidnou populáciou USA. Prevalencia ochorenia v Afrike je okolo 40/100 tis. obyvateľov, prevahu majú ženy. V Ázii je sarkoidóza zriedkavá, s výnimkou Japonska. Podľa veľkých populačných štúdií je incidencia sarkoidózy u mužov 5,9 na 100 tis. za rok, ženy majú incidenciu 6,3 na 100 tis. [2].
Najčastejšie postihuje sarkoidóza dospelých (vek 25–50 rokov), vzácne sa vyskytuje aj v detskom veku a počas dospievania (vek 9–15 rokov). Ochorenie postihuje obidve pohlavia v rovnakej miere [1,2].
Podkladom sarkoidózy je pravdepodobne aberantná imunologická odpoveď organizmu, a to konkrétne v zložke tzv. IV. neskorého typu precitlivelosti. Po neidentifikovanom spúšťacom podnete (predpokladá sa infekčný agens) vzniká zvýšená produkcia polyklonových Th1 lymfocytov CD4 a po ich aktivácii a sekrécii vybraných cytokínov (napr. IL‑2, IL‑12, TNF‑alfa) dochádza k poškodeniu cieľových okrskov tkaniva [2,3]. Klinické prejavy sarkoidózy sú všeobecné (únava, slabosť, zníženie hmotnosti, zvýšená teplota, nočné potenie) a špecifické viazané na poruchu štruktúry a funkcie konkrétneho poškodeného orgánu alebo systému.
V literatúre sú rôzne diagnostické kritéria neurosarkoidózy. Podľa Zajicka et al je diagnóza neurosarkoidózy pravdepodobná v prípade, že ďalšie alternatívne diagnózy ako možné príčiny klinického obrazu vylúčia pomocné vyšetrenia (napr. komplexné imunologické vyšetrenie séra a likvoru vrátane hladiny ACE, MR vyšetrenie mozgu a miechy, CT vyšetrenie hrudníka, bronchoalveolárna laváž, Kweimov kožný test). Diagnózu neurosarkoidózy považujú za definitívnu po kladnom histopatologickom vyšetrení postihnutého nervového tkaniva [3,4]. V posledných rokoch sa objavili viaceré návrhy modifikovaných diagnostických kritérií, podľa ktorých pre stanovenie definitívnej diagnózy neurosarkoidózy postačuje histopatologické potvrdenie systémového granulomatózneho procesu spojeného s ložiskovým (viacložiskovým) neurologickým poškodením pri vylúčení iných príčin neuropatológie [5–10].
Kazuistika
Opisujeme prípad 36-ročného muža s anamnézou solitárneho kolapsového stavu po maratónskom behu pred piatimi rokmi. V posledných troch rokoch bol pacient sledovaný pneumoalergológom pre syndróm dráždivého kašľa. Pacient bol prijatý na neurologickú kliniku pre dva týždne trvajúce ťažkosti v zmysle zhoršenej chôdze a slabosti dolných končatín spojených s parestéziami dolných končatín pri chôdzi a neskôr aj v pokoji. Ťažkosti sa postupne zvýrazňovali a v čase prijatia na kliniku sa prejavila aj dyzúria s nevyhnutnosťou použiť brušný lis pri močení.
Objektívny neurologický nález ukázal normálnu funkciu kraniálnych nervov. Statika a dynamika krčného úseku osového orgánu bola normálna s výnimkou pacientom udávaného Lhermitteovho fenoménu pri predklone hlavy. Nález na horných končatinách bol fyziologický s výnimkou zvýšenej úrovne brachioradiálneho a styloradiálneho reflexu vpravo. Brušné a kostoabdominálne reflexy boli živé a stranovo symetrické. Reflex Achillovej šľachy mal zvýšenú úroveň obojstranne. Vpravo sme vyvolali podráždením tzv. Vítkovej zóny patologický Babinskiho extenčný pyramídový príznak, pričom vľavo bol prítomný fyziologický kožný plantárny reflex. Pri vyšetrení postoja sme zistili pozitívny Rombergov príznak a pri vyšetrení chôdze sme konštatovali ľahkú paraparézu dolných končatín s prevahou postihnutia vpravo.
MRI vyšetrenie mozgu a hlavy ukázalo normálny nález. MRI vyšetrenie krčného a hrudného úseku spinálneho kanála ukázalo (T2, STIR) hyperintenzívne intramedulárne ložisko vo výške C6 a C7 lokalizované centrálne a paracentrálne vľavo (obr. 1). Ložisko malo nepravidelný tvar a nasledovné rozmery (predozadný 9 mm, laterolaterálny 9 mm a kraniokaudálny 26 mm). Po podaní paramagnetickej kontrastnej látky sa ložisko nepravidelne sýtilo. Canalis centralis bol dilatovaný nad aj pod miestom patologického ložiska (kraniálne po úroveň dens axis a kaudálne do výšky Th4). Vedľajší nález predstavovali pakety lymfatických uzlín v mediastíne.
Image 1. MRI krčnej miechy (STIR, sagitálny rez) s rozsiahlym intramedulárnym hyperintenzívnym ložiskom. 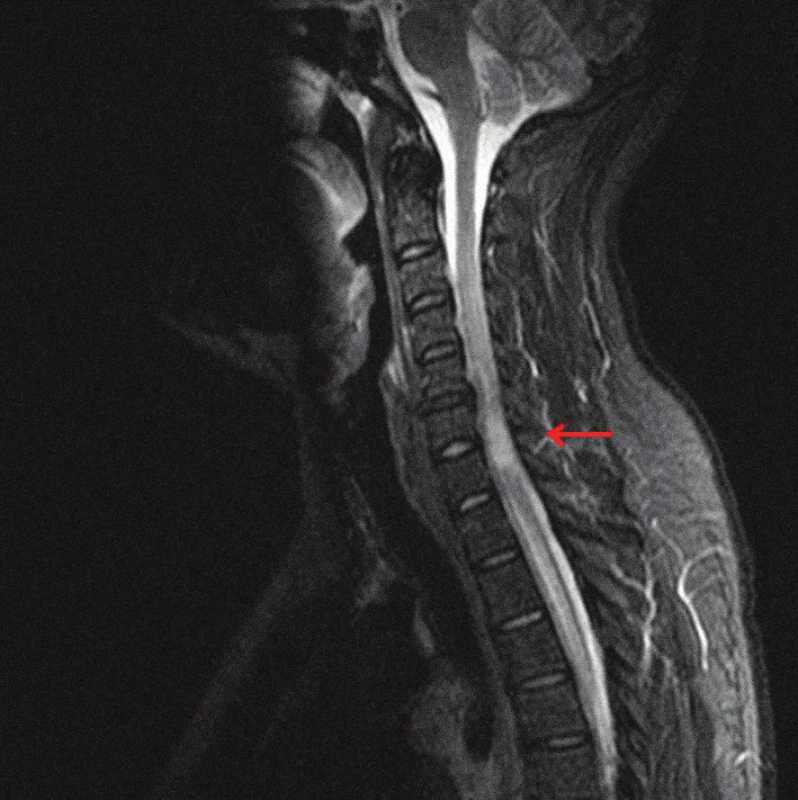
CT vyšetrenie hrudníka potvrdilo v mediastíne patologicky zväčšené lymfatické uzliny veľkosti 20–45 mm (paratracheálne, pod karinou, pred oblúkom aorty, v hiloch). Najväčšie lymfatické uzliny mali centrálny nekrotický okrsok. Po podaní kontrastnej látky dochádzalo k nehomogénnemu sýteniu zväčšených lymfatických uzlín. V pravom pľúcnom krídle ventrálne parakardiálne bol 5–6 mm veľký uzol vs fibrotického pozápalového charakteru a vpravo bazálne bola prítomná pleurodiafragmatická adhézia. CT vyšetrenie abdomenu a príslušného skeletu ukázalo normálny nález.
Vyšetrenie likvoru ukázalo ľahkú hyperproteinorrhachiu a ľahkú pleiocytózu (bielkoviny 0,663 g/l, 44/3 monocytov a lymfocytov). Hodnota prealbumínu, albumínu, alfa 1, alfa 2 a beta globulínu bola normálna. Celkový gamma globulín bol ľahko zvýšený na 13,5 (norma 5,6–11,4) pri zachovaní proporcionality jednotlivých podtried IgG, IgM a IgA. Prítomnosť oligoklonových a monoklonových pásov nebola v likvore dokázaná. Vyšetrenie kvalitatívneho cytosedimentu potvrdilo nízky počet pokojových foriem monocytov a lymfocytov bez prítomnosti ďalších buniek. Prietoková cytometria likvoru zameraná na imunofenotypové znaky buniek potvrdila zachovaný imunoregulačný index CD4/CD8 a vylúčila prítomnosť lymfoproliferatívneho ochorenia CNS.
Ďalšie laboratórne vyšetrenia priniesli nasledovné výsledky. Krvný obraz, glykémia, mineralogram, hepatálne testy, markery renálnych funkcií a vyšetrenie moča boli normálne. Celkové bielkoviny, ELFO bielkovín vrátane podtried gamma globulínu IgG, IgM a IgA boli v pásme referenčných hodnôt. Prítomnosť paraproteínu v sére nebola dokázaná. Prietoková cytometria krvi ukázala ľahkú lymfopéniu a zníženie absolútnych počtov lymfocytov CD4, CD3 a CD8 ako aj NK buniek. Imunoregulačný index CD4/CD8 bol zachovaný. FW po dvoch hodinách bola 19/38, mukoproteíny v sére 416 a vysoko senzitívny CRP a cirkulujúce imunokomplexy v sére boli v norme. ANA, ANCA a všetky vyšetrené orgánové autoprotilátky boli negatívne. Serologické vyšetrenie krvi a likvoru na prítomnosť protilátok proti B. burgdorferi, Ch. trachomatis, Ch. pneumoniae, HSV1, HSV2, VZV, CMV bolo rovnako negatívne. Taktiež TPHA test v sére a likvore a kožný Mantoux test boli negatívne.
Vyšetrenia VEP, BAEP a SEP pri stimulácii nn. mediani boli fyziologické. Vyšetrenie SEP pri stimulácii nn. tibiales potvrdilo ľahkú léziu demyelinizačného typu centrálneho úseku somatosenzitívnej dráhy pri stimulácii vpravo. Kondukčné štúdie n. fibularis, n. tibialis (vrátane F odpovedí a H reflexu n. tibialis), n. plantaris medialis a n. suralis vpravo ukázali fyziologický nález.
Torakoskopicky bol vykonaný odber patologicky zväčšenej lymfatickej uzliny z mediastína. Histopatologickým vyšetrením bol dokázaný granulomatózny zápalový proces typu sarkoidózy.
Pacient bol liečený steroidmi podľa odporučení v literatúre [8,10–12]. Po pulznej liečbe metylprednisolonom vnútrožilovo v dávke 4,5 g nasledovala perorálna terapia prednizonom v dávke 40 mg denne v trvaní päť mesiacov. Potom sme začali dennú dávku postupne znižovať. Súčasná udržiavacia dávka je 10 mg prednizonu obdeň. Po vnútrožilovej liečbe ustúpila slabosť dolných končatín a porucha močenia. Pretrvával ešte pocit pálenia dolných končatín. V priebehu niekoľkých týždňov úplne vymizli všetky subjektívne príznaky ochorenia a súčasne došlo k normalizácii objektívneho neurologického nálezu. Kontrolné MRI vyšetrenie potvrdilo regresiu ložiskového procesu v krčnej mieche (obr. 2). Kontrolné vyšetrenie SEP pri stimulácii nn. tibiales ukázalo fyziologický nález rovnako ako MEP z dolných končatín vyvolané transkraniálnou magnetickou stimuláciou. Pacient ukončil práceneschopnosť a vrátil sa do zamestnania.
Image 2. MRI krčnej miechy (STIR, sagitálny rez) s regresiou ložiska. po pulznej vnútrožilovej liečbe metylprednizolonom. 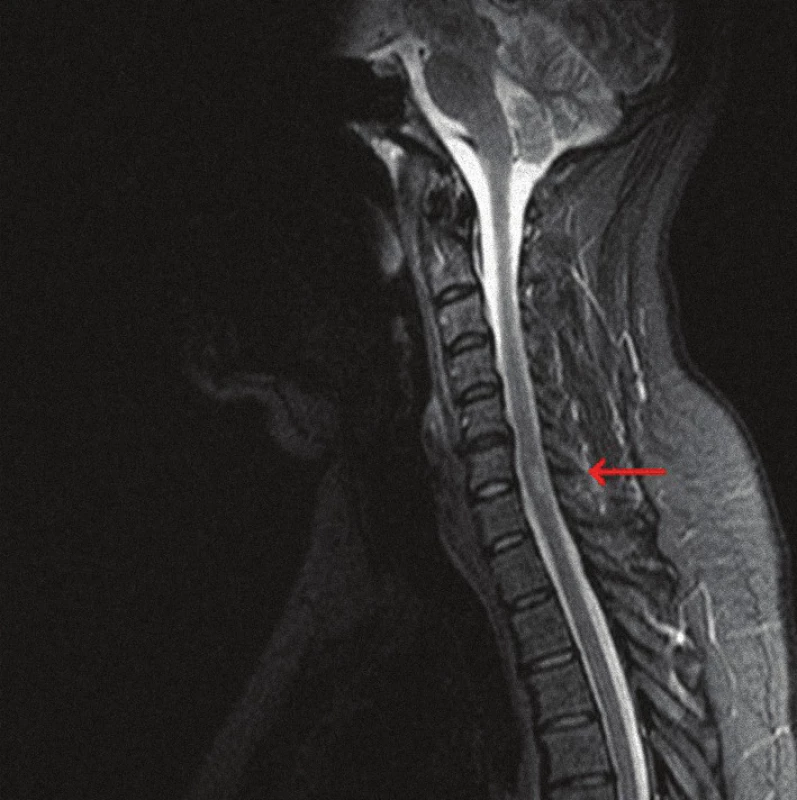
Diskusia
V diagnostickej rozvahe sme v prvom rade uvažovali o nádorovom alebo zápalovom procese. Vyšetrenie likvoru nepotvrdilo lymfoproliferatívne ochorenie a charakter ložiskového procesu v MR obraze pri kontrolných vyšetreniach rovnako nesvedčil pre primárny alebo sekundárny nádor CNS. Pomocné vyšetrenia nesvedčili ani pre demyelinizačné ochorenie CNS, transverzálnu myelitídu, infekčné ochorenie CNS alebo pre paraneoplastický etiopatomechanizmus. Histopatologickým vyšetrením mediastinálnej lymfatickej uzliny sme dokázali pľúcnu formu sarkoidózy a nateraz považujeme aj ložiskový proces v krčnej mieche za extrapulmonálny prejav detegovaného základného ochorenia – spinálnu neurosarkoidózu. Terapeutická odpoveď na liečbu steroidmi a ďalší vývoj klinického stavu spolu s výsledkami kontrolných pomocných vyšetrení (MRI, klinická neurofyziológia) nám umožňujú vysloviť tento diagnostický záver. Je pochopiteľné, že bioptické vyšetrenie ložiskového procesu krčnej miechy pre stanovenie definitívnej diagnózy neurosarkoidózy je v danej lokalizácii problémové a môže znamenať potenciálne iatrogénne poškodenie pacienta. Pacient tento diagnostický výkon aj odmietol.
Záverom konštatujeme, že spinálna neurosarkoidóza je zriedkavá nozologická jednotka, ktorá ale rozhodne patrí do diagnostickej rozvahy pri riešení ložiskových alebo ložiskovo-difúznych miechových procesov. Upozorňujeme aj na skutočnosť, že v určitých prípadoch nie je možné stanoviť definitívnu diagnózu podľa tradičných diagnostických kritérií, ale je nevyhnutné sa uspokojiť s diagnózou pravdepodobnou, resp. s naplnením navrhnutých upravených diagnostických kritérií neurosarkoidózy.
MUDr. Ema Kantorová
Neurologická klinika
JLF UK a MFN
Kollárova 2
036 59 Martin
e‑mail: ekantorova@marticonet.sk
Prijato k recenzii: 2. 4. 2008
Prijato do tlače: 18. 7. 2008
Sources
1. Hoitsma E, Faber CG, Drent M, Sharma OP. Neurosarcoidosis: a clinical dilemma. Lancet Neurol 2004; 3(7): 397–407.
2. Shetty AK, Gedalia A. Sarcoidosis: a pediatric perspective. Clin Pediatr (Phila) 1998; 37(12): 707–717.
3. Zajicek JP, Scolding NJ, Foster O, Rovaris M, Evanson J, Moseley IF et al. Central nervous system sarcoidosis – diagnosis and management. QJM 1999; 92(2): 103–117.
4. Zajicek JP. Neurosarcoidosis. Curr Opin Neurol 2000; 13(3): 323–325.
5. Toth C, Martin L, Morrish W, Coutts S, Parney I. Dramatic MRI improvement with refractory neurosarcoidosis treated with infliximab. Acta Neurol Scand 2007; 116(4): 259–262.
6. Sakuta M, Kumamoto T, Iizuka T, Nishiyama K, Oritsu M. Diagnostic criteria of neurosarcoidosis. No To Shinkei 2006; 58(6): 471–476.
7. Kolek V, Penicková V, Herman M, Gronych B,Houdek M. Neurosarcoidosis. Role of new examination methods for early diagnosis and therapy. Čas Lék česk 1996; 135(5): 141–144.
8. Patel AV, Stickler DE, Tyor WR. Neurosarcoidosis. Curr Treat Options Neurol 2007; 9(3): 161–168.
9. Caneparo D, Lucetti C, Nuti A, Cipriani G, Tessa C, Fazzi P et al. A case of sarcoidosis presenting as a non‑specific intramedullary lesion. Eur J Neurol 2007; 14(3): 346–349.
10. Stern BJ. Neurological complications of sarcoidosis. Curr Opin Neurol 2004; 17(3): 311–316.
11. Marangoni S, Argentiero V, Tavolato B. Neurosarcoidosis. Clinical description of 7 cases with a proposal for a new diagnostic strategy. J Neurol 2006; 253(4): 488–495.
12. Scott TF, Yandora K, Valeri A, Chieffe C,Schramke C. Aggressive therapy for neurosarcoidosis: long‑term follow‑up of 48 treated patients. Arch Neurol 2007; 64(5): 691–696.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2008 Issue 5-
All articles in this issue
- Neurologické poruchy v rámci kritického stavu
- Matrixové metaloproteinázy v patogenezi roztroušené sklerózy
- Současná diagnostika a léčba oligodendrogliomů
- Význam monitorování mozkové aktivity pomocí integrované amplitudy EEG aktivity u novorozenců s časným asfyktickým syndromem
- Pravo/levorukost a preference druhostranné dolní končetiny. Testování laterality a mozečkové dominance
- Traumatické poranění mozku a zlomeniny obličejového skeletu
- Radiochirurgická léčba kraniofaryngeomů v kombinaci s ostatními stereotaktickými metodami
- Kombinované poranění atlasu a čepovce
- Míšní metastáza adenokarcinomu – kazuistika
- Neurosarkoidóza: zriedkavý prípad sarkoidózy krčnej miechy – kazuistika
- Intradurální výhřez bederní meziobratlové ploténky manifestující se syndromem kaudy – kazuistika
- Mozková gliomatóza – kazuistika
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Neurologické poruchy v rámci kritického stavu
- Intradurální výhřez bederní meziobratlové ploténky manifestující se syndromem kaudy – kazuistika
- Současná diagnostika a léčba oligodendrogliomů
- Traumatické poranění mozku a zlomeniny obličejového skeletu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

