-
Medical journals
- Career
Včasní nonrespondéri pri liečbe teriparatidom: retrospektívna analýza
Authors: Masaryk Pavol; Letkovská Alexandra
Authors‘ workplace: Národný ústav reumatických chorôb, Piešťany
Published in: Clinical Osteology 2020; 25(1): 45-49
Category:
Overview
Teriparatid (TPTD) je účinný osteoanabolický liek. Potenciálnou nevýhodou spojenou s liečbou teriparatidom je zlyhanie účinku. Výskyt nonrespondérov závisí od definície nedostatočnej odpovede na liečbu, vstupnou hustotou kosti, trvaním liečby, predchádzajúcou antiresorpčnou liečbou a presnosťou merania. V našej štúdii sme analyzovali tzv. včasných nonrespondérov po 6 a 12 mesiacoch liečby v súbore 306 pacientov. Ako včasných nonrespondérov sme identifikovali 36 (11,7 %) pacientov, z toho 18 po 6 mesiacoch liečby a 18 po roku liečby. V súbore boli len 4 muži a až 32 žien, ale percentuálne zastúpenie nonrespondérov medzi pohlaviami bolo približne rovnaké (muži 10,5 %, ženy 11,9 %). Výrazne viacej boli zastúpení včasní nonrespondéri u glukokortikoidovej osteoporózy. Predchádzajúca antiresorpčná liečba, hlavne bisfosfonátmi, zvyšovala riziko nedostatočnej odpovede na liečbu teriparatidom.
Klíčová slova:
nonrespondéri – teriparatid
Úvod
Liečba osteoporózy v súčasnosti zahŕňa lieky s antiresorpčným účinkom a lieky s osteoanabolickým efektom. Parathormón alebo jeho amino-terminálne fragmenty a analógy zabraňujú, zastavujú alebo čiastočne revertujú úbytok kostí u zvierat a ľudí v závislosti od formy aplikácie [1,2]. Teriparatid (rekombinantný ľudský paratyroidný hormón – PTH) je rekombinantná molekula zložená z 34 aminokyseliny amino-terminálneho konca ľudského PTH. V pulznej aplikácii má osteoanabolický efekt [3].
V základnej registračnej štúdii Neera et al teriparatid znižoval relatívne riziko nových zlomenín stavcov o 65 % a nonvertebrálnych zlomenín o 53 %. V porovnaní s placebom dávky parathormónu 20 μg a 40 μg hormónu zvýšili kostnú minerálnu hustotu o 9–13 % v bedrovej chrbtici a o 3–6 % v stehennej kosti [4].
Potenciálnou nevýhodou spojenou s liečbou TPTD je zlyhanie účinku. Gallagher et al definovali dobrú odpoveď na liečbu TPTD minimálnym zvýšením hustoty kostného minerálu (BMD – Bone Mineral Density) bedrovej chrbtice od východiskovej hodnoty o 3 %. V jeho analýze liečby TPD 20 a 40μg/deň sa potom dobrá odpoveď pohybovala od 87 do 94 % [5]. Autori však neboli schopní zistiť žiadne rozdiely v základných charakteristikách medzi pacientmi, ktorí odpovedali, a tými, ktorí odpovedali nedostatočne. Heaney et al v ďalšej štúdii zistili, že miera odpovede na TPTD môže byť variabilnejšia a do istej miery nižšia, s pozitívnou odpoveďou BMD 82,5 % v oblasti bedrovej oblasti chrbtice a 44,8 % v oblasti total femur [6].
Vzhľadom na to, že liečba TPTD je spojená s vysokými nákladmi, je popri indikačných obmedzeniach dôležité identifikovať prediktory zlyhania liečby [7].
Teriparatid na Slovensku
Teriparatid je na Slovensku registrovaný od roku 2003. Jeho účinnosť bola dokumentovaná viacerými štúdiami aj empiricky [8,9].
TPTD na Slovensku má prísne indikačné a preskripčné obmedzenia s dĺžkou podávania maximálne 18 mesiacov. Liečba u pacientov s postmenopauzálnou osteoporózou a osteoporózou u mužov je indikovaná v prípadoch, v ktorých T-skóre femoru je < -2,9 a súčasne sú prítomné aspoň 2 zlomeniny stavcov, alebo došlo k zlyhaniu doterajšej 2-ročnej antiresorpčnej liečby, t. j. objavila sa nová zlomenina, alebo sa zaznamenal pokles BMD femoru ≥ 6 %. U glukokortikoidovej osteoporózy je nutná liečba prednisonom (či jeho ekvivalentom) v dávke > 5 mg po dobu > 3 mesiace a súčasne je prítomná aspoň jedna osteoporotická zlomenina, alebo T-skóre < -2,9 na chrbtici, alebo femore. Liečba je vyhradená len pre 5 osteocentier (Univerzitná nemocnica Bratislava-Ružinov, NURCH Piešťany, Fakultná nemocnica Banská Bystrica, NEDU Ľubochňa, Nemocnica Košice-Šaca). Liečba TPD je tiež prísne monitorovaná v 6-mesačných intervaloch, a pokiaľ sa zistí nedostatočný efekt, nie je liečba ďalej poisťovňou hradená. Za dostatočnú odpoveď na liečbu po 6 mesiacoch sa považuje vzostup markera osteoformácie viacej ako 20 % a za dostatočnú odpoveď po 12 mesiacoch preukázané zastavenie poklesu BMD. V opačnom prípade sa liečba ukončuje a takýchto pacientov je možno považovať za „včasných“ nonrespondérov.
Cieľom našej štúdie bolo analyzovať výskyt včasných nonrespondérov v našom súbore pacientov a identifikovať faktory, ktoré predikujú včasnú nedostatočnú odpoveď na liečbu TPTD.
Súbor pacientov
V našej práci ide o retrospektívnu analýzu časti pacientov Osteocentra NURCH Piešťany.
Do analýzy bolo zaradených 306 pacientov, ktorým bol v rokoch 2006–2018 podávaný teriparatid v dávke 20 μg/deň s.c., z toho bolo 38 mužov a 268 žien. Indikáciami boli závažná postmenopauzálna osteoporóza u žien (172 pacientok), závažná osteoporóza u mužov (16 pacientov) a glukokortikoidmi indukovaná osteoporóza (118 pacientov).
Včasní nonrespondéri boli definovaní nasledovne: Nonrespondéri po 6 mesiacoch: vzostup markera osteoformácie (osteokalcin, alebo PINP – N-terminálny fragment prokolagénu typu I) < 20 %, nonrespodnéri po 12 mesiacoch: pokles BMD o LSC (na našom pracovisku: L1–L4 3,06 %,. total neck: 3,49 %). Analyzovali sme spoločne celú skupinu včasných nonrespondérov.
Súbor sme analyzovali podľa pohlavia, veku, indikácie liečby, vstupných parametrov fosfokalciového metabolizmu, kostnej denzity, prevalentných zlomenín a predchádzajúcej antiporotickej liečby. Analýzu podľa markerov kostného metabolizmu sme nemohli vykonať, keďže sme pracovali s údajmi od odosieľajúcich lekárov s rôznymi laboratórnymi metódami. Na analýzu kontinuálnych parametrov sme použili nepárový t-test a pre analýzu kategoriálnych parametrov χ2-test.
Výsledky
V tab. 1 sú základné antropometrické charakteristiky celého súboru 306 pacientov rozdelených podľa pohlavia., v tab. 2. je rozdelenie súboru podľa typu osteoporózy.
Table 1. Antropometrické charakteristiky súboru podľa pohlavia: priemer + SD (min–max) 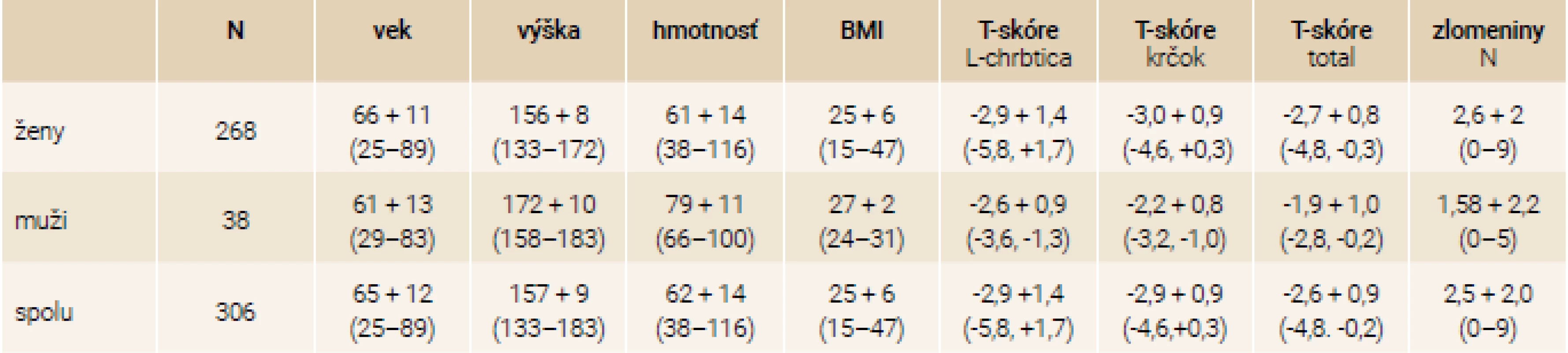
Table 2. Antropometrické charakteristiky súboru podľa typu osteoporózy: priemer + SD (min–max) 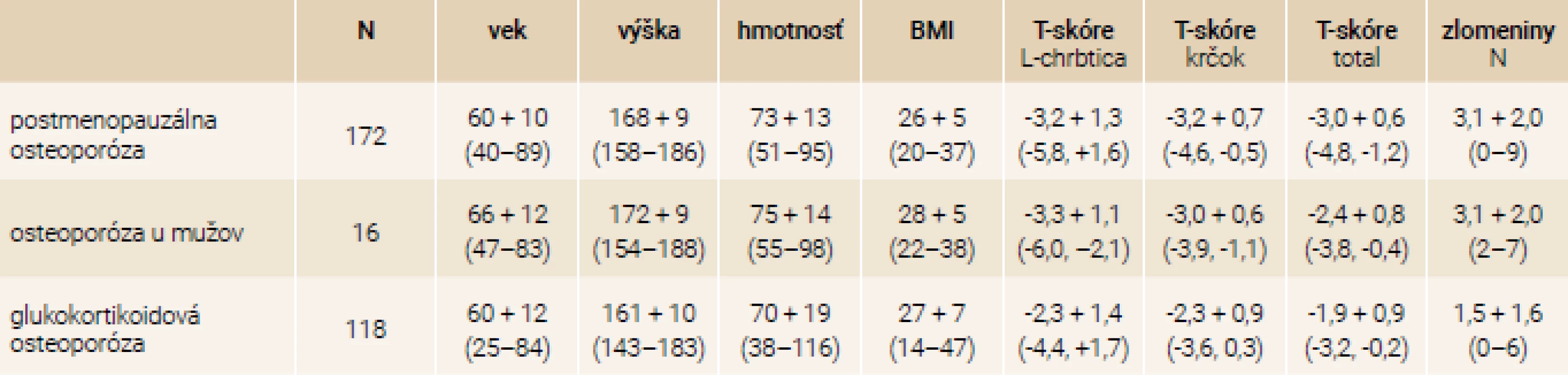
Terapiu TPD v plnej dĺžke 18 mesiacov ukončilo 226 pacientov. Nonrespondérov (zlepšenie BMD chrbtice <3 %) bolo 7 (3,1 %). Predčasne ukončilo liečbu 80 pacientov.
Dôvody predčasného ukončenia boli nasledovné: úmrtie 11 pacientov, intolerancia lieku 17 pacientov, odmietnutie pokračovať 7 pacientov, iné 9 pacientov, včasní nonrespondéri 36 pacientov, z toho 18 po 6 mesiacoch liečby a 18 po roku liečby.
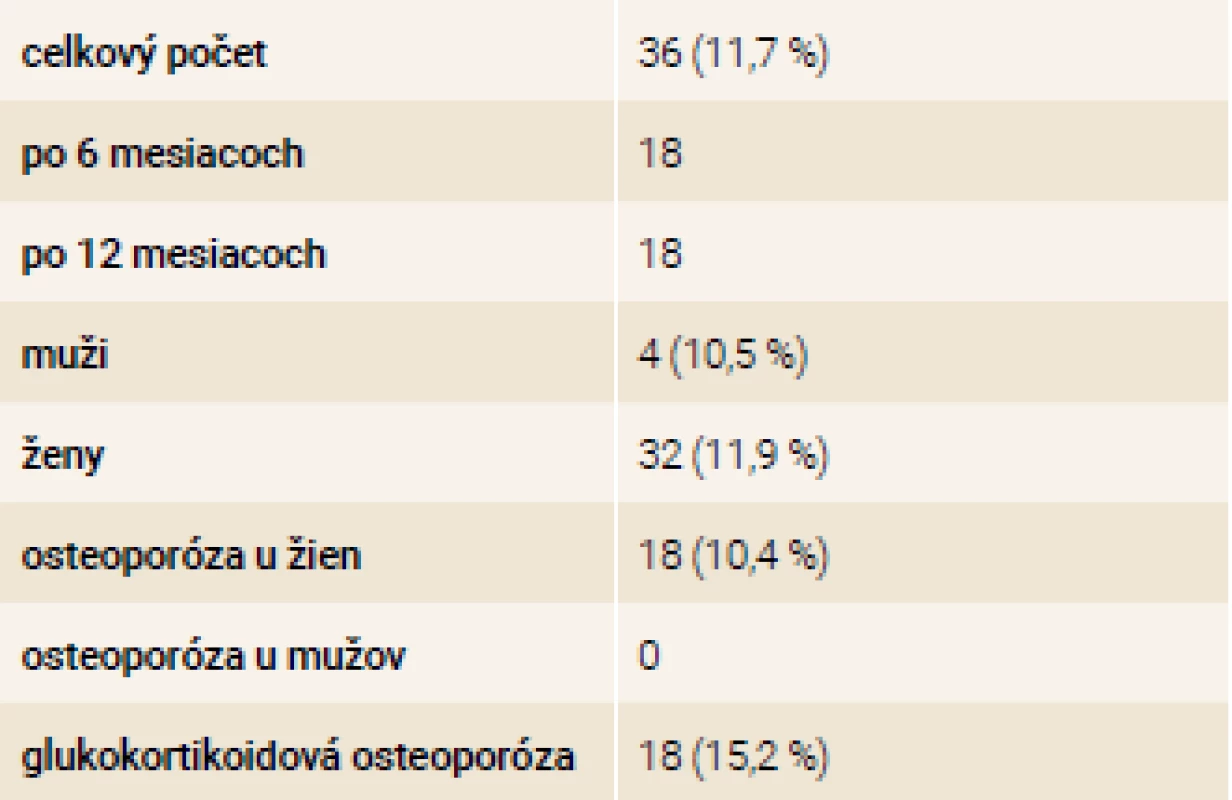
V tab. 3. sú základné údajne o včasných nonrespondéroch. Tvorili 11,7 % súboru pacientov, ktorí ukončili liečbu. V súbore boli len 4 muži a až 32 žien, ale percentuálne zastúpenie nonrespondérov medzi pohlaviami bolo približne rovnaké ( muži 10,5 %, ženy 11,9 %). Výrazne viacej boli zastúpení včasní nonrespondéri u glukokortikoidovej osteoporózy.
V tab. 4 je analýza prediktorov nedostatočnej odpovede podľa jednotlivých parametrov veku, výšky hmotnosti, kostnej denzity, počtu zlomenín a fosfokalciového metabolizmu a predchádzajúcej liečby. Včasní nonrespondéri mali signifikantne vyššiu hmotnosť, mali menej prevalentných zlomenín a boli častejšie liečení bisfosfonátmi. Nižší výskyt prevalentných zlomenín zrejme súvisí s vyšším zastúpením nonrespondérov v glukokortikoidovej skupine, v ktorej indikácia liečby TPTD nevyžaduje nutne prítomnosť zlomeniny.
Table 4. Prediktory nedostatočnej odpovede 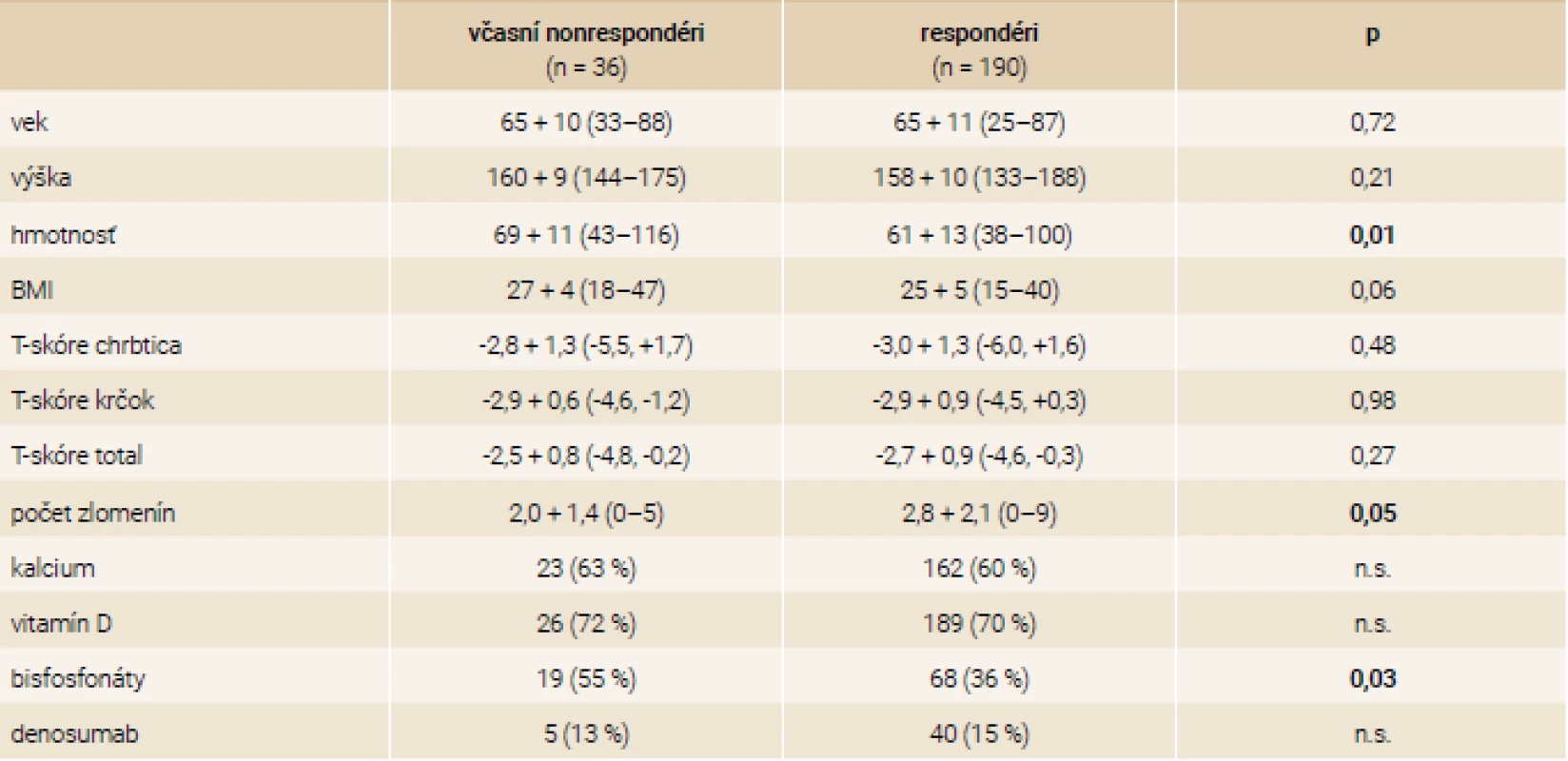
Diskusia
V dostupnej literatúre sme nenašli žiadnu štúdiu o „včasných nonrespondéroch“ pri liečbe TPTD. Všetky dostupné štúdie hodnotia výskyt nonrespondérov po ukončení štúdie, t. j. po 12–24 mesiacoch. Jednotlivé štúdie definujú nonrespondérov rôzne a pracujú s rôzne definovanými základnými súbormi, čo do počtu, ale aj závažnosti osteoporózy.
Minne et al v štúdii EUROFORS (EUROpean study of FORSteo) analyzovali efekt ročnej liečby TPTD u pacientov s manifestnou osteoporózou, rozdelených na 3 skupiny pacientov: dovtedy neliečení (n = 204) , predchádzajúca antiresorpčná liečba (prevažne bisfosfonáty/n = 240) a pacienti so zlyhaním predchádzajúcej liečby (n = 421). BMD chrbtice vzrástlo u všetkých 3 skupín (8,2 %, 7,1 %, 6,2 %), avšak BMD femoru vzrástla len u naivných (+1,8 %), u osôb s predchádzajúcou liečbou sa signifikantne nemenila (+0,4 %,resp. -0,3 %) [10].
Elraiyah et al vykonali retrospektívnu štúdiu liečby TPTD u 494 pacientov s osteopéniou alebo osteoporózou. Za zlyhanie liečby považovali výskyt osteoporotickej zlomeniny po 6 mesiacoch liečby, alebo vzostup BMD chrbtice či femoru < 3 % po 12 mesiacoch liečby. V ich súbore 35 pacientov (7,1 %) utrpelo osteoporotickú zlomeninu 172 (34,8 %) pacientov a nedosiahlo terapeutickú odpoveď BMD > 3 %. Predchádzajúca liečba bisfosfonátmi a vitamínom D boli signifikantnými prediktormi nedostatočnej odpovede. Nezaznamenali žiadne rozdiely medzi respondérmi a nonrespondérmi v antropometrických parametroch, sprievodných ochoreniach a vstupných hodnotách kostných markerov [7].
Niimi et al analyzovali výskyt nonrespondérov v súbore 354 japonských žien a mužov liečených počas 2 rokov TPTD. Indikácia liečby podliehala japonským kritériám a zahŕňala 4 rôzne kombinácie zníženej kostnej denzity, veku a počtu zlomenín. Do analýzy nebolo zaradených 277 pacientov, ktorí nedokončili 2-ročnú liečbu. Nonrespondéri boli definovaní pri vzostupe BMD chrbtice < 3 %. V tomto súbore popísali 42 (11,8 %) nonrespondérov. V skupine nonrespondérov sa vyskytlo 6 (14,2 %) klinických zlomenín oproti 17 (5,4 %) zlomeninám u respondérov. Priemerná zmena BMD chrbtice u nonrespondérov bola -0,8 % , oproti +15,1 % u respondérov, a BMD femoru u nonrespondérov bola -1,1%, oproti +4,2 % u respondérov. BMD chrbtice aj femoru boli merané v 4-mesačných intervaloch, u respondérov kontinuálne stúpala, kdežto u nonrespondérov sa prakticky nemenila. Kostné markery sPINP a uNTX stúpali u oboch skupín, aj keď u nonrespondérov niečo menej, ale nie signifikantne. Takže sa vlastne nedá hovoriť o skutočných nonresponedérov! Ako prediktory zlej odpovede boli v univariačnej analýze zistené: predchádzajúca liečba bisfosfonátmi, nizky sPINP a uNTx, čo sa však v multivariačnej analýze nepotvrdilo [11].
Kim et al tiež definovali nonrespodérov ako pacientov, ktorých zlepšenie BMD L-chrbtice nedosiahlo 3 % . V súbore 78 osteoporotických pacientov liečených TPTD počas 18–24 mesiacov našli 13 (16,7 %) nonrespondérov. Nenašli žiadne signifikantné prediktory nedostatočnej odpovede na liečbu TPTD. Hoci zistili signifikantne vyššie hladiny BSAP po 4 mesiacoch u pacientov, ktorí neodpovedajú na TPTD, po 24 mesiacoch už neboli žiadne významné rozdiely medzi respondérmi a nonrespondérmi. Zvýšenie markerov vo včasných fázach liečby TPD ešte nemusí znamenať dobrú odpoveď na liečbu [12].
Premenopauzálne ženy s idiopatickou osteoporózou (IOP) majú abnormálnu kortikálnu a trabekulárnu mikroarchitektúru. Cohen et al podávali TPTD u 21 premenopauzálnych žien 18–24 mesiacov. BMD sa zvýšila v chrbtici o 10,8 %, total o 6,2 % a krčku stehennej kosti o 7,6 %. Výskyt nonrespondérov bol 4 (19 %), ktorí nereagovali vzostupom BMD, a nárast PINP a CTx bol u nich nižší ako u respondérov. Ako prediktory autori identifikovali nižšie bazálne hodnoty CTx a osteokalcínu a zvýšené hodnoty IGF [13].
Nízky výskyt nonrespondérov v našom súbore (3 %) je evidentne spôsobený preselekciou, t. j. vylúčením včasných nonrespondérov. Nemali sme síce možnosť zistiť, ako by včasní nonrespondéri reagovali na pokračovanie liečby a aký by bol výsledný efekt po uplynutí celej možnej doby liečby 18 mesiacov, ale zo štúdie Nimiho et al vyplýva, že pokračovanie liečby u týchto včasných nonrespondérov by zrejme neviedlo k dobrej odpovedi ani po 18 mesiacoch.
Negatívny efekt predchádzajúcej liečby bisfosfonátmi popísali už Ettinger et al. Porovnávali efekt liečby TPD na kostné markery po predchádzajúcej liečbe raloxifenom (RLX) a alendronátom (ALN). Liečba TPTD stimulovala kostný obrat u pacientov liečených RLX aj ALN. Predchádzajúca liečba RLX vykazovala očakávané zvýšenie BMD vyvolané TPTD porovnateľné so zvýšením u pacientov predtým neliečených. Naproti tomu predchádzajúca liečba ALN bránila najmä zvýšeniu BMD v prvých 6 mesiacoch [14].
Je možné, že predchádzajúca liečba bisfosfonátmi suprimuje kostný metabolizmus, a tým zhoršuje parametre kostných markerov počas liečby, ev. oneskoruje nástup terapeutickej odpovede. Prakticky je teda treba upozorniť indikujúcich lekárov, ale aj pacientov na potenciálne nebezpečenstvo včasného zlyhania liečby u pacientov na predchádzajúcej liečbe bisfosfonátmi. Na druhej strane to môže byť aj potvrdenie, že osteoanabolická liečba by mala byť liekom prvej voľby, aby sa mohol plne využiť jej potenciál v budovaní kostnej hmoty a následná antiresorpčná liečba by takto získanú hmotu udržiavala.
Podobne ako Heaney et al aj Nimmi et al sú presvedčení, že nepresnosť merania je ďalší dôvod nedostatočnej odpovede BMD na liečbu. V ich štúdii 34 z 42 (81 %) pacientov, ktorí nereagovali na liečbu po 24 mesiacoch, vykázali ≥ 3% zvýšenie LS BMD po 20 mesiacoch. To znamená, že niektorí pacienti mohli byť klasifikovaní ako nereagujúci v dôsledku nepresností merania [6,11].
TPTD môže stimulovať novotvorbu kosti na endosteálnych aj periosteálnych povrchoch, čím sa zvyšuje kortikálny priemer, čo môže byť ďalším dôvodom, ktorý vysvetľuje, prečo môže byť odpoveď BMD femoru pri liečbe TPTD nedostatočná. Predpokladá sa, že mechanizmus, ktorý je podkladom prechodného poklesu BMD femoru, môže byť spojený s periosteálnou apozíciou novosyntetizovanej, čiastočne mineralizovanej kosti, a to sa môže javiť ako strata BMD [15,16]. Z toho pohľadu môže byť monitorovanie odpovede na liečbu TPTD pomocou BMD femoru problematické.
Záver
Terapeutická odpoveď pri liečbe TPD bola v našom súbore veľmi dobrá. Výskyt nonrespondérov po 18 mesiacoch liečby bol len 3% pri 11,7 % včasných nonrespondéroch. Monitorovanie liečby po 6 a 12 mesiacoch umožňuje eliminovať včasných nonrespondérov, a tým zvýšiť efektivitu liečby. Predchádzajúca antiresorpčná liečba, hlavne bisfosfonátmi, zvyšuje riziko nedostatočnej odpovede na liečbu teriparatidom, hlavne pri glukokortikoidovej osteoporóze.
MUDr.Pavol Masaryk, PhD. | pavol.masaryk@nurch.sk | www.nurch.sk
Received | Doručené do redakcie | Doručeno do redakce 19. 3. 2020
Accepted | Prijaté po recenzii | Přijato po recenzi 1. 6. 2020
Received | Doručeno do redakce | Doručené do redakcie 19. 3. 2020
Accepted | Přijato po recenzi | Prijaté po recenzii 1. 6. 2020
Sources
Eriksen EF, Keaveny TM, Gallagher ER et al. Literature review: The effects of teriparatide therapy at the hip in patients with osteoporosis. Bone 2014; 67 : 246–256. Dostupné z DOI: <http://dx.doi.org/10.1016/j.bone.2014.07.014>.
Dempster DW, Cosman F, Parisien M et al. Anabolic actions of parathyroid hormone on bone. Endocr Rev 1993; 14(6): 690–709. Dostupné z DOI: <http://dx.doi.org/10.1210/edrv-14–6-690>.
Body JJ, Gaich GA, Scheele WH et al. A randomized double-blind trial to compare the efficacy of teriparatide [recombinant human parathyroid hormone (1–34)] with alendronate in postmenopausal women with osteoporosis. J Clin Endocrinol Metab 2000; 87(10): 4528–4535. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2002–020334>.
Neer RM, Arnaud CD, Zanchetta JR et al. Effect of parathyroid hormone (1–34) on fractures and bone mineral density in postmenopausal women with osteoporosis. N Engl J Med 2001; 344(19): 1434–1441. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJM200105103441904>.
Gallagher JC, Rosen CJ, Chen P et al. Response rate of bone mineral density to teriparatide in postmenopausal women with osteoporosis. Bone 2006; 39(6): 1268–1275. Dostupné z DOI: <http://dx.doi.org/10.1016/j.bone.2006.06.007>.
Heaney RP, Watson P. Variability in the measured response of bone to teriparatide. Osteoporos Int 2011; 22(6): 1703–1708. Dostupné z DOI: <http://dx.doi.org/10.1007/s00198–010–1376–1>.
Elraiyah T, Ahmed AH, Wang Z et al. Predictors of teriparatide treatment failure in patients with low bone mass. Bone Reports 2016; 4 : 17–22. Dostupné z DOI: <http://dx.doi.org/10.1016/j.bonr.2015.11.001>.
Payer J, Tomková S, Jackuliak P et al. Teriparatid v liečbe ťažkej osteoporózy u starších pacientok: výsledky multicentrickej prospektívnej štúdie. Clin Osteol 2018; 23(3): 88–93.
Payer J, Tomková S, Killinger Z et al. 18-mesačná liečba teriparatidom zlepšuje u pacientov s glukokortikoidmi indukovanou osteoporózou hodnoty hustoty kostného minerálu a trabekulárne kostné skóre: výsledky prospektívneho sledovania (register OSTEO.sk). Clin Osteol 2018; 23(4): 138–145.
Minne H, Audran M, Maria E et al. Bone density after teriparatide in patients with or without prior antiresorptive treatment: one-year results from the EUROFORS study. Curr Med Res Opin 2008; 24(11): 3117–3128. Dostupné z DOI: <http://dx.doi.org/10.1185/03007990802466595>.
Niimi R, Kono T, Nishihara TA et al. A retrospective analysis of nonresponse to daily teriparatide treatment. Osteoporos Int 2016; 27(9): 2845–2853. Dostupné z DOI: <http://dx.doi.org/10.1007/s00198–016–3581-z>. Erratum in Erratum to: A retrospective analysis of nonresponse to daily teriparatide treatment.
Niimi R, Kono T, Nishihara A et al. Osteoporos Int 2016; 27(9): 2887–2888. Dostupné z DOI: <http://dx.doi.oerg/10.1007/s00198–016–3625–4>.
Kim SY, Zhang M, Bockman R. Bone Mineral Density Response from Teriparatide in Patients with Osteoporosis. HSSJ 2017; 13(2): 171–177. Dostupné z DOI: <http://dx.doi.org/10.1007/s11420–016–9537–1>.
Cohen A, Stein EM, Recker RR et al. Teriparatide for Idiopathic Osteoporosis in Premenopausal Women: A Pilot Study. J Clin Endocrinol Metab 2013; 98(5): 1971–1981. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2013–1172>.
Ettinger B, San Martin J, Crans G et al. Differential effects of teriparatide on BMD after treatment with raloxifene or alendronate. J Bone Miner Res 2004; 19(5): 745–751. Dostupné z DOI: <http://dx.doi.org/10.1359/JBMR.040117>.
Lindsay R, Zhou H, Cosman F et al. Effects of a one-month treatment with PTH(1–34) on bone formation on cancellous, endocortical, and periosteal surfaces of the human ilium. J Bone Miner Res 2007; 22(4): 495–502. Dostupné z DOI: <http://dx.doi.org/10.1359/jbmr.070104>.
Borggrefe J, Graeff C, Nickelsen T N el al. Quantitative computed tomographic assessment of the effects of 24 months of teriparatide treatment on 3D femoral neck bone distribution, geometry, and bone strength: results from the EUROFORS study. J Bone Miner Res 2010; 25(3): 472–481. Dostupné z DOI: <http://dx.doi.org/10.1359/jbmr.090820>.
Labels
Clinical biochemistry Paediatric gynaecology Paediatric radiology Paediatric rheumatology Endocrinology Gynaecology and obstetrics Internal medicine Orthopaedics General practitioner for adults Radiodiagnostics Rehabilitation Rheumatology Traumatology Osteology
Article was published inClinical Osteology

2020 Issue 1-
All articles in this issue
- Prevencia sekundárnych fraktúr: multiodborové konsenzuálne stanovisko ku klinickým odporúčaním – komentár k pretlači
- Vplyv mentálnej anorexie na kostný metabolizmus
- Včasní nonrespondéri pri liečbe teriparatidom: retrospektívna analýza
- Netypické případy sekundární hyperparatyreózy při onemocnění a selhání ledvin: kazuistiky
- Manažment osteoporózy a porúch metabolizmu vápnika v čase pandémie ochorenia COVID-19
- Doporučení pro pacienty s osteoporózou v době pandemie COVID-19
- Prevence sekundárních fraktur: multioborové konsenzuální stanovisko ke klinickým doporučením
- Clinical Osteology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Netypické případy sekundární hyperparatyreózy při onemocnění a selhání ledvin: kazuistiky
- Doporučení pro pacienty s osteoporózou v době pandemie COVID-19
- Vplyv mentálnej anorexie na kostný metabolizmus
- Manažment osteoporózy a porúch metabolizmu vápnika v čase pandémie ochorenia COVID-19
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career