-
Medical journals
- Career
Postmenopauzálna osteoporóza: štandardný diagnostický a terapeutický postup
Authors: Payer Juraj; Killinger Zdenko; Jackuliak Peter; Kužma Martin
Authors‘ workplace: V. interná klinika LF UK a UNB, Nemocnica Ružinov, Bratislava ; Spoločnosť pre osteoporózu a metabolické ochorenia kostí
Published in: Clinical Osteology 2018; 23(1): 18-27
Category:
Overview
Ministerstvo zdravotníctva v spolupráci s odborníkmi aktívne pracuje na tvorbe štandardných preventívnych, diagnostických a terapeutických postupov. Štandardné diagnostické a terapeutické postupy sú akousi pomyselnou príručkou na liečbu danej diagnózy. Spoločnosť pre osteoporózu a metabolické ochorenia kostí pripravila štandardný diagnostický a terapeutický postup u pacientok s postmenopauzálnou osteoporózou.
Kľúčové slová:
antiresorpčná terapia – fraktúra – kalcium – liečba – osteoanabolická liečba – osteoporóza – prevencia – vitamín D
Kompetencie
Poskytovanie zdravotnej starostlivosti o pacientky s osteoporózou môže:
- a) cieľové zdravotnícke zariadenie:
- pracovisko ambulantnej zdravotnej starostlivosti v špecializačných odboroch endokrinológia, reumatológia, ortopédia, vnútorné lekárstvo, gynekológia
- pracovisko ústavnej zdravotnej starostlivosti – interné, ortopedické, reumatologické, endokrinologické, gynekologické
- zariadenie spoločných vyšetrovacích a liečebných zložiek – laboratórium klinickej biochémie a hematológie
- b) kompetentný zdravotnícky pracovník – lekár so špecializáciou minimálne v jednom z týchto špecializačných odborov:
- endokrinológia
- reumatológia
- ortopédia
- vnútorné lekárstvo
- gynekológia
Úvod
Osteoporóza je systémové ochorenie skeletu, ktoré sa definuje ako zníženie obsahu kostnej hmoty a narušenie mikroarchitektúry kostného tkaniva zapríčiňujúce zvýšenú fragilitu, čo rezultuje do zvýšeného rizika zlomenín už pri minimálnej traume (definícia WHO).
Najčastejšie miesta zlomenín sú distálne predlaktie, stavce, proximálny koniec femuru. Prevalencia osteoporózy sa odhaduje asi na 6 % v našej populácii. Riziko osteoporotickej fraktúry v uvedených miestach u žien po menopauze predstavuje asi 40 %. Mortalita u pacientok so zlomeninami stavcov a proximálneho femuru je asi 6–8-krát vyššia ako u zdravej populácie.
Termín osteoporóza je z patofyziologického hľadiska vyhradený pre zníženie množstva kostnej masy na jednotku objemu kosti. Zloženie kosti je však histologicky a biochemicky normálne. Ide o zlomeniny vznikajúce na podklade neadekvátne nízkej energie úrazu. Typické lokality sú stavce a dlhé kosti, najmä horná tretina stehennej kosti a dolná tretina vretennej kosti.
Diagnostika a liečba osteoporózy si vyžaduje multidisciplinárnu spoluprácu viacerých medicínskych odborov. Komplexnú zdravotnú starostlivosť – prevenciu, diagnostiku a liečbu osteoporózy vrátane dispenzarizácie pacientok vykonáva osteologicky zameraný lekár (ďalej len „osteológ“) so špecializáciou v odbore ortopédia, reumatológia, endokrinológia a osteológ so špecializáciou v odbore interná medicína a gynekológia. Iní lekári špecialisti vykonávajú konzultačnú činnosť pre potreby diagnostiky, diferenciálnej diagnostiky a liečby.
Epidemiológia
Celosvetove utrpí 1 z 3 žien a 1 z 5 mužov vo veku > 50 rokov niektorú z typických osteoporotických zlomenín (predlaktie, chrbtica, proximálny femur). V priemere 20–25 % žien starších > 50 rokov má 1, ev. viac vertebrálnych fraktúr.
Celoživotné riziko osteoporotickej zlomeniny sa odhaduje na 40 %, čo je podobné riziku srdcovocievnych ochorení. 50-ročná žena má až 39% riziko osteoporotickej zlomeniny a 50-ročný muž asi 13%.
Zlomeniny u starších pacientov majú často závažné dôsledky a výrazne tak ovplyvňujú kvalitu ich života. Napriek adekvátnej liečbe až 20 % pacientov zomiera do jedného roka po zlomenine v oblasti bedrového kĺbu a ďalších 30 % zostáva trvalo imobilných.
Patofyziológia
Osteoporóza je multifaktoriálne podmienené ochorenie, u ktorého významnú úlohu zohráva genetická predispozícia s ďalšími neovplyvniteľnými, ale aj ovplyvniteľnými rizikovými faktormi.
Neovplyvniteľné rizikové faktory sú genetická predispozícia (belosi, pozitívna rodinná anamnéza osteoporotických fraktúr, prekonaná zlomenina po inadekvátnej traume, gracilný habitus), vek, ženské pohlavie.
Ovplyvniteľné rizikové faktory sú fyzická aktivita, prívod kalcia v potrave (nedostatočný prívod kalcia v potrave, porucha jeho resorpcie v gastrointestinálnom trakte, zvýšená exkrécia v obličkách), fajčenie, alkohol, niektoré lieky.
Taktiež poznáme celú radu ochorení vedúcich k sekundárnej osteoporóze – deficit pohlavných hormónov a rastového hormónu, hyperkorticizmus, hypertyreóza, hyperprolaktinémia, hyperparatyreóza, nedostatočný príjem kalcia, nedostatočný príjem vitamínu D, poruchy trávenia a malabsorpčné syndrómy, renálna osteopatia, inaktivita, chronické zápalové ochorenia, nádorové ochorenia, osteoporóza navodená medikamentózne (kortikosteroidy, hormóny štítnej žľazy, antiepileptiká, heparín a perorálne antikoagulanciá, cyklosporín A, cytostatiká, metotrexát, antiestrogénna liečba, androgén-deprivačná terapia), tab. 1.
Table 1. Stavy, ochorenia a medikácie spôsobujúce alebo vedúce k osteoporóze a fraktúram 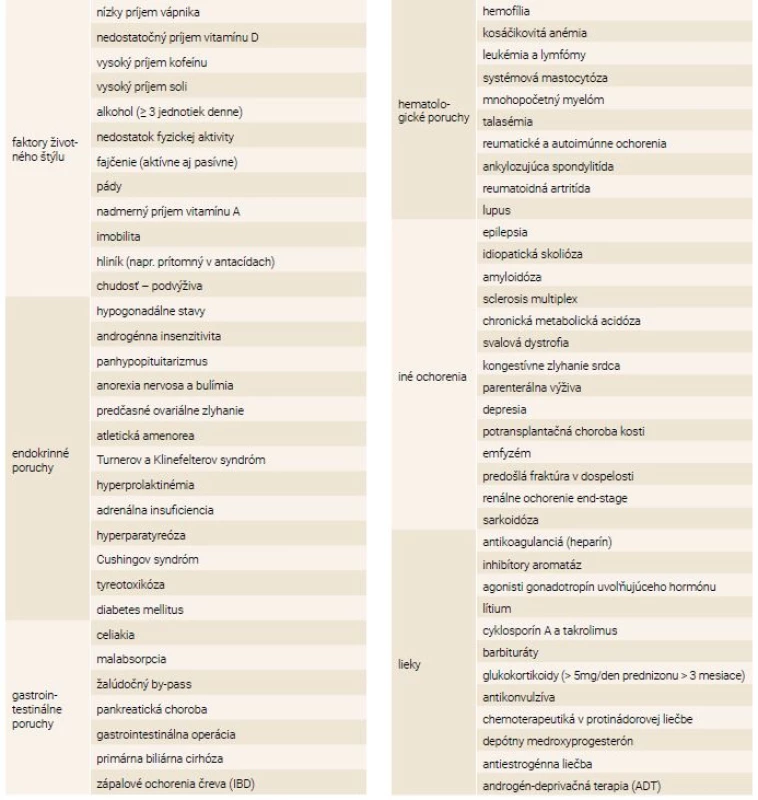
IBD – zápalové ochorenia čreva/Inflammatory Bowel Diseases Klasifikácia
Podľa etiopatogenetického hľadiska rozlišujeme dva základné typy osteoporózy – primárnu osteoporózu a sekundárnu osteoporózu.
Primárna osteoporóza
Primárna osteoporóza zahŕňa dva typy navzájom sa patogeneticky i charakterom komplikácií líšiacich typov osteoporózy:
postmenopauzálnu osteoporózu (typ I)
senilnú osteoporózu (typ II)
Postmenopauzálna osteoporóza
Charakteristický výskyt postmenopauzálnej osteoporózy je asi 15–20 rokov po menopauze, pričom najviac je postihnutá trabekulárna kosť. Za hlavný patofyziologický mechanizmus vzniku postmenopauzálnej osteoporózy sa považuje deficit estrogénov. Hlavnou klinickou manifestáciou sú fraktúry kostí s vyšším podielom trabekulárnej kosti (distálne predlaktie, stavce). Väčšina pacientok s postmenopauzálnou osteoporózou býva bez klinických príznakov, až kým neutrpia zlomeninu. Pokročilé ochorenie sa prejavuje najmä bolesťami v oblasti chrbta a prípadným znížením telesnej výšky z dôvodu deformít chrbtice spôsobených zlomeninami a kompresiou tiel stavcov.
Senilná osteoporóza
Senilná osteoporóza sa vyskytuje prevažne vo veku > 70 rokov. Postihuje ženy len o niečo častejšie ako mužov (2 : 1). K najvýznamnejším patogenetickým faktorom senilnej osteoporózy patrí vekom sa znižujúca osteoformácia (znížená vitalita a aktivita osteoblastov a osteoklastov), cirkulačné a neurotrofické poruchy kosti, štrukturálne zmeny kostného kolagénu podmienené vekom a sekundárna hyperparatyreóza pri zníženej absorpcii vápnika v dôsledku zníženej tvorby kalcitriolu. Manifestuje sa fraktúrami, tak v oblasti kortikálnej ako i trabekulárnej kosti.
Klinický obraz a diagnostika
Rutinné vyšetrovacie metódy:
- anamnéza a fyzikálne vyšetrenie
- krvný obraz, sedimentácia erytrocytov
- sérové kalcium, albumín, fosfor, alkalická fosfatáza
- transaminázy, kreatinín, elektroforéza bielkovín
- chemická analýza moču
- vylučovanie kalcia a fosfátov do moču za 24 hod (prípadne ich frakčné exkrécie)
- denzitometrické vyšetrenie
Špecializované vyšetrovacie metódy:
- trabekulárne kostné skóre (Trabecular Bone Score – TBS)
- roentgenologické vyšetrenie (chrbtica, panva, lebka, horné končatiny, dolné končatiny)
- VFA – bočná morfometria stavcov (Vertebral Fracture Assessment) metódou DXA (dual X-ray absorptiometry)
- CT a MRI vyšetrenie
- sérové a močové osteomarkery
- vyšetrenia na vylúčenie sekundárnej osteoporózy: sérový PTH, 25-OH D, TSH, fT4, STH, IGF1, gonadotropíny (LH, FSH), prolaktín, močový voľný kortizol, ACTH v sére, pohlavné hormóny (estradiol, testosterón), kostná biopsia, biopsia z tenkého čreva a špecifické antigliadínové protilátky, onkomarkery
Anamnéza a fyzikálne vyšetrenie
Pri klinickom vyšetrení sa treba zamerať na cielené zistenie rizikových faktorov a ochorení vedúce k sekundárnej osteoporóze, zmeny výšky, zvýraznenie hrudnej kyfózy, vykleňovanie brucha, nízku hmotnosť (BMI < 19 kg/m2), gracilnú postavu, vzdialenosť medzi lopatou bedrovej kosti a posledným rebrom < na 3 prsty, fyzikálny nález svedčiaci pre iné ochorenie, ktoré môže viesť k sekundárnej osteoporóze, fyzikálny nález typický pre iné metabolické osteopatie.
Biochemické vyšetrenie
Cieľom biochemického vyšetrenia je diferenciálna diagnostika sekundárnej osteoporózy, posúdenie stavu fosfokalciového metabolizmu, zhodnotenie aktivity kostného metabolizmu, (teda oddiferencovať vysoko-obratovú a nízko-obratovú osteoporózu).
Za referenčné markery sa považuje sérová hladina P1NP (Procollagen type 1 N-Propeptide) ako marker kostnej formácie a CTX (C-terminal cross-linking telopeptide of type 1 collagen) ako marker kostnej resorpcie.
Osteodenzitometrické vyšetrenie
Typy denzitometrií:
a) periférna denzitometria:
- dvoj-energetická roentgenová absorpciometria (DXA) – predlaktie
- kvantitatívna ultrasonografická denzitometria (USD) – päta
b) centrálna denzitometria (DXA):
- štandardne merané oblasti: - proximálny femur a chrbtica
- doplňujúce merania: - celotelová (vrátane body composition) - bočný morfometrický scan - denzitometria u pacientov po endoprotéze
- trabekulárne kostné skóre (Trabecular Bone Score – TBS)
c) kvantitatívna výpočtová tomografia qCT – meranie v oblasti chrbtice
Indikácie pre denzitometrické vyšetrenie:
- deficit estrogénov: predčasná menopauza (< 45 rokov), prolongovaná sekundárna amenorea (> 1 rok), primárny hypogonadizmus
- liečba kortikoidmi dávkou ≥ 5 mg prednizónu, ktorej trvanie sa predpokladá > 3 mesiace, je indikáciou na zmeranie kostnej denzity ešte pred začatím liečby
- anamnéza zlomenina krčka stehennej kosti u matky
- nízky index telesnej hmotnosti (Body Mass Index – BMI < 19 kg/m2)
- všetky ochorenia asociované s osteoporózou: anorexia nervosa, malabsorpcia, primárna hyperparatyreóza, difúzne ochorenia spojiva, reumatoidná artritída, chronické zápalové ochorenia čreva, posttransplantačný syndróm, chronická renálna insuficiencia, hypertyreóza, prolongovaná imobilizácia, Cushingov syndróm, chronické hepatopatie, myeloproliferatívne ochorenia, genetické a iné metabolické ochorenia kostí
- podozrenie na osteoporózu z RTG snímky, alebo nález vertebrálnej deformity
- zlomenina femuru, chrbtice, predlaktia po neadekvátnej traume
- významná strata výšky (> 4 cm oproti výške v mladosti alebo > 2 cm za 2 roky, alebo torakálna kyfóza
- monitoring liečby antiporotikami
- chronické užívanie liekov (antikoagulanciá, antiepileptiká, tyroidálne hormóny, imunosupresíva, cytostatiká, ADT, antiestrogény)
- ženy vo veku > 65 rokov
- muži vo veku > 70 rokov
Denzitometrické vyšetrenie indikuje po splnení indikačných kritérií lekár so špecializáciou v odbore reumatológia, endokrinológia, ortopédia a lekár so špecializáciou v odbore interná medicína, gynekológia. Iní špecialisti odosielajú pacienta na na vyššie uvedenú ambulanciu, ktorá disponuje denzitometrom a príslušným špecialistom so skúsenosťami v diagnostike a liečbe osteoporózy (reumatológia, endokrinológia, ortopédia).
Periférna denzitometria v diagnostike osteoporózy
Meranie na predlaktí je možné použiť na diagnostiku osteoporózy len v týchto prípadoch: u pacientov s primárnou hyperparatyreózou, u pacientov s extrémnou obezitou (presahujúcou limity denzitometrického stola), u pacientov, u ktorých nie je merateľná alebo hodnotiteľná oblasť chrbtice a femuru. Pre stanovenie diagnózy osteoporózy je v prípade merania na predlaktí potrebné hodnotiť denzitu v oblasti označovanej ako 33% radius, alebo 1/3 radius nedominantnej hornej končatiny.
USD meranie denzity v oblasti päty má len prediktívny význam pre posúdenie rizika fraktúry, ale neumožňuje stanovenie diagnózy osteoporózy.
Kontrolné denzitometrické vyšetrenie
Metóda merania
Na hodnotenie dynamiky kostných zmien sa odporúča použiť meranie v AP-projekcii v oblasti lumbálnej chrbtice alebo oblasti celého proximálneho femuru – označovanej ako tzv. total femur. Periférna denzitometria v oblasti predlaktia (SXA – X-ray Absorptiometry a DXA) a päty (kvantitatívna ultrasonografická denzitometria/ultrasound densitometry – USD) nie sú vhodné pre monitorovanie účinku liečby osteoporózy.
Kontrolné meranie
Kontrolné meranie kostnej denzity má význam, ak očakávaná zmena bude ≥ ako je stanovaná signifikantná zmena kostnej denzity (Least Significant Change – LSC) na danom pracovisku. Po nasadení alebo zmene antiporotickej liečby je meranie indikované spravidla po roku liečby a po preukázaní dostatočnej efektivity tejto liečby je možné interval merania predĺžiť.
V indikovaných prípadoch, ak je odôvodnený predpoklad, že LSC sa dosiahne skôr ako za 1 rok (sekundárna osteoporóza ako napríklad kortikoidmi indukovaná osteoporóza), je možné skrátiť interval kontrolného merania aj na < 1 rok.
Požiadavky na vyhodnotenie denzitometrického merania sú uvedené v tab. 2.
Table 2. Požiadavky na vyhodnotenie denzitometrického merania 
BMD – denzita kostných minerálov/Bone Mineral Density Požiadavky na kvalitu denzitometrických pracovísk: Program kontroly kvality (Quality Control – QC) má byť v súlade s odporúčaním výrobcu o udržiavaní systému. Ak to nie je odporúčané výrobcom, vhodné sú nasledovné QC procedúry: periodické (aspoň 1-krát týždenne) skenovanie fantómu ako nezávislé hodnotenie systémovej kalibrácie, tlač a analýza dát o kalibrácii a skenoch fantómu, verifikácia priemerného BMD fantómu po každom servisnom zásahu do denzitometra. Hodnotenie presnosti merania patrí do štandardnej klinickej praxe a každé denzitometrické pracovisko si má vypočítať LSC. Chyba merania udávaná výrobcom nemá byť používaná.
Diagnostika osteoporózy u žien v postmenopauze a mužov nad 50 rokov
Je potrebné postupovať podľa WHO klasifikácie. Potrebný je dôkaz zníženia kostnej hustoty T-skóre < –2,5 SD aspoň v jednej z nasledovných lokalizácií: lumbálna chrbtica v AP-projekcii (AP – Antero-Posterior/predozadná), proximálny femur, krčok femuru, pričom do úvahy sa berú najnižšie hodnoty nameraného T-skóre (tab. 3). Hodnotia sa stavce L1 až L4. Stavce skreslené lokálnymi štrukturálnymi zmenami je potrebné z priemeru vylúčiť, pričom však je potrebné analyzovať minimálne 2 stavce. Z denzity jedného stavca nie je možná diagnostika osteoporózy.
Table 3. Diagnostické kritéria pre ženy v postmenopauze (WHO) 
SD – štandardná odchýlka/Standard Deviation T-skóre – násobok štandardnej odchýlky od priemeru normálnej mladej zdravej populácie Diagnostika osteoporózy u žien v premenopauze
Pre diagnostiku osteoporózy je vhodné použiť Z-skóre. Osteoporóza môže byť diagnostikovaná vtedy, ak je nízka BMD, Z-skóre < –2,0 SD, spojené aj so sekundárnymi príčinami osteoporózy (hypogonadizmus, primárna hyperparatyreóza, hyperkortisizmus, tyreotoxikóza, osteomalácia, malabsorpčný syndróm, difúzne ochorenia spojiva, ochorenia pečene, zápalové ochorenia čreva, ochorenia obličiek, osteogenesis imperfecta, hyperkalciúria, hypofosfatázia, deficit rastového hormónu, mastocytóza, myeloproliferatívne ochorenia, lieky vedúce k osteoporóze) alebo je už aj prítomná osteoporotická fraktúra (fraktúra stavca alebo dve periférne zlomeniny po neadekvátnej traume).
Diagnóza osteoporózy u žien v premenopauze a mužov vo veku < 50 rokov sa nemôže stanoviť len na základe samotných denzitometrických meraní. Samotné zníženie Z-skóre < –2,0 SD by malo byť hodnotené len ako zníženie BMD pod očakávanú hodnotu pre daný vek, a nie ako osteopénia alebo osteoporóza. Z skóre > – 2,0 SD by malo byť hodnotené ako hodnota v očakávanom rozsahu. (Z-skóre je násobok štandartnej odchýlky od priemeru normálnej zdravej populácie rovnakého veku a pohlavia.)
FRAX
FRAX® je počítačový algoritmus, ktorý počíta 10-ročnú pravdepodobnosť akejkoľvek veľkej zlomeniny (bedra, chrbtice, ramennej kosti alebo zápästia) a 10-ročnej pravdepodobnosti zlomeniny bedra. Riziko zlomeniny je vypočítané na základe veku, BMI a dichotomizovaných rizikových faktorov, ktoré zahŕňajú osteoporotickú zlomeninu v minulosti, rodičovskú anamnézu fraktúry bedra, fajčenie, dlhodobé užívanie perorálnych glukokortikoidov, reumatoidnú artritídu, iné príčiny sekundárnej osteoporózy a konzumáciu alkoholu. Na zvýšenie predikcie rizika zlomenín môže byť voliteľne pridaná minerálna hustota kostného krčku femuru (BMD). Za vysokorizikových sa považujú pacienti s FRAX ≥ 20 % pre „major“ (akúkoľvek veĺkú osteoportickú) zlomeninu alebo FRAX ≥ 3 % pre fraktúru proximálneho femuru (hip).
Trabekulárne kostné skóre
TBS je nedávno vyvinutý nástroj, ktorý na základe textúry skenov lumbálnej chrbtice realizovaných pomocou DXA zachytáva informácie týkajúce sa trabekulárnej mikroarchitektúry. Nízke TBS je významné asociované s incidenciou osteoporotických zlomenín a je čiastočne nezávislé od klinických rizikových faktorov a BMD v oblasti v bedrovej chrbtice a proximálnej stehennej kosti. Môže sa teda použiť ako doplnok merania BMD a je softvérovou možnosťou pre denzitometre. Štúdie vrátane metaanalýzy ukázali zlepšenie predikcie zlomeniny, keď sa používa TBS bedrovej chrbtice v kombinácii s nástrojom FRAX. TBS môže tiež zohrávať úlohu pri hodnotení rizika fraktúry pri niektorých príčinách sekundárnej osteoporózy (napríklad diabetes, hyperparatyreoidizmus a osteoporóza indukovaná glukokortikoidmi).
RTG vyšetrenie
Z roentgenologického vyšetrenia je možné stanoviť diagnózu osteoporózy jednoznačne, len ak sú už prítomné deformity stavcových tiel. Zníženie výšky tela stavca o viac ako 20 % (predná, zadná hrana, alebo stred – semikvantitatívne hodnotenie podľa Genanta) sa považuje za fraktúru, (obr). Na posúdenie deformít stavcov je možné využiť aj vyšetrenie CT, MRI, alebo morfometrické vyšetrenie v bočnej projekcii pri DXA. Je potrebné vylúčiť inú etiológiu zníženia výšky tela stavca. Zlomeniny stavcov, aj keď sú asymptomatické, sú silnými rizikovými faktormi ďalšej zlomeniny.
Obr | Semikvantitatívne hodnotenie zlomenín stavcov podľa Genanta 
Indikácie pre IVA, resp. VFA
Zobrazenie bočnej chrbtice so štandardnou rádiografiou (Instant Vertebral Assessment - IVA) alebo denzitometrickým VFA (Vertebral Fracture Assessment) je indikované, keď T-skóre je < -1,0 a je prítomné ≥ 1 z nasledujúcich:
- ženy vo veku ≥ 70 rokov alebo muži vo veku ≥ 80 rokov
- strata výšky > 4 cm
- vertebrálna zlomenina udávaná pacientom, dovtedy nedokumentovaná
- liečba glukokortikoidmi ≥ 5 mg prednizónu alebo ekvivalent denne počas ≥ 3 mesiacov
Diferenciálna diagnostika
Diferenciálna diagnostika zahŕňa zistenie ochorení, ktoré vedú k vzniku sekundárnej osteoporózy, ako sú deficit pohlavných hormónov a rastového hormónu, hyperkorticizmus, hypertyreóza, hyperprolaktinémia, hyperparatyreóza, nedostatočný príjem kalcia, nedostatočný príjem vitamínu D, poruchy trávenia a malabsorpčné syndrómy, anorexia nervosa, chronické hepatopatie, renálna osteopatia, inaktivita, chronické zápalové ochorenia, nádorové ochorenia, osteoporóza navodená medikamentózne (kortikosteroidy, hormóny štítnej žľazy, antiepileptiká, heparín a perorálne antikoagulanciá, cyklosporín A, cytostatiká, metotrexát), difúzne ochorenia spojiva, reumatoidná artritída, posttransplantačný syndróm, myeloproliferatívne ochorenia, genetické a iné metabolické ochorenia kostí. Taktiež v rámci diferenciálnej diagnostiky je nutné vylúčiť postihnutie kosti pri iných ochoreniach spôsobujúcich zmenu kostnej denzity (metabolické osteopatie, nádorové ochorenia a iné).
Prevencia
Prevenciou osteoporózy a následne aj osteoporotických fraktúr je vhodné sa začať zaoberať nielen u pacientov s prítomnými rizikovými faktormi osteoporózy, ale aj u zdravých žien po menopauze.
Prevencia fraktúr u žien vo veku > 50 rokov:
- vylúčenie známych rizikových faktorov (alkohol, fajčenie, lieky)
- fyzicky aktívny životný štýl
- udržiavanie BMI > 19 kg/m2
- primeraná expozícia slnečnému žiareniu eventuálne i suplementácia D-vitamínu (800–1000 IU denne), najmä vo vyšších vekových skupinách
- adekvátny príjem kalcia v diéte (1 000–1 200 mg denne), ak to nie je možné zabezpečiť, odporúča sa suplementácia kalcia v dávke podľa veku, pohlavia a hormonálneho statusu
- u žien po menopauze s rizikovými faktormi vzniku osteoporózy, alebo denzitometricky verifikovanou zníženou kostnou denzitou (osteopénia) a klimakterickým syndrómom zvážiť možnosť hormonálnej substitučnej liečby, pokiaľ nie je kontraindikovaná
Liečba
Cieľom liečby osteoporózy je predovšetkým redukcia rizika fraktúry. Pred začatím liečby je potrebné vylúčiť sekundárnu osteoporózu a iné metabolické ochorenia kostí prejavujúce sa nízkou kostnou denzitou.
Farmakologická liečba osteoporózy
Najbežnejšie používané lieky sú raloxifén, bisfosfonáty alendronát, ibandronát, risedronát a kyselina zoledrónová, teriparatid a denosumab. Ukázalo sa, že znižujú riziko zlomeniny stavcov a v niektorých prípadoch sa ukázalo, že redukujú riziko nonvertebrálnych zlomenín (tab. 4). Uvedené lieky (alendronát, risedronát, ibandronát, kyselina zoledrónová, raloxifén, denosumab) je možné indikovať u pacientov s denzitometricky verifikovanou osteoporózou alebo u pacientov s dokázanou osteoporotickou fraktúrou. Indikácia liečby teriparatidom podlieha špeciálnym indikačným kritériám (tab. 5).
Table 4. Súhrn účinkov antiporotickej liečby 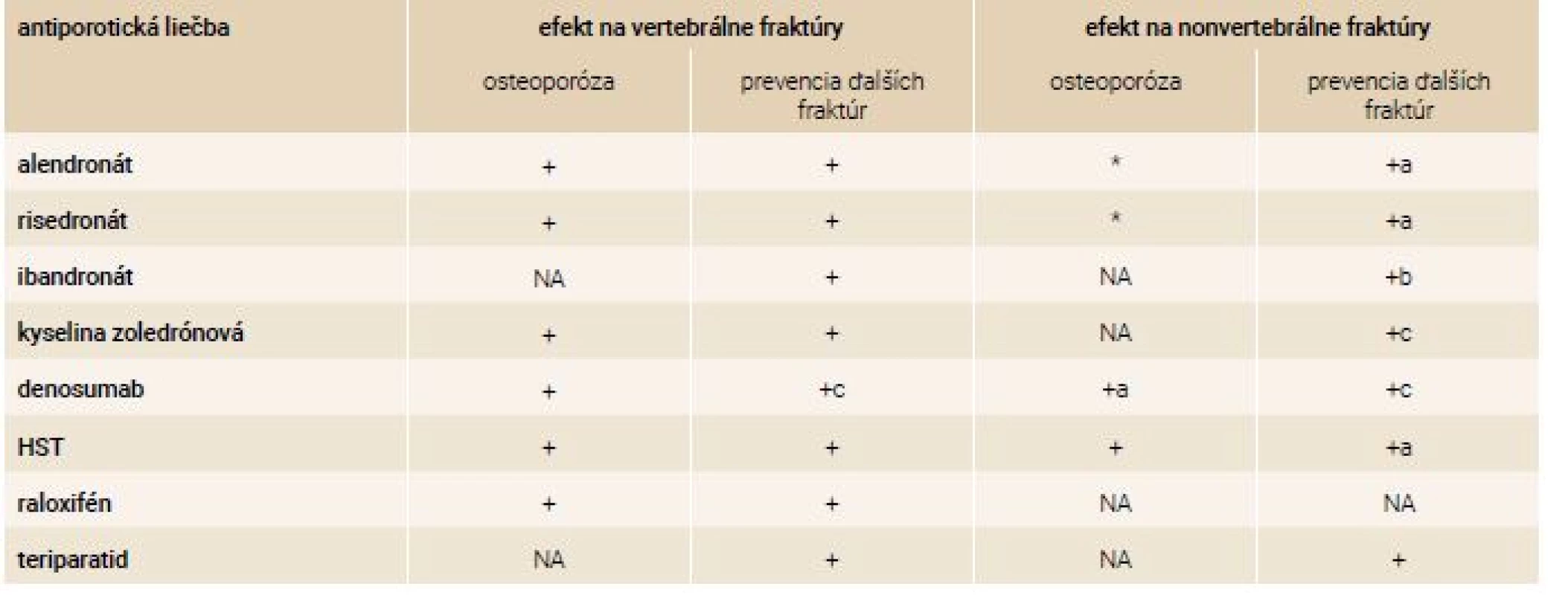
+ – dokázaný klinický účinok NA – nemá dokázaný EBM účinok * – predpokladaná účinnosť ale klinicky neoverená GIOP – glukokortikoidmi indukovaná osteoporóza HST – hormonálna substitučná terapia (estrogény) a – vrátane HIP fraktúry b – len u časti pacientov podľa post-hoc analýz c – zmiešaná skupina pacientov s alebo bez prevalentnej vertebrálnej fraktúry d – indikovaný u mužov s karcinómom prostaty po hormonálnej ablácii Table 5. Indikácie liečby 
d – deň PMO – postmenopauzálna osteoporóza GIOP – glukokortikoidmi indukovaná osteoporóza Kalcium a vitamín D3 (u starších žien v postmenopauze s nízkou expozíciou slnečnému žiareniu, nižším príjmom kalcia v strave a nízkou fyzickou aktivitou) sú indikované na liečbu i na prevenciu osteoporózy. Suplementácia kalcia a D-vitamínu je trvalá a je podmienku každej liečby osteoporózy.
Priaznivý efekt hormonálnej substitučnej liečby na kosti bol dokázaný, vzhľadom však na pomer risk/benefit tejto liečby nie je aktuálne indikovaná na prevenciu a liečbu osteoporózy. Indikáciou na začatie liečby je klimakterický syndróm a pri jeho liečbe je prevencia osteoporózy výrazne aditívnym účinkom. Súčasťou všetkých uvedených antiresorpčných terapeutických postupov je dodržiavanie opatrení uvedených v prevencii.
Liečba osteoporózy by mala byť dlhodobá, trvajúca minimálne 5 rokov. Horná hranica dĺžky liečby nie je presne definovaná.
Preskripcia uvedených liekov sa riadi podľa zoznamu liečiv a liekov plne uhrádzaných alebo čiastočne uhrádzaných na základe verejného zdravotného poistenia.
Kalcium a vitamín D
Kalcium a vitamín D sú indikované na prevenciu aj liečbu osteoporózy a ich suplementácia je potrebná pri užívaní aj iných antiporotík. Na Slovensku je platné a odporúčané v osteologickej indikácii prevencie aj liečby podávať 1 000 – 1 200 mg kalcia spolu s 800 – 1 000 IU vitamínu D.
Bisfosfonáty
Pôsobením bisfosfonátov dochádza k dysfunkcii až apoptóze osteoklastov, spomaľuje sa osteoresorpcia a podľa typu bisfosfonátu môže prísť k narušenej remodelácii. Medzi bisfosfonáty používané v liečbe osteoporózy patria alendronát, rizedronát, ibandronát a kyselina zoledrónová. Majú dokumentované účinky na redukciu osteoporotických fraktúr (vertebrálnych, krčka femuru aj nevertebrálnych) u postmenopauzálnych žien, redukciu rizika zlomenín u pacientov s osteoporózou indukovanou glukokortikoidmi, ako aj u mužov s osteoporózou. Dávkovanie: alendronát – 70 mg p.o. 1-krát týždenne, v minulosti sa užíval 10 mg p.o. denne / rizedronát – 35 mg p.o. 1-krát týždenne alebo 75 mg p.o. 2 dni v mesiaci po sebe / ibandronát – 150 mg p.o. 1-krát mesačne, alebo 3 mg 1-krát za 3 mesiace intravenózne / kyselina zoledrónová – 5 mg 1-krát ročne intravenózne.
Selektívne modulátory estrogénových receptorov
Selektívne modulátory estrogénových receptorov (SERM) sú látky, ktoré pôsobia ako silní estrogénoví agonisti na kosť a kardiovaskulárny aparát a zároveň majú antagonistický účinok na tkanivo prsnej žľazy. Majú dokumentovaný efekt na redukciu vertebrálnych fraktúr. SERM redukujú riziko karcinómu prsníka. Raloxifén sa podáva v dávke 60 mg perorálne denne.
Denosumab
Denosumab kauzálne zasahujúci do patogenézy osteoporózy je rekombinantná, plne ľudská monoklonálna protilátka proti RANKL (Receptor Activator for Nuclear Faktor kappa-b Ligand), ako kľúčovému mediátoru diferenciácie, funkcie a prežívania osteoklastov. Má dokumentovaný efekt na redukciu vertebrálnych aj nonvertebrálnych fraktúr. Podáva sa subkutánne 60 mg 1-krát za 6 mesiacov.
Teriparatid
Teriparatid (rhPTH 1–34, aminoterminálna sekvencia 34 aminokyselín molekuly ľudského parathormónu) predstavuje anabolikum používané v liečbe závažnej osteoporózy. V závislosti od dávky stimuluje osteoformáciu i resorpciu a môže viesť k zvyšovaniu alebo poklesu kostnej hmoty. Výrazne zvyšuje kostnú denzitu a redukuje riziko vertebrálnych aj nevertebrálnych fraktúr. Liečba e teriparatidom je vyhradená pre najťažšie typy osteoporózy. Aplikuje sa subkutánne denne po dobu 18 (Slovensko) až 24 mesiacov (EMA, FDA).
Hormonálna substitučná liečba
Vzhľadom na zvýšené riziko invazívneho karcinómu prsníka, tromboembolických príhod a kardiovaskulárnych a cerebrovaskulárnych komplikácií v súčasnosti nie je hormonálna substitučná liečba indikovaná na liečbu osteoporózy, ale protektívny kostný efekt sa využíva len pri indikácii liečby klimakterického syndrómu.
Monitoring liečby osteoporózy
Pre antiresorpčnú liečbu sa za efektívnu liečbu považuje reduckia rizika zlomenín podporená vzostupom BMD a poklesom markerov kostného obratu.
Monitoring liečby pomocou kostných markerov
Zmeny v kostných markeroch indukované liečbou sú rýchlejšie ako zmeny BMD a typicky sa merajú približne po 3 až 6 mesiacoch po začiatku liečby. Medzi krátkodobým poklesom markerov kostného obratu a znížením rizika zlomenín stavcov a nonvertebrálnych zlomenín použitím antiresorpčnej liečby (raloxifén a bisfosfonáty) existuje významná asociácia. V prípade bisfosfonátov bola IOF (International Osteoporosis Foundation) navrhnutá skríningová stratégia na základe odpovede P1NP a CTX po 3 mesiacoch liečby. Ak sa nepozoruje žiadna zmena, lekár by mal prehodnotiť dodržiavanie liečby a tiež iné ďalšie možné problémy(vylúčenie sekundárnej osteoporózy atď).
Monitoring liečby pomocou denzitometrie
Metaregresie, založené na súhrnných štatistikách, preukazujú silnejšiu koreláciu medzi zmenou BMD a znížením rizika zlomeniny. Zatiaľ čo 16% zníženie rizika zlomeniny po liečbe alendronátom bolo spojené s nárastom BMD na bedrovej chrbtici, väčšie zvýšenia BMD na chrbtici aj bedra pozorované s alendronátom boli spojené s väčším znížením rizika nonvertebrálnych zlomenín. Napriek tomu, u pacientov liečených risedronátom alebo raloxifénom zmeny BMD predpovedajú horšie stupeň redukcie zlomenín chrbtice (raloxifén) alebo bezvertebrálnych (risedronát). V prípade raloxifénu predstavovali percentuálne zmeny v BMD 4 % pozorovaného zníženia rizika vertebrálnych zlomenín. Percentuálna zmena BMD bedra po 3 rokoch terapie denosumabom viedla k 35% zníženiu nových zlomenín stavcov a až o 84 % znížila rizika nevertebrálnej fraktúry.
Pri osteoanabolickej terapii zvýšenie BMD vedie k zníženia rizika vertebrálnych zlomenín o tretinu.
Pri postmenopauzálnej osteoporóze sú nárasty BMD pomocou antiresorpčenej liečby s presnosťou chýb opakovaných meraní (zvyčajne 1–2 %) mierne (zvyčajne 2 % ročne), takže časový interval opakovania meraní BMD musí byť dostatočný, aby sa zistilo, či je akákoľvek zmena skutočná. Pre osteoanabolickú liečbu je nárast BMD oveľa rýchlejší, a preto sa môžu realizovať kontrolné merania BMD častejšie.
Zlyhanie liečby osteoporózy
Za zlyhanie liečby sa považuje, ak je prítomné jedno z nasledujúcich:
- výskyt druhej osteoporotickej zlomeniny počas liečby
- pre antiresorpčné lieky pokles CTx a P1NP < LSC (ak nie sú známe vstupné hodnoty, pozitívna odpoveď = menej ako priemerná hodnota mladých zdravých dospelých); pre teriparatid vzostup kostných markerov < LSC.
- zníženie BMD > LSC pri 95% spoľahlivosti
Dĺžka liečby osteoporózy
Odporúča sa štandardne 5-ročná liečba bisfosfonátmi. Po 5 rokoch je nutné prehodnotiť rizikový profil pacienta. Následne možno liečbu nechať prerušenú tak dlho, kým je BMD stabilizovaná a nevznikne nová fraktúra. U pacientov s vysokým rizikom by liečba mala trvať najmenej 10 rokov. V prípade denosumabu a raloxifénu by mala byť liečba vzhľadom na reverzibilný charakter efektu zrejme dlhodobá. Teriparatid a parathormón majú určenú dĺžku liečby 18 až 24 mesiacov.
Kombinovaná a sekvenčná liečba
Vzhľadom na to, že liečba osteoanabolickými liekmi (teriparatid) je obmedzená na 24 mesiacov a účinnosť sa zníži po ukončení liečby, ich väčší účinok na BMD môže byť udržiavaný inhibítormi kostného obratu po liečbe. Pri absencii podania antiresorptíva po liečbe osteoanabolikom sa nárasty BMD získané počas liečby teriparatidom postupne strácajú.
prof. MUDr Juraj Payer, PhD., MPH, FRCP
Doručené do redakcie: 6. 8. 2018
Sources
-
Bilezikian JP, Khan AA, Potts JT jr. Guidelines for the Management of Asymptomatic Primary Hyperparathyroidism: Summary Statement from the Third International Workshop. J Clin Endocrinol Metab 2009; 94(2): 335–339.
-
Genant HK, Wu CY, van Kuijk C et al. Vertebral fracture assessment using a semiquantitative technique. J Bone Miner Res 1993; 8(9): 1137–1148.
-
Hans DB, Shepherd JA, Schwartz EN et al. Peripheral dual-energy X-ray absorptiometry in the management of osteoporosis: the 2007 ISCD Official Positions. J Clin Densitom 2008; 11(1): 188–206.
-
Hernlund E, Svedbom A, Ivergard M et al. Osteoporosis in the European Union: medical management, epidemiology and economic burden. A report prepared in collaboration with the International Osteoporosis Foundation (IOF) and the European Federation of Pharmaceutical Industry Associations (EFPIA). Arch Osteoporos 2013; 8 : 136. Dostupné z DOI: <http://doi: 10.1007/s11657–013–0136–1>.
-
Kanis JA, Borgstrom F, Compston J et al. SCOPE: a scorecard for osteoporosis in Europe. Arch Osteoporos 2013; 8 : 144. Dostupné z DOI: <http://doi: 10.1007/s11657–013–0144–1>.
-
Kanis JA, Johnell O, Oden A et al. FRAX and the assessment of fracture probability in men and women from the UK. Osteoporos Int 2008; 19(4): 385–397.
-
Kanis JA, McCloskey EV, Johansson Het al. European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int 2013; 24(1): 23–57.
-
Cosman F, de Beur SJ, LeBoff MS et al. National Osteoporosis Foundation: Clinician´s Guide to Prevention and Treatment of Osteoporosis. Washington, DC: National Osteoporosis Foundation; 2010. Osteoporos Int 2014; 25(10): 2359–2381.
-
Odborné usmernenie MZ SR pre diagnostiku a liečbu osteoporózy. Vestník MZ SR, čiastka 9–16, ročník 54, zo dňa 1. marca 2006.
-
Odborné usmernenie MZ SR pre diagnostiku a liečbu glukokortikoidmi indukovanej osteoporózy (GIOP). Vestník MZ SR, čiastka 51–53, ročník 57, zo dňa 13. novembra 2009.
-
Odborné usmernenie MZ SR o diagnostike a liečbe pacienta po osteoporotických zlomeninách. Vestník MZ SR, čiastka 1–3, ročník 59, zo dňa 4. februára 2011.
-
Official Positions of the International Society for Clinical Densitometry 2015. Dostupné z WWW: <http://www.iscd.org/official-positions/2015-iscd-official-positions-adult>.
-
Payer J, Killinger Z et al. Osteoporóza. Herba: Bratislava 2012. ISBN 978–80–8971–94–1.
-
Payer J, Borovský M (eds). Osteoporóza u vybranných ochorení. Herba: Bratislava 2014. ISBN 978–80–8963–11–93.
-
Payer J, Brazdilova K, Jackuliak P. Management of glucocorticoid-induced osteoporosis: prevalence, and emerging treatment options. Drug Healthc Patient Saf 2010; 2 : 49–59.
-
Saag KG, Shane E, Boonen S et al. Teriparatide or alendronate in glucocorticoid-induced osteoporosis. N Engl J Med 2007; 357(20): 2028–2039.
-
Svedbom A, Hernlund E, Ivergard M et al. Osteoporosis in the European Union: a compendium of country-specific reports. Arch Osteoporos 2013; 8 : 137. Dostupné z DOI: http://doi: 10.1007/s11657–013–0137–0>.
-
Watts NB, Adler RA, Bilezikian JP et al. Osteoporosis in Men: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 2012; 97(6): 1802–1822.
Labels
Clinical biochemistry Paediatric gynaecology Paediatric radiology Paediatric rheumatology Endocrinology Gynaecology and obstetrics Internal medicine Orthopaedics General practitioner for adults Radiodiagnostics Rehabilitation Rheumatology Traumatology Osteology
Article was published inClinical Osteology

2018 Issue 1-
All articles in this issue
- Vliv střevního mikrobiomu na metabolizmus kostní tkáně
- Sekundárna osteoporóza pri nádorových ochoreniach
- Postmenopauzálna osteoporóza: štandardný diagnostický a terapeutický postup
- Dlouhodobá léčba osteoporózy denosumabem a její přerušení: odborné stanovisko pracovní skupiny Společnosti pro metabolická onemocnění skeletu České lékařské společnosti J. E. Purkyně
- Hypofosfatemická křivice vázaná na chromosom X (XLH) – léčba přípravkem KRN 23 (burosumab): odborné stanovisko Společnosti pro metabolická onemocnění skeletu České lékařské společnosti J. E. Purkyně
- Sekundárna osteoporóza pri nádorových ochoreniach: štandardný diagnostický a terapeutický postup u pacientov s protinádorovou liečbou navodenou kostnou stratou – osteoporózou
- Clinical Osteology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Postmenopauzálna osteoporóza: štandardný diagnostický a terapeutický postup
- Dlouhodobá léčba osteoporózy denosumabem a její přerušení: odborné stanovisko pracovní skupiny Společnosti pro metabolická onemocnění skeletu České lékařské společnosti J. E. Purkyně
- Hypofosfatemická křivice vázaná na chromosom X (XLH) – léčba přípravkem KRN 23 (burosumab): odborné stanovisko Společnosti pro metabolická onemocnění skeletu České lékařské společnosti J. E. Purkyně
- Sekundárna osteoporóza pri nádorových ochoreniach: štandardný diagnostický a terapeutický postup u pacientov s protinádorovou liečbou navodenou kostnou stratou – osteoporózou
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

