-
Medical journals
- Career
Novinky v paliativní systémové terapii análního spinocelulárního karcinomu
Authors: R. Lohynská 1,2; Z. Pechačová 2
Authors‘ workplace: Onkologická klinika 1. LF UK a FTN Praha 1; Ústav radiační onkologie, 1. LF UK a FN Bulovka, Praha 2
Published in: Klin Onkol 2022; 35(3): 190-194
Category: Review
doi: https://doi.org/10.48095/ccko2022190Overview
Východiska: Metastatický a lokálně recidivující inoperabilní anální dlaždicobuněčný karcinom (anal squamous cell carcinoma – ASCC) patří mezi vzácné nádory – ASCC tvoří asi 2 % nádorů zažívacího traktu, přičemž přibližně u 15 % pacientů je potvrzeno synchronní metastatické postižení a u pacientů po kurativní léčbě dochází k relapsu ve formě vzdálených metastáz asi ve 20 % případů. Standardem paliativní systémové léčby je v současné době režim PF ve složení fluorouracil (5-FU) s cisplatinou (cDDP) nebo kombinace karboplatiny s paklitaxelem. Cíl: Cílem předkládaného sdělení je souhrn dalších možností systémové paliativní léčby u ASCC vč. výsledků relevantních klinických studií s novými či modifikovanými režimy. Trojkombinace s taxany přinesly slibné léčebné výsledky a zejména zařazení režimu DCF (cDDP + 5-FU + docetaxel) do 1. linie léčby přináší významné zvýšení léčebných odpovědí při dobré toleranci léčby. Další slibnou možností paliativní léčby je imunoterapie checkpoint inhibitory PD-1 nebo PD-L1, které se mohou úspěšně uplatnit v paliativní systémové léčbě nebo i v rámci kurativních režimů. Předmětem výzkumu zůstávají kombinace chemoterapie s inhibitory receptoru pro epidermální růstový faktor, jejichž role v primární nebo paliativní léčbě ASCC není nyní jasná. Závěr: Dostupná data potvrzují zlepšení léčebných výsledků oproti standardním režimům při užití trojkombinace DCF s docetaxelem nebo imunoterapie checkpoint inhibitory v léčbě metastatického ASCC.
Klíčová slova:
cisplatina – imunoterapie – chemoterapie – docetaxel – 5-fluorouracil – anální karcinom
Úvod
Anální dlaždicobuněčný karcinom (anal squamous cell carcinoma – ASCC) patří mezi vzácné nádory – představuje přibližně 2 % nádorů zažívacího traktu. V roce 2018 činila incidence v ČR 1,54/100 tisíc obyvatel, mortalita dosahovala 0,75/100 tisíc obyvatel, přičemž incidence mírně narůstá [1]. Častější je výskyt ASCC u žen, nejčastěji bývá diagnostikován ve věku 60–75 let. Zhoubné nádory postihují anální kanál, nebo anální okraj (kůže do 5 cm od análního kanálu).
Cílem léčby ASCC je zachování funkčního análního svěrače s udržením co nejlepší kvality života nejen po léčbě, ale i během kurativní radioterapie či chemoradioterapie (CHRT). Standardem léčby pokročilejších tumorů je CHRT – ozáření tumoru a spádových lymfatických uzlin s konkomitantním podáním chemoterapie (CHT) na bázi fluoropyrimidinů a mitomycinu [2,3]. Chirurgická excize je rezervována pouze pro definovanou podskupinu velmi časných stadií. Ačkoli incidence ASCC narůstá, mortalita se nezvyšuje [1], k čemuž přispívá zlepšení lokální kontroly při přesnějším stagingu díky technologickému rozvoji zobrazovacích metod radiodiagnostiky, nukleární medicíny a v zásadní míře užití přesnějších technik v radiační onkologii za účelem přizpůsobení výše dávky riziku postižení uzlin (dose painting) a lepšího šetření zdravých tkání [4,5]. V současné době je tedy možné radikálně léčit většinu pacientů ambulantně se zachováním vysoké kvality života v průběhu léčby i v poléčebném období [6].
V době diagnózy má synchronní metastatické postižení přibližně 15 % pacientů s ASCC a u pacientů po primární kurativní léčbě (se vstupním nemetastatickým onemocněním) dojde k rozvoji relapsu ve formě vzdálených metastáz cca ve 20 % případů [7]. Samostatná chemoterapie s paliativním záměrem je vyhrazena pro metastatická stadia, inoperabilní perzistenci či rekurentní inoperabilní lokální recidivu onemocnění, a to u pacientů v dobrém celkovém stavu. Novinkou posledních let je možnost zařazení imunoterapie u ASCC [7,8].
Paliativní chemoterapie
V paliativních režimech se dlouhodobě uplatňoval především 5-FU v kombinaci s cisplatinou (cDDP), tj. režim PF; v současné době se na základě výsledků randomizovaných studií jako optimální režim pro 1. linii léčby jeví kombinace na bázi karboplatiny (CBDCA) s paklitaxelem (PTX).
Standardní režim pro 2. linii nebyl přesně definován, složení je určeno v závislosti na kombinaci CHT aplikované v 1. linii, po režimu PF byly podávány karboplatina (AUC 5) s PTX (175 mg/m2 à 28 dní). Pokud je v 1. linii aplikována kombinace CBDCA + PTX, je ve 2. linii navrhováno více preparátů a jejich kombinací – cDDP + 5-FU, irinotekan, kombinace s taxany nebo přidání cetuximabu [7,8]. Nová doporučení Evropské společnosti pro klinickou onkologii (ESMO) z roku 2021 zmiňují i užití doxorubicinu [7]. V doporučení National Comprehensive Cancer Network (NCCN) je ve 2. linii doporučena imunoterapie s nivolumabem nebo pembrolizumabem [8].
Základním režimem paliativní chemoterapie 1. linie byl dlouhá léta režim PF: cDDP (100 mg/m2 1. den 28denního cyklu) s 5-FU (1 000 mg/m2 1–5. den kontinuální infuze v 28denním cyklu) podávaný do progrese či dle tolerance. Celková objektivní odpověď dosahuje kolem 30 % [9]. Medián přežití bez progrese (progression-free survival – PFS) dle retrospektivních dat byl 5,8–7,0 měsíce a 5leté celkové přežití (overall survival – OS) bylo 20–30% [10,11].
Variantami v rámci režimu PF je 4týdenní podání cDDP 75 mg/m2 s kontinuální infuzí 5-FU (750 mg/m2 1–5. den) [12] nebo 3týdenní režim PF cDDP 60 mg/m2 s kontinuálním 5-FU (1 000 mg/m2 1–4.den). V NCCN je redukovaný režim cDDP (75mg/m2 1. den 28denního cyklu) s 5-FU (1 000 mg/m2 1–4.den 28denního cyklu) doporučen pro konkomitantní CHRT u limitovaného metastatického onemocnění.
Proběhlo několik studií s novými či modifikovanými režimy s cílem prokázat vyšší účinnost a přijatelnou toxicitu oproti standardní CHT cDDP + 5-FU.
Režim FOLFCIS (ccDDP 40 mg/m2 1. den cyklu, leukovorin 400 mg/m2 1. den cyklu a 5-FU 400 mg/m2 bolus 1. den následovaný kontinuální 48hod i.v. infúzí 5-FU 1 000 mg/m2 ve 14denním cyklu) v 1. linii chemoterapie u metastatického či neresekabilního lokálně recidivujícího ASCC. Léčebná odpověď byla 48 % při mediánu sledování 41,6 měsíce. PFS bylo 7,1 měsíce a OS 22,1 měsíce. V testovaném souboru byl zjišťován také genomický profil nádorových buněk a i přes nízké zastoupení HPV-negativních nádorů bylo zřejmé, že tato podskupina vykázala nižší přínos CHT FOLFCIS a bylo u nich detekováno odlišné mutační spektrum zejména v genech TP53, TERT a CDKN2A [13].
Prospektivní multicentrická randomizovaná studie fáze II „InterAACT“ (iniciovaná mezinárodní skupinou pro vzácné nádory se zastoupením expertů ze Spojeného království, USA, Evropy a Austrálie) demonstrovala vyšší účinnost a lepší snášenlivost režimu karboplatina a týdenní PTX oproti cDDP a 5-FU u inoperabilních lokálně recidivujících a metastatických ASCC v 1. linii CHT. Výsledky celkové léčebné odpovědi byly statisticky srovnatelné (59 vs. 57 %), PFS bylo bez signifikantního rozdílu (8,1 vs. 5,7 měsíce; p = 0,375) a OS bylo statisticky významně delší ve skupině léčené CBDCA/PTX (20 vs. 12,3 měsíce, p = 0,014). Toxicita stupně ≥ 3 se vyskytla u 71 vs. 76 %. Počet hlášených závažných vedlejších účinků byl 36 vs. 62 % (p = 0,016). Výsledky studie naznačují, že režim CHT karboplatina (CBDCA 1. den AUC 5 à 28 dní) s týdenním PTX (1., 8., 21. den 80 mg/m2 à 28 dní) účinněji prodlužuje přežití ve srovnání s cDDP (1. den 80 mg/m2 à 21 dní) a 5-FU (1–4. den 1 000 mg/m2/24 hod. à 21 dní). Studie „InterAACT“ proběhla u 91 pacientů s mediánem věku 61 let [14,15].
Trojkombinace s taxany dosahují velmi slibných výsledků.
Dvě francouzské prospektivní multicentrické studie fáze II „Epitopes-HPV01“ a „Epitopes-HPV02“ potvrdily benefit standardního (sDCF) a modifikovaného (mDCF) režimu 5-FU/cDDP/docetaxel u metastatického a lokálně rekurentního neresekabilního ASCC a prokázaly objektivní léčebnou odpověď u 87,7 % pacientů s 40,3 % kompletních odpovědí.
Modifikovaný režim mDCF sestává z 8 cyklů kombinované CHT a je indikován u pacientů nad 75 let a/nebo celkovým stavem podle Eastern Cooperative Oncology Group Performance Status (ECOG PS) = 1 (1–2. den docetaxel 40 mg/m2/den, cDDP 40 mg/m2/den a 5-FU 1 200 mg/m2/den po 2 týdnech) a standardní režim sDCF je složen z 6 cyklů CHT a je indikován u pacientů s ECOG PS = 0 a u pacientů do 75 let (1–5.den docetaxel 75 mg/m2/den, cDDP 75 mg/m2/den a 5-FU 750 mg/m2/den po 3 týdnech). U obou režimů je vhodné aplikovat profylakticky růstové faktory myelopoézy (G-SCF).
Analýza obou studií ukázala medián PFS 12,2 měsíce a medián OS 39,2 měsíce. Pětileté PFS bylo 24,5 % a 5leté OS 44,4 %. Mezi režimy 6× sDCF a 8× mDCF nebyl významný rozdíl. Tyto režimy jsou tak díky vysoké účinnosti kandidáty na standardní režim 1. linie léčby metastatického ASCC [16].
Režim 5-FU/CBDCA/PTX prokázal v malé studii fáze II 65% celkovou odpověď u ASCC, nicméně zastoupení metastatických onemocnění bylo v tomto souboru poměrně malé [17].
Přehled režimů a parametrů relevantních klinických studií shrnuje tab. 1.
Table 1. Srovnání klinických studií paliativních režimů CHT 1. linie u dlaždicového análního karcinomu (podrobnější vysvětlení v textu). 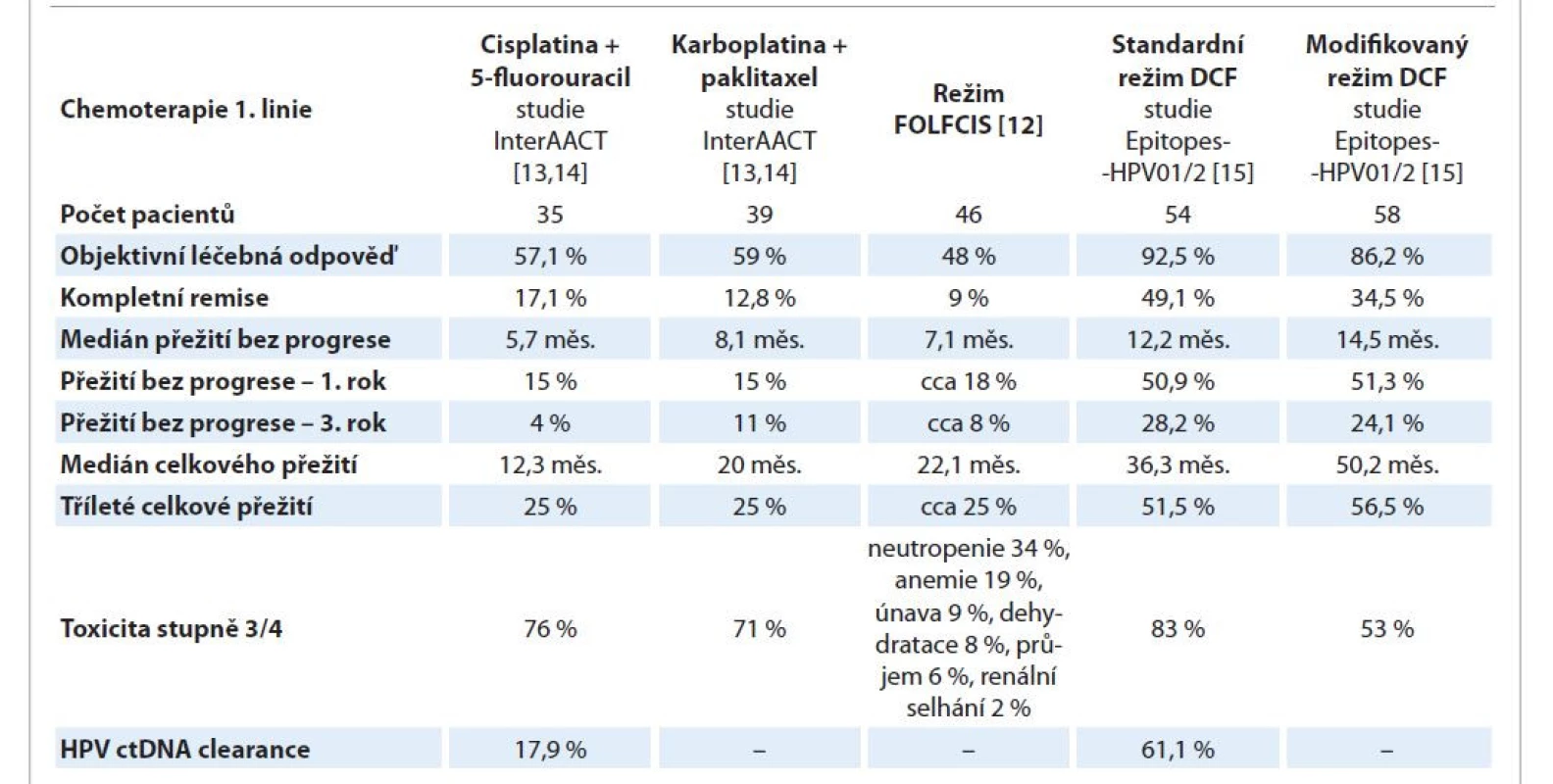
DCF – docetaxel, cisplatina, 5-fluorouracil, FOLFICIS – cisplatina 40 mg/m2 1. den cyklu, leukovorin 400 mg/m2 1. den cyklu a 5-fluorouracil 400 mg/m2 bolus 1. den následovaný kontinuální 48hod i.v. infúzí 5-fluorouracilu 1 000 mg/m2 ve 14denním cyklu, HPV – lidský papilomavirus V NCCN je zařazen jako možnost pro 1. linii léčby ASCC i režim FOLFOX, který je standardně indikován pro léčbu kolorektálního adenokarcinomu. Nebyly publikovány studie s režimem FOLFOX v léčbě metastatického ASCC a sami autoři doporučení NCCN v diskusi komentují, že režim byl zařazen na základě názoru expertů, neboť publikovány byly pouze jednotlivé kazuistiky s léčbou adenokarcinomu análního kanálu [18,19].
Imunoterapie a cílená léčba
Imunoterapie nivolumabem či pembrolizumabem je od roku 2018 součástí léčebných doporučení NCCN pro 2. linii léčby metastatického análního dlaždicobuněčného karcinomu. Imunoterapie prodlužuje PFS a OS [20], v ČR je nyní tato léčba k dispozici po schválení úhrady revizním lékařem zdravotní pojišťovny.
V současné době probíhá celá řada klinických studií, kdy je imunoterapie podána v 1. či 2. linii léčby metastatického nebo relabujícího ASCC, příp. je přidána ke standardní kurativní konkomitantní chemoradioterapii nemetastatických stadií.
Nivolumab (plně humánní protilátka IgG4 selektivně blokující inhibiční receptor programované buněčné smrti PD 1 na aktivovaných T lymfocytech, čímž umožňuje restart protinádorové odpovědi) byl testován v randomizované studii fáze II v dávce 3 mg/kg à 2 týdny u 37 pacientů s metastatickým spinocelulárním análním karcinomem. Léčba přinesla kompletní remisi (complete remission – CR) u 5 %, parciální remisi (PR) u 19 % pacientů a stabilizaci onemocnění (stable disease – SD) u 47 % pacientů. Medián trvání odpovědi u pacientů, kteří odpověděli na léčbu, byl 5,8 měsíce (PFS 4,1 měsíce a OS 11,5 měsíce). Tolerance nivolumabu v monoterapii byla dobrá (nežádoucí účinky stupně 3 byly zaznamenány u 13 % pacientů, nebyl pozorován stupeň 4). U pacientů, kteří odpověděli na léčbu, byla zaznamenána vyšší exprese PD-L1 než u pacientů, u nichž nedošlo k léčebné odpovědi [21].
Pembrolizumab (humanizovaná monoklonální protilátka / ligand proti receptoru PD1) byl hodnocen ve studii fáze Ib KEYNOTE-028 u metastatických předléčených pacientů s PD-L1 pozitivními nádory ≥ 1 % v dávce 10 mg/kg à 2 týdny po dobu max. 2 let nebo do progrese či neakceptovatelné toxicity. Zařazeno bylo 24 pacientů, z nichž u 4 (17 %) bylo dosaženo PR a u 10 (42 %) byla potvrzena SD. Medián přežití bez nemoci byl 3 měsíce a medián OS 9,3 měsíce. PD-L1-pozitivní spinocelulární anální karcinomy prokázaly slibnou odpověď na terapii pembrolizumabem v monoterapii [22].
Probíhá studie SCARCE GERCOR (NCT03519295) fáze II s atezolizumabem (PD-L1 checkpoint inhibitor) přidaným na 12 měsíců k modifikovanému režimu docetaxel, cDDP a 5-FU (mDCF) v 1. linii léčby metastatického nebo neresekabilního rekurentního onemocnění ASCC. Ve studii Epitopes-HPV02 modifikovaný DCF režim dosáhl 1letého PFS 47 %. V rameni mDCF + atezolizumab obdrží pacienti fixní dávku atezolizumabu 800 mg à 2 týdny. Ačkoli studie Epitopes-HPV02 zlepšila prognózu pacientů s metastatickým ASCC, u 50 % pacientů byla prokázána progrese v odstupu 12 měsíců po léčbě. Cílem studie je objasnění otázky, zda přidání imunoterapie k CHT mDCF sníží/oddálí progresi ve 12 měsících od léčby [23].
Ve studii fáze II CARACAS je kombinován cetuximab preparát cílený na receptor epidermálního růstového faktoru (epipdermal growth factor receptor – EGFR) s anti-PD-L1 avelumabem nebo podává samotný avelumab u recidivujících neresekabilních lokálně pokročilých nebo metastatických ASCC ve 2. linii systémové léčby (NCT03944252).
Studie NCT02314169 fáze II bude srovnávat nivolumab (à 4 týdny) s kombinací nivolumab s ipilimumabem (à 8 týdnů) ve 2. linii systémové léčby recidivujících neresekabilních lokálně pokročilých nebo metastatických ASCC.
Nádorové buňky ASCC exprimují receptor pro EGFR a mutace RAS jsou reportovány jen zřídka [24], proto byl u tohoto onemocnění testován potenciální účinek anti-EGFR preparátů – cetuximabu a panitumumabu.
Podání cetuximabu s irinotekanem v 1. linii metastatického ASCC vedlo v malé retrospektivní studii k léčebné odpovědi u 5 ze 7 pacientů, zbývající 2 pacienti (s mutací KRAS) zprogredovali [24]. V další kazuistice parciální léčebné odpovědi u pacienta s ASCC bez mutace KRAS a EGFR 2+ byla popsána PR jaterních metastáz po kombinaci cetuximabu a FOLFIRI s OS 21 měsíců [25].
Ani v kurativní chemoradioterapii nevedlo přidání cetuximabu či panitumumabu ke zlepšení výsledků léčby [26–30].
Postavení anti-EGFR preparátů v léčbě ASCC je zatím nejasné a je třeba dalšího výzkumu k nalezení vhodného režimu i podskupiny pacientů, kteří mohou z léčby profitovat.
Závěr
S ohledem na nízkou četnost análního karcinomu a jeho metastatických nebo relabujících inoperabilních forem je k dispozici poměrně málo dat o vhodných režimech systémové léčby, nicméně dostupné výsledky jednoznačně potvrzují přínos některých nových režimů. Zlepšení léčebných výsledků oproti standardním režimům přináší zejména trojkombinace DCF s docetaxelem, jež aspiruje na nový léčebný standard 1. linie léčby metastatického a lokálně rekurentního inoperabilního ASCC. Slibná data vykazuje také zařazení imunoterapie checkpoint inhibitory do paliativní léčby.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential confl icts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE recommendation for biomedical papers.Obdrženo/Submitted: 28. 7. 2021
Přijato/Accepted: 24. 10. 2021MUDr. Radka Lohynská, Ph.D.
Onkologická klinika
1. LF UK a FTN Praha
Vídeňská 800
140 59 Praha 4
e-mail: radka.lohynska@ftn.cz
Sources
1. Epidemiologie zhoubných nádorů v České republice. [online]. Dostupné z: http: //www.svod.cz.
2. Národní radiologické standardy – radiační onkologie. Věstník Ministerstva zdravotnictví České republiky 2/2016, Praha 2016.
3. Modrá kniha České onkologické společnosti, 28. aktualizace. [online]. Dostupné z: https: //www.linkos.cz/lekar-a-multidisciplinarni-tym/personalizovana-onkologie/modra-kniha-cos/aktualni-vydani-modre - knihy/.
4. Lohynská R, Nýdlová A, Drbohlavová T et al. Hematologická toxicita u IMRT/VMAT v kurativní léčbě análního karcinomu. Klin Onkol 2020; 33 (4): 288–294. doi: 10.14735/amko2020288.
5. Lohynska R, Mazana E, Novakova-Jiresova A et al. Improved survival in patients with FDG-PET/CT-based radiotherapy treatment planning for squamous cell anal cancer. Neoplasma 2020; 67 (5): 1157–1163. doi: 10.4149/neo_2020_191229N1350.
6. Lohynská R, Pechačová Z. Kapecitabin v léčbě análního spinocelulárního karcinomu. Klin Onkol 2022; 35 (1): 38–43. doi: 10.48095/ccko202238.
7. Rao S, Guren MG, Khan K et al. Anal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2021; 32 (9): 1087–1100. doi: 10.1016/j.annonc.2021.06.015.
8. Anal Carcinoma, version 2.2021. National Comprehensive Cancer Network: NCCN Clinical Practice Guidelines in Oncology. [online]. Available from: https: //www.nccn.org/professionals/physician_gls/pdf/anal.pdf
9. Sclafani F, Hesselberg G, Thompson SR et al. Multimodality treatment of oligometastatic anal squamous cell carcinoma: a case series and literature review. J Surg Oncol 2019; 119 (4): 489–496. doi: 10.1002/jso.25 320.
10. Faivre C, Rougier P, Ducreux M et al. Carcinome épidermoïde métastatique de l‘anus: étude rétrospective de l‘efficacité de l‘association de 5-fluoro-uracile en perfusion continue et de cisplatine [5-fluorouracile and cisplatinum combination chemotherapy for metastatic squamous-cell anal cancer]. Bull Cancer 1999; 86 (10): 861–865.
11. Moureau-Zabotto L, Venderely V, Abromwitz L et al. Anal cancer: French Intergroup Clinical Practice Guidelines for diagnosis, treatment and follow-up (SNFGE, FFCD, GERCOR, UNICANCER, SFCD, SFED, SFRO, SNFCP). Dig Liver Dis 2017; 49 (8): 831–840. doi: 10.1016/j.dld. 2017.05.011.
12. Eng C, Chang GJ, You YN et al. The role of systemic chemotherapy and multidisciplinary management in improving the overall survival of patients with metastatic squamous cell carcinoma of the anal canal. Oncotarget 2014; 5 (22): 11133–11142. doi: 10.18632/oncotarget. 2563.
13. Mondaca S, Chatila WK, Bates D et al. FOLFCIS treatment and genomic correlates of response in advanced anal squamous cell cancer. Clin Colorectal Cancer 2019; 18 (1): e39–e52. doi: 10.1016/j.clcc.2018.09. 005.
14. Rao S, Sclafani F, Eng C et al. InterAACT: a multicentre open label randomised phase II advanced anal cancer trial of cisplatin (CDDP) plus 5-fluorouracil (5-FU) vs carboplatin© plus weekly paclitaxel (P) in patients (pts) with inoperable locally recurrent (ILR) or metastatic treatment naive disease – an International Rare Cancers Initiative (IRCI) trial. [online]. Available from: https: //www.annalsofoncology.org/article/S0923-7534 (19) 50413-6/ fulltext.
15. Rao S, Sclafani F, Eng C et al. International rare cancers initiative multicenter randomized phase II trial of cisplatin and fluorouracil versus carboplatin and paclitaxel in advanced anal cancer: InterAAct. J Clin Oncol; 38 (22): 2510–2518. doi: 10.1200/JCO.19.03266.
16. Kim S, Meurisse A, Spehner L et al. Pooled analysis of 115 patients from updated data of Epitopes-HPV01 and Epitopes-HPV02 studies in first-line advanced anal squamous cell carcinoma. Ther Adv Med Oncol 2020; 12 : 1758835920975356. doi: 10.1177/1758835920975 356.
17. Martini G, Arrichiello G, Borrelli C et al. How I treat anal squamous cell carcinoma. ESMO Open 2020; 4 (Suppl 2): e000711. doi: 10.1136/esmoopen-2020-000711.
18. Matsunaga M, Miwa K, Oka Y et al. Successful treatment of metastatic anal canal adenocarcinoma with mFOLFOX6 + bevacizumab. Case Rep Oncol 2016; 9 (1): 249–254. doi: 10.1159/000446107.
19. Yamaura M, Yamada T, Watanabe R et al. Anal canal adenocarcinoma with neuroendocrine features accompanying secondary extramammary Paget disease, successfully treated with modified FOLFOX6: a case report. BMC Cancer 2018; 18 (1): 1142. doi: 10.1186/s12885-018-5084-0.
20. Phuong L, Rajdev L. Immunotherapy in anal cancer. Curr Oncol Rep 2020; 22 (9): 94. doi: 10.1007/s11912-020-00946-3.
21. Morris VK, Salem ME, Nimeiri H et al. Nivolumab for previously treated unresectable metastatic anal cancer (NCI9673): a multicentre, single-arm, phase 2 study. Lancet Oncol 2017; 18 (4): 446–453. doi: 10.1016/S1470-2045 (17) 30104-3.
22. Ott PA, Piha-Paul SA, Munster P et al. Safety and antitumor activity of the anti-PD-1 antibody pembrolizumab in patients with recurrent carcinoma of the anal canal. Ann Oncol 2017; 28 (5): 1036–1041. doi: 10.1093/annonc/mdx029.
23. Kim S, Buecher B, André T et al. Atezolizumab plus modified docetaxel-cisplatin-5-fluorouracil (mDCF) regimen versus mDCF in patients with metastatic or unresectable locally advanced recurrent anal squamous cell carcinoma: a randomized, non-comparative phase II SCARCE GERCOR trial. BMC Cancer 2020; 20 (1): 352. doi: 10.1186/s12885-020-06841-1.
24. Lukan N, Ströbel P, Willer A et al. Cetuximab-based treatment of metastatic anal cancer: correlation of response with KRAS mutational status. Oncology 2009; 77 (5): 293–299. doi: 10.1159/000259615.
25. Barmettler H, Komminoth P, Schmid M et al. Efficacy of cetuximab in combination with FOLFIRI in a patient with KRAS wild-type metastatic anal cancer. Case Rep Oncol 2012; 5 (2): 428–433. doi: 10.1159/000341371.
26. Leon O, Guren MG, Radu C et al. Phase I study of cetuximab in combination with 5-fluorouracil, mitomycin C and radiotherapy in patients with locally advanced anal cancer. Eur J Cancer 2015; 51 (18): 2740–2746. doi: 10.1016/j.ejca.2015.08.029.
27. Garg MK, Zhao F, Sparano JA et al. Cetuximab plus chemoradiotherapy in immunocompetent patients with anal carcinoma: a phase II Eastern Cooperative Oncology Group-American College of Radiology Imaging Network Cancer Research Group trial (E3205). J Clin Oncol 2017; 35 (7): 718–726. doi: 10.1200/JCO.2016.69.1667.
28. Sparano JA, Lee JY, Palefsky J et al. Cetuximab plus chemoradiotherapy for HIV-associated anal carcinoma: a phase II AIDS Malignancy Consortium trial. J Clin Oncol 2017; 35 (7): 727–733. doi: 10.1200/JCO.2016.69.1642.
29. Vendrely V, Lemanski C, Gnep K et al. Anti-epidermal growth factor receptor therapy in combination with chemoradiotherapy for the treatment of locally advanced anal canal carcinoma: results of a phase I dose-escalation study with panitumumab (FFCD 0904). Radiother Oncol 2019; 140 : 84–89. doi: 10.1016/j.radonc.2019.05.018.
30. Feliu J, Garcia-Carbonero R, Capdevila J et al. VITAL phase 2 study: Upfront 5-fluorouracil, mitomycin-C, panitumumab and radiotherapy treatment in nonmetastatic squamous cell carcinomas of the anal canal (GEMCAD 09-02). Cancer Med 2020; 9 (3): 1008–1016. doi: 10.1002/cam4.2722.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2022 Issue 3-
All articles in this issue
- Oslepení
- Změny N-glykosylací na sérových proteinech při nádorových onemocněních
- Novinky v paliativní systémové terapii análního spinocelulárního karcinomu
- Metabolická plasticita nádorových buněk
- Neurobiológia nádorových chorôb – význam inervácie nádorového tkaniva
- Přímé a nepřímé dopady pandemie COVID-19 na pacienty s nádory plic a pleury – retrospektivní analýza dat pacientů léčených na Klinice nemocí plicních a tuberkulózy FN Brno v době 2. a 3. koronavirové vlny
- Meigsův syndrom
- Informace z České onkologické společnosti
- Remineralizace kosti po paliativní radioterapii
- Aktuality z odborného tisku
- Prof. MUDr. Luboš Petruželka, CSc.
- Souvislost polymorfizmu IL-8 -251T>A a IL-18 -607C>A s náchylností ke karcinomu prsu – metaanalýza
- Analýza výsledků radioterapie a chemoradioterapie na pozadí imunoterapie pacientů s karcinomem ústní dutiny a orofaryngu
- Difuzní velkobuněčný B-lymfom asociovaný s ileocekální intususcepcí v dospělosti
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Meigsův syndrom
- Analýza výsledků radioterapie a chemoradioterapie na pozadí imunoterapie pacientů s karcinomem ústní dutiny a orofaryngu
- Změny N-glykosylací na sérových proteinech při nádorových onemocněních
- Metabolická plasticita nádorových buněk
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

