-
Medical journals
- Career
Neinvazivní analýza pulzní vlny u pacientů s akutní dekompenzací chronického systolického srdečního selhání
Authors: O. Ludka
Authors‘ workplace: ICRC Brno ; Interní kardiologická klinika FN Brno a LF MU, Brno
Published in: Kardiol Rev Int Med 2011, 13(4): 241-248
Overview
Úvod:
V posledních letech narůstá počet důkazů o tom, že se v patofyziologii srdečního selhání uplatňuje tuhost arteriální stěny. Zvýšený pulzní tlak je asociován se zvýšenou kardiovaskulární morbiditou a mortalitou u pacientů s asymptomatickou dysfunkcí levé komory a taktéž u pacientů s mírným srdečním selháním. Naopak snížený pulzní tlak je dle některých prací asociován se zvýšenou mortalitou u pacientů s akutní dekompenzací chronického srdečního selhání a u pacientů s pokročilým srdečním selháním a je taktéž asociován se zvýšenými hodnotami B-typu natriuretického peptidu (BNP).Cíl:
Zjistit velikost pulzního tlaku a dalších parametrů pulzní vlny pomocí její neinvazivní analýzy u pacientů hospitalizovaných pro akutní dekompenzaci chronického systolického srdečního selhání.Metodika:
Prospektivní monocentrická studie se zaměřením na neinvazivní analýzu pulzní vlny pomocí přístroje SphygmoCor.Soubor:
130 konsekutivních pacientů, 77 % mužů, 23 % žen, věk 70 let, body mass index 28,4 kg/m2, etiologie chronického srdečního selhání – 65,9 % ischemická choroba srdeční, 29,5 % dilatační kardiomyopatie, 4,6 % ostatní, NYHA anamnesticky dlouhodobě I/II/III – 17/41,9/41,1 %, při přijetí – otoky dolních končetin 58,9 %, chrůpky na plicích 88,3 %, ortopnoe 53,1 %, BNP při přijetí 1 765,7 pg/ml, při propuštění 962,3 pg/ml, ejekční frakce levé komory 27,5 %, délka hospitalizace 9 dnů.Výsledky:
(medián; 5 percentil; 95 percentil) pulzní tlak 32; 18; 59 mmHg, augmentační tlak 6; 0; 19 mmHg, augmentační index 17; 2; 37.Závěr:
Pacienti hospitalizovaní pro akutní dekompenzaci chronického systolického srdečního selhání mají po stabilizaci stavu nižší hodnoty pulzního tlaku, augmentačního indexu a augmentačního tlaku oproti referenčním hodnotám.Klíčová slova:
chronické srdeční selhání – neinvazivní analýza pulzní vlny – pulzní tlak – augmentační tlak – augmentační indexÚvod
Pulzní tlak, augmentační tlak a augmentační index, tedy parametry cévní tuhosti, jsou pozitivně asociovány s kardiovaskulárním rizikem [1]. Jednou ze základních funkcí tepen je kromě zajištění přívodu krve periferním orgánům i funkce, která má zmenšit tlakové oscilace vyvolané kontrakcemi levé komory srdeční a přeměnit přerušovaný krevní proud v plynulý – nárazníková funkce. Za normálních okolností se během systoly dostává do periferních tkání asi 40 % tepového objemu, zbylá krev zůstává ve velkých tepnách a je vypuzována během diastoly. Při selhání této nárazníkové funkce centrálních tepen dochází k nadměrnému zvýšení systolického krevního tlaku v centrálním řečišti a tím ke zvýšení afterloadu levé komory [2]. V posledních letech narůstá počet důkazů o uplatnění tuhosti arteriální stěny v patofyziologii srdečního selhání. Zvýšený pulzní tlak je asociován se zvýšenou kardiovaskulární morbiditou a mortalitou u pacientů s asymptomatickou dysfunkcí levé komory a s mírným srdečním selháním. Naopak snížený pulzní tlak je dle některých prací asociován se zvýšenou mortalitou u pacientů s akutní dekompenzací chronického srdečního selhání a u pacientů s pokročilým srdečním selháním a je taktéž asociován se zvýšenými hodnotami B-typu natriuretického peptidu (BNP) [3,4]. U pacientů se systolickým srdečním selháním bylo zaznamenáno kratší trvání ejekce dle analýzy pulzní vlny [3], naopak u pacientů s diastolickou dysfunkcí levé komory srdeční bylo zjištěno delší trvání ejekce. Analýza pulzní vlny tedy může být nápomocna v rozlišení míry diastolické a systolické dysfunkce levé komory srdeční [5].
Cíl
Cílem naší práce bylo zjistit velikost pulzního tlaku, augmentačního tlaku, augmentačního indexu a dalších parametrů pulzní vlny pomocí její neinvazivní analýzy u pacientů hospitalizovaných pro akutní dekompenzaci chronického systolického srdečního selhání.
Metodika
Do studie byli, po podpisu informovaného souhlasu, zařazeni pacienti starší 18 let přijatí na Interní kardiologickou kliniku Fakultní nemocnice Brno s diagnózou akutní dekompenzace chronického systolického srdečního selhání splňující diagnostická kritéria Evropské kardiologické společnosti z roku 2005 a vyžadující intravenózní léčbu. Anamnéza chronického srdečního selhání musela být delší než tři měsíce a pacienti museli mít ejekční frakci levé komory (EF LK) ≤ 45 % (měřeno v průběhu posledních šesti měsíců). Mezi vyřazovací kritéria patřily především akutní koronární syndrom, pravostranné srdeční selhání zapříčiněné primárně plicním onemocněním, anamnéza transplantace srdce nebo čekatelé na transplantaci, nestabilní angina pectoris nebo onemocnění koronárních tepen pravděpodobně vyžadující kardiochirurgickou revaskularizaci myokardu – coronary artery bypass graft (CABG) nebo perkutánní koronární intervenci (PCI) před randomizací, anamnéza nebo přítomnost jakéhokoli jiného onemocnění s prognózou přežití méně než tři roky, přítomnost hemodynamicky signifikantní mitrální stenózy nebo mitrální regurgitace, kromě mitrální regurgitace způsobené sekundárně dilatací levé komory, přítomnost hemodynamicky významné aortální stenózy, hemodynamicky významné obstrukce výtokového traktu levé komory a nespolupráce pacienta. Všichni pacienti podstoupili kompletní klinické (anamnéza, objektivní vyšetření, základní fyzikální měření) a biochemické vyšetření včetně stanovení plazmatických hladin BNP při přijetí a před propuštěním z nemocnice, v ostatní dny hospitalizace bylo provedeno běžné klinické vyšetření včetně základních fyzikálních měření a nutných laboratorních vyšetření a pacient byl monitorován a léčen dle standardů péče o nemocné s akutním srdečním selháním a dle aktuální potřeby. Krevní tlak byl měřen konvenčním způsobem za použití automatického manometru OMRON M7 dle platných doporučení České kardiologické společnosti z roku 2008. V den přijetí bylo nemocným provedeno elektrokardiografické vyšetření (EKG) a rentgen (RTG) hrudníku. Klidové transtorakální echokardiografické vyšetření bylo prováděno na přístroji GE Healthcare Vivid 7 sondou M4S ze standardních projekcí (parasternální dlouhá a krátká osa, apikální dvou - a čtyřdutinová, subxifoideální) po stabilizaci stavu před propuštěním nemocného do domácí péče. Průměrné hodnoty byly kalkulovány ze tří měření. Ke kalkulaci ejekční frakce levé komory byla využita metoda sumace disků, označovaná jako Simpsonova formule. Před propuštěním bylo taktéž pacientům provedeno neinvazivní vyšetření přístrojem SphygmoCor Px, kterým byla provedena analýza pulzní vlny z radiální artérie. Za použití integrovaných transformačních funkcí Cardiovascular Management Suite Version 8 byla provedena kalkulace pulzního tlaku (PP), augmentačního tlaku (AP) a indexu (AI) včetně korekce na tepovou frekvenci 75/min, doby trvání ejekční fáze (ED) a indexu subendokardiální viability (SEVR). Tento přístroj tedy umožňuje odvození centrální aortální tlakové pulzní vlny pomocí matematické transformace. V průběhu vyšetření probíhala kontrola kvality záznamu následujícími způsoby: analýza pulzní vlny – vizuálně přijatelné nahrávky pulzní křivky byly akceptovány pouze v případě, že výkyvy amplitudy či délky pulzů byly do 5 % a průměrná amplituda byla vyšší než pulz 80 mV a index kvality hodnocený softwarově byl > 80 %. U každého pacienta byla taktéž zaznamenána veškerá terapie od přijetí až po propuštění. Stanovení BNP probíhalo v certifikované centrální laboratoři FN Brno do 20 min od odběru krevního vzorku. Ke stanovení BNP bylo využito setů Axsym od firmy Abbott. Odběr žilní krve byl součástí běžných odběrů v rámci hospitalizace a byl prováděn za standardních podmínek z kubitální žíly. Získaná data byla statisticky vyhodnocena v Institutu biostatistiky a analýz Masarykovy Univerzity Brno. Základní popis získaných dat je prováděn s použitím standardních statistických metod, pro kontinuální proměnné pomocí průměru, mediánu, směrodatné odchylky, minima a maxima, pro kategoriální proměnné pomocí tabulek četnosti. Pro stanovení rozdílů v kontinuálních proměnných mezi dvěma skupinami nemocných je použit dle normality t-test nebo Mann-Whitney test. Vztah mezi dvěma kategoriálními proměnnými je stanoven pomocí Fisher exact testu nebo chí-square testu. Hodnoty p < 0,05 jsou brány jako standardní limit pro statistickou významnost, případně jsou korigovány na násobné testování. Ke statistickému zpracování dat byl využit software SPSS 18.0.2 a Statistica 9.1. Studie byla schválena Etickou komisí Fakultní nemocnice Brno.
Charakteristika souboru
Do studie bylo zařazeno 130 pacientů (77 % mužů, 23 % žen), základní charakteristika souboru včetně rozdílů mezi muži a ženami je uvedena v tab. 1a a 1b.
Tab. 1a. Základní charakteristika pacientů – spojité parametry. 
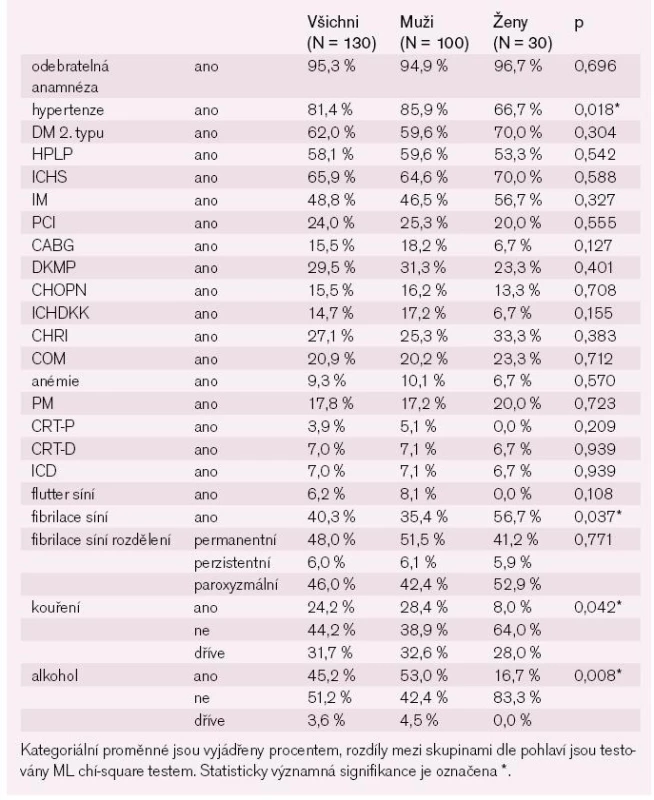
Tab. 1b. Základní charakteristika pacientů – kategoriální prametry. 
Všichni nemocní v našem souboru měli systolickou dysfunkci levé komory a jen necelá čtvrtina těchto nemocných měla zachované diastolické plnění levé komory. Na vstupním RTG hrudníku jsme nalezli u více než 80 % nemocných známky městnání na plicích a u téměř poloviny nemocných fluidothorax. Více než polovina nemocných měla při přijetí otoky dolních končetin a více než 88 % jich mělo klinické známky městnání na plicích. Ortopnoi udávala více než polovina nemocných. Mezi nejčastější komorbidity patřila hypertenze, diabetes mellitus 2. typu a hyperlipoproteinemie, nezanedbatelný je ale samozřejmě i poměrně vysoký výskyt fibrilace síní, která je ale téměř v polovině případů jen paroxyzmální. Jednotlivé komorbidity včetně rozdílů mezi muži a ženami jsou uvedeny v tab. 2.
V etiologii chronického srdečního selhání převažuje ischemická choroba srdeční (65,9 %) nad dilatační kardiomyopatií (29,5 %) a ostatními příčinami (kardiomyopatie po chemoterapii, posttachykardická kardiomyopatie a kardiomyopatie pozánětlivá). Spojité a kategoriální biochemické charakteristiky pacientů ukazují tab. 3a a 3b.
Tab. 3a. Biochemické charakteristiky pacientů – spojité parametry. 
Tab. 3b. Biochemické charakteristiky pacientů – kategoriální parametry. 
Kromě rozdílu v koncentraci hemoglobinu jsme nenalezli žádný další rozdíl v uvedených biochemických parametrech mezi muži a ženami. Za hospitalizace jsme u pacientů zaznamenali statisticky významný pokles BNP (p < 0,001). Více než třetina nemocných měla pozitivní troponin T v rámci akutní dekompenzace chronického srdečního selhání bez souvislosti s akutním koronárním syndromem. Téměř tři čtvrtiny nemocných měli dlouhodobě zavedenou léčbu blokátory renin-angiotenzin-aldosteronového systému (RAAS) a betablokátory (tab. 4).
Table 2. Farmakoterapie – chronická (dle anamnézy). 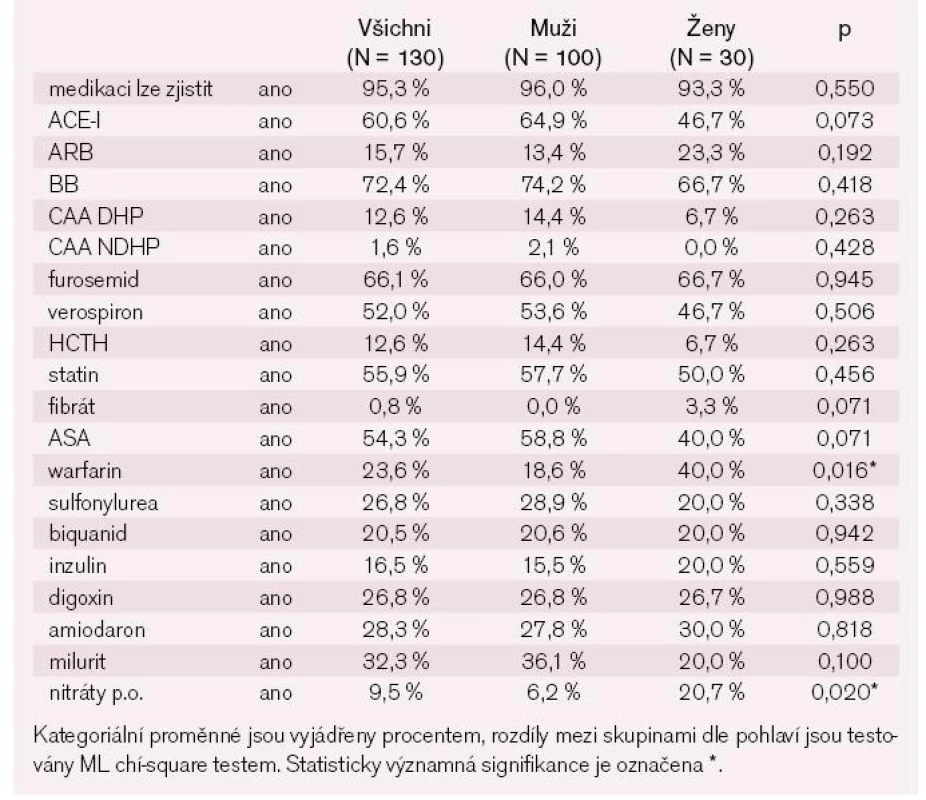
Při propuštění se zastoupení těchto lékových skupin mírně zvýšilo. Statisticky významně ale narostl počet pacientů léčených kličkovými diuretiky a blokátory mineralokortikoidních receptorů. I přes fakt, že jakoukoli formou fibrilace síní trpí více než 40 % nemocných v našem souboru, je pouze necelých 24 % pacientů léčeno p.o. antikoagulační terapií (tab. 5).
Table 3. Farmakoterapie při propuštění. 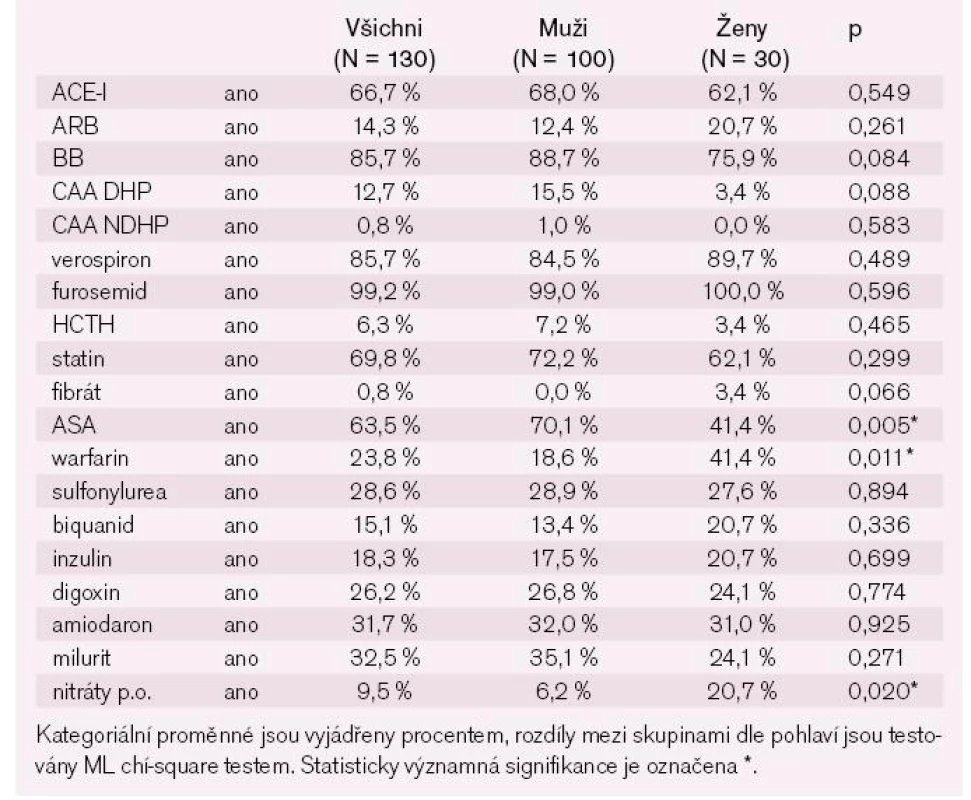
V tab. 6 je uvedena vybraná farmakologická i nefarmakologická terapie za hospitalizace. Většina nemocných byla v průběhu hospitalizace léčena kličkovými i.v. diuretiky, délku jejich podávání a kumulativní dávku ukazuje tab. 7.
Table 4. Léčba za hospitalizace (nefarmakologická + farmakologická) – kategoriální parametry. 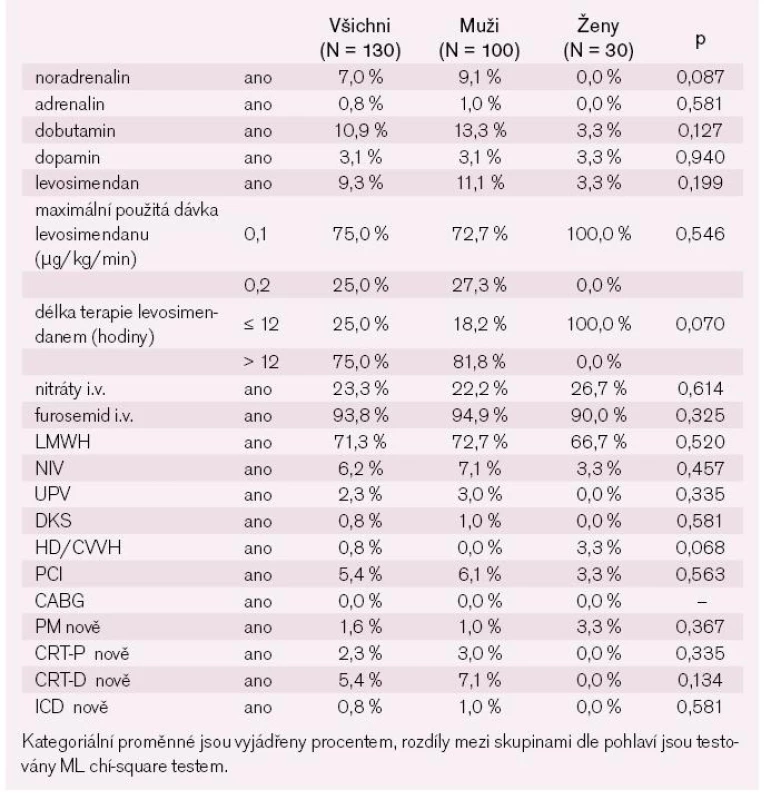
Table 5. Léčba za hospitalizace – spojité parametry. 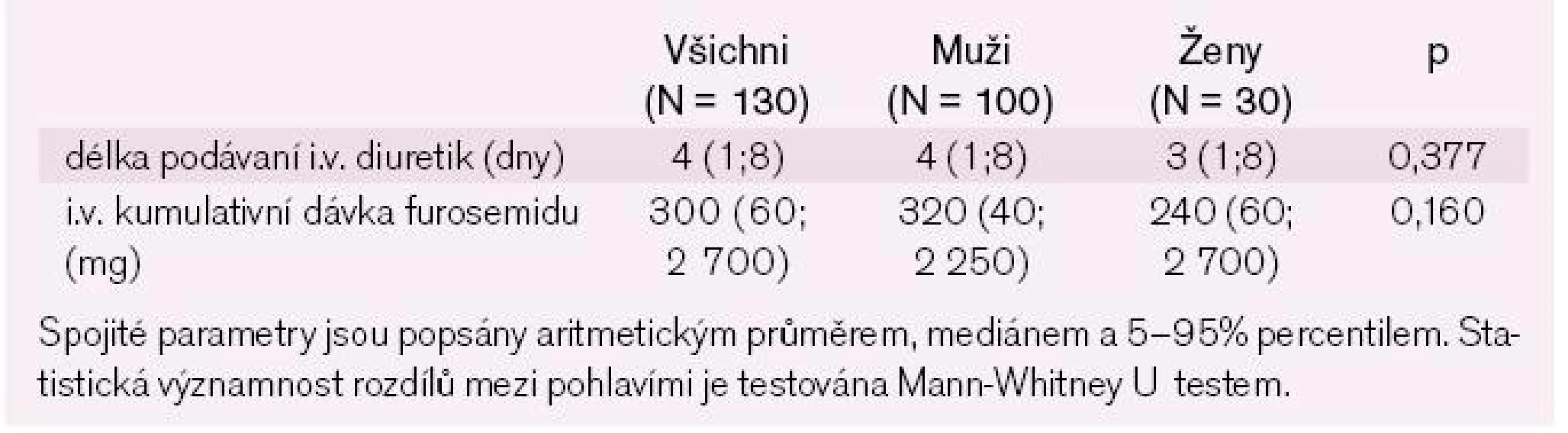
Z pozitivně inotropních léků byl v léčbě akutní dekompenzace chronického srdečního selhání nejvíce využíván dobutamin následovaný levosimendanem. Cílové dávky 0,2 µg/kg/min však dosáhlo jen 25 % nemocných. Umělou plicní ventilací (invazivní a neinvazivní) bylo léčeno 8,5 % nemocných. Délku hospitalizace nemocných ukazuje tab. 8.
Plicní edém se vyskytl u čtvrtiny nemocných a kardiogenní šok u 2,4 % nemocných, ostatní nemocní měli dle Killip//Forresterovy klasifikace mírné srdeční selhání s dominancí levostranného srdečního selhání dozadu bez zjevného vyvolávajícího faktoru (tab. 9). Mezi nejčastější komplikace za hospitalizace patřila infekce, zejména respirační (tab. 10).
Table 7. Charakteristika ASS – kategoriální parametry. 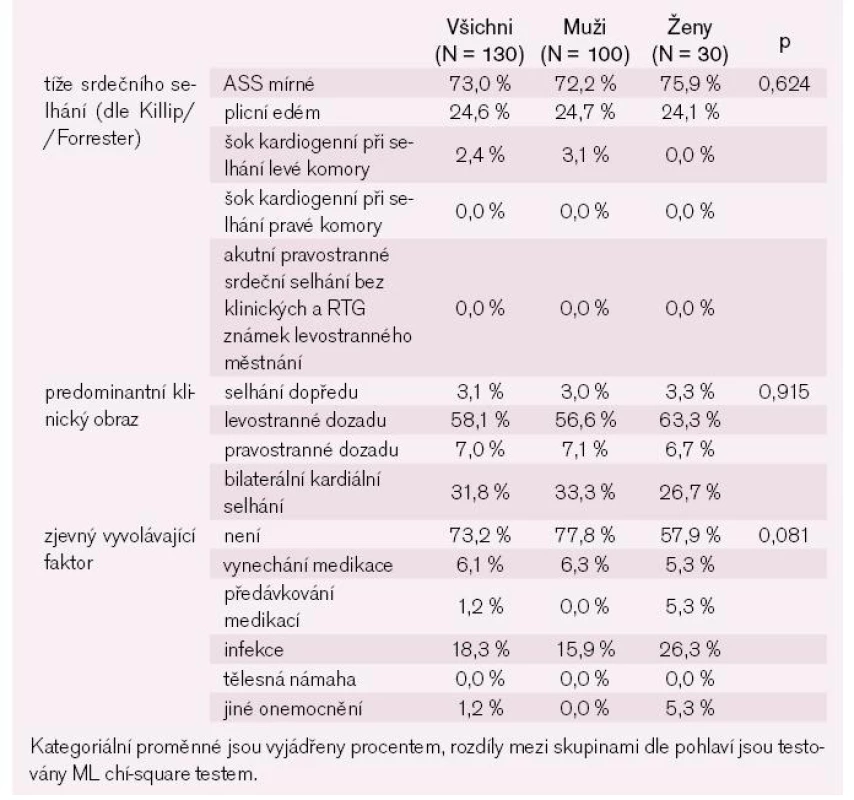
Table 8. Komplikace za hospitalizace – kategoriální parametry. 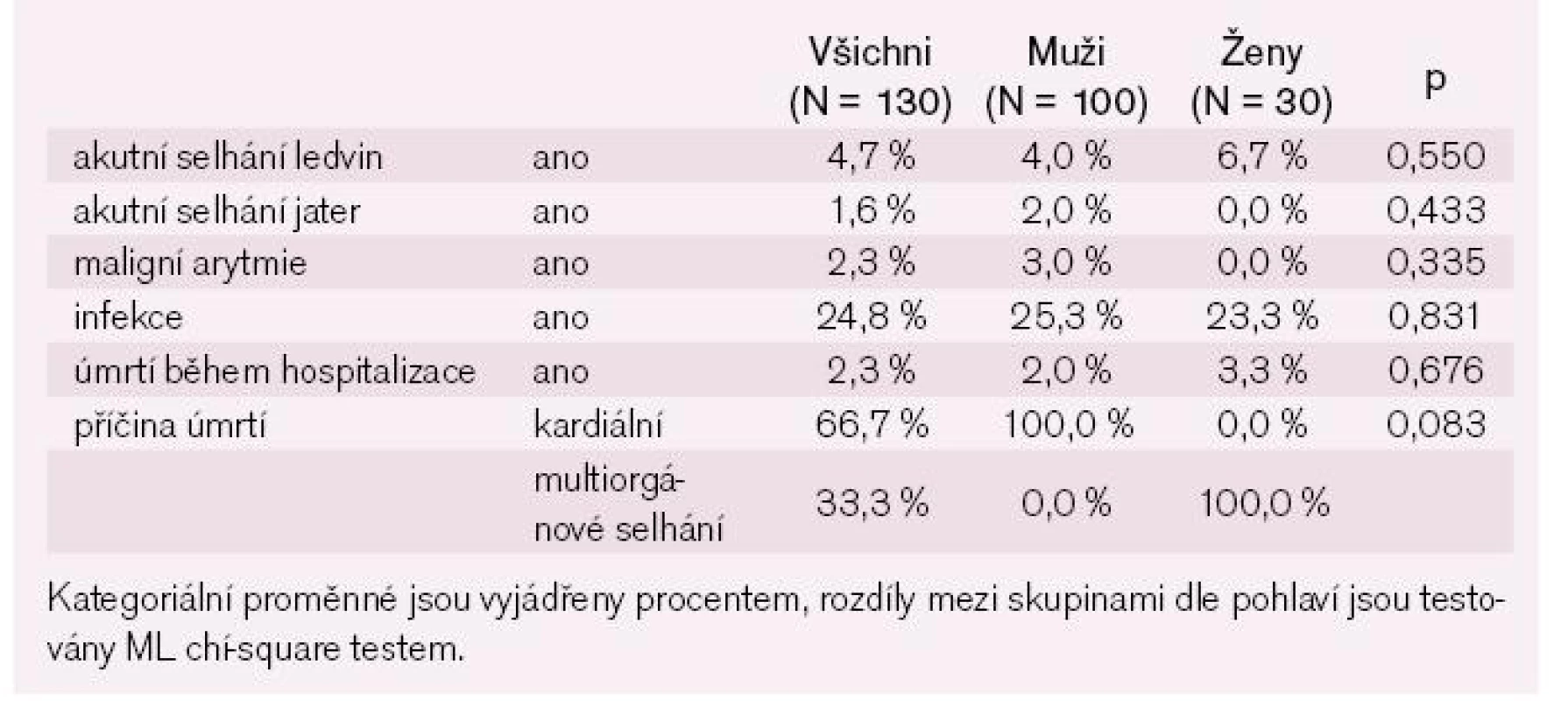
Výsledky
Výsledky neinvazivní analýzy pulzní vlny ukazuje tab. 11. Nedostatečně kvalitní záznam pulzní vlny jsme zaznamenali u 17 mužů a tří žen, proto jsme pulzní vlnu analyzovali jen u 110 nemocných. Po adjustaci na věk a pohlaví mělo snížený pulzní tlak 49 %, normální 44,5 % a zvýšený 6,5 % nemocných; snížený augmentační tlak 60,4 %, normální 34,6 % a zvýšený 5 % nemocných; snížený augmentační index korigovaný na tepovou frekvenci 75/min 42,8 %, normální 50,5 % a zvýšený 6,7 % nemocných; sníženou dobu trvání ejekční fáze 65,5 %, normální 31,8 % a zvýšenou 2,7 % nemocných; snížený index subendokardiální viability 6,4 %, normální 37,3 % a zvýšený 56,3 % nemocných.
Table 9. Neinvazivní analýza pulzní vlny – spojité parametry. 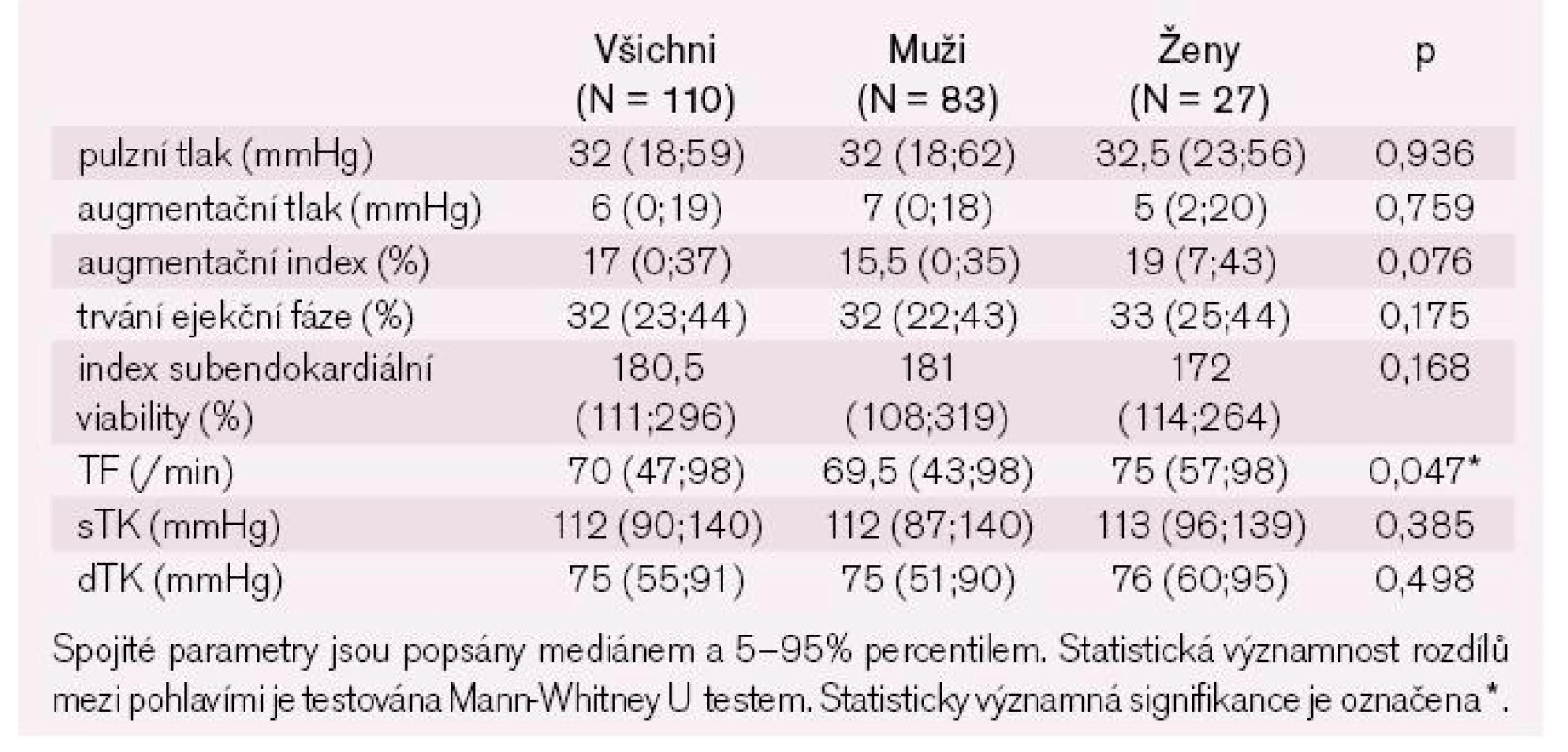
Diskuze
V posledních letech dochází k neustálému nárůstu výskytu srdečního selhání, zvyšuje se počet hospitalizací těchto nemocných a akutní srdeční selhání u nich patří mezi nejčastější příčiny, zejména u starší populace. Přibližně polovina nemocných s akutním srdečním selháním je do jednoho roku rehospitalizována, což vede k nárůstu ekonomické náročnosti léčby srdečního selhání. Za hospitalizace umírá až třetina a do jednoho roku až polovina nemocných hospitalizovaných pro akutní srdeční selhání [6]. Pro optimalizaci péče o nemocné s akutním srdečním selháním je tedy velmi důležité stanovení jejich prognózy. Naše studie má v budoucnu (dostatečně dlouhý follow-up) za cíl identifikovat nejvýznamnější neinvazivní prognostické ukazatele a vytvořit model kombinující tyto parametry k co nejpřesnější identifikaci nemocných ohrožených nepříznivým průběhem onemocnění se zaměřením na neinvazivní analýzu pulzní vlny, plazmatické hladiny natriuretických peptidů a na echokardiografické parametry. V tomto článku se však zatím věnujeme jen základní charakteristice souboru a výsledkům neinvazivní analýzy pulzní vlny.
Od konce minulého století narůstá počet důkazů o pozitivní asociaci pulzního tlaku, augmentačního indexu a rychlosti šíření pulzní vlny, tedy parametrů cévní tuhosti, s vyšším rizikem kardiovaskulární morbidity a mortality [7–13].
Taktéž v souvislosti s prognózou nemocných se srdečním selháním je v posledních letech stále častěji diskutována problematika cévní tuhosti a narůstá počet důkazů o jejím uplatnění v patofyziologii srdečního selhání. Zvýšený pulzní tlak je asociován se zvýšenou kardiovaskulární morbiditou a mortalitou u pacientů s asymptomatickou dysfunkcí levé komory anebo s mírným srdečním selháním [14]. Tento nález je připisován škodlivému účinku snížené poddajnosti velkých cév, která je následována porušením nárazníkové funkce a zvýšením zátěže levé komory. Zvýšená cévní tuhost má tedy škodlivé účinky na myokard kvůli zvýšenému afterloadu, zvýšené spotřebě kyslíku myokardem, narušené relaxaci a subendokardiální ischemii. Jakmile však dochází k progresi srdečního selhání, může se vztah mezi pulzním tlakem a prognózou změnit. Vlastnosti primární tlakové vlny jsou závislé především na funkci levé komory a na vlastnostech centrálních elastických tepen, zatímco sekundární vlna je dána především rychlostí šíření tlakové vlny a místem odrazu. Výsledná tlaková vlna pak vzniká sumací těchto vln [2]. Pulzní tlak je tedy determinován zejména tepovým objemem a tepennou compliance. Když jsou systolická funkce levé komory a tepový objem normální, je elevovaný pulzní tlak dán především snížením elasticity velkých cév. U pacientů po infarktu myokardu s asymptomatickou dysfunkcí levé komory či s mírným srdečním selháním je pulzní tlak ovlivněn jak levokomorovou dysfunkcí, tak poklesem elasticity velkých cév. U těchto pacientů se však zdá důležitější vliv tuhosti cévní stěny. U pacientů s těžkým srdečním selháním je dominantní pokles tepového objemu v rámci srdečního selhání, zatímco tuhost cévní stěny ustupuje do pozadí [3]. Pulzní tlak je tedy ovlivněn zejména systolickou a diastolickou dysfunkcí levé komory [15]. Pulzní tlak u těchto nemocných koreluje nejen s ejekční frakcí levé komory, ale taktéž se srdečním indexem [16]. Snížený pulzní tlak je dle některých prací asociován se zvýšenou mortalitou u pacientů s akutní dekompenzací chronického srdečního selhání [15] a u pacientů s pokročilým srdečním selháním a je taktéž asociován se zvýšenými hodnotami B-typu natriuretického peptidu [17].
Podobně jako pulzní tlak i augmentační tlak a index jsou ovlivněny hemodynamickými faktory, jako jsou střední arteriální tlak, ejekční frakce levé komory [1] a tepová frekvence, což může ovlivnit jejich prognostickou hodnotu u srdečního selhání [16]. Nejsou tedy pravděpodobně vhodné k posuzování míry působení odražené vlny na celkovou amplitudu tlakové vlny u pacientů se srdečním selháním. Pokles augmentačního tlaku a indexu by tedy neměl být špatně interpretován jako důkaz zpožděného nebo sníženého odrazu vln u pacientů se srdečním selháním. Naopak, je to právě selhávající myokard, který není schopný vytvářet dostatečný tlak, a proto se odražená vlna nemůže projevit na tlakové vlně. Augmentační tlak a augmentační index jsou dle některých prací nezávislými prediktory kardiovaskulární morbidity a mortality, zejména u pacientů s ischemickou chorobou srdeční podstupujících perkutánní koronární intervenci [13]. Neexistují však zatím dostatečně silné důkazy o vlivu těchto parametrů na prognózu nemocných se srdečním selháním.
V naší studii jsme vyšetřili pacienty s poměrně vysokým průměrným věkem a s vysokým výskytem hypertenze a dalších komorbidit, které mohou ovlivnit vlastnosti cév. Pokud by se jednalo o pacienty bez srdečního selhání, očekávali bychom u nich zvýšený pulzní a augmentační tlak a taktéž zvýšený augmentační index, naši pacienti však měli v průměru těžkou systolickou dysfunkci levé srdeční komory, čímž se u nich projevil hemodynamický vliv selhávající levé komory na tyto parametry. U více než poloviny jsme zaznamenali snížený pulzní i augmentační tlak. Brachiální pulzní tlak nebyl v naší práci předmětem výzkumu, neboť dle některých prací [1] je centrální pulzní tlak na rozdíl od brachiálního pulzního tlaku asociován s ejekční frakcí levé komory. Navíc je u pacientů s kardiovaskulárním rizikem, zejména u pacientů se srdečním selháním, centrální pulzní tlak na rozdíl od brachiálního pulzního tlaku lepším ukazatelem prognózy těchto nemocných.
U pacientů se systolickým srdečním selháním bylo zaznamenáno kratší trvání ejekce dle analýzy pulzní vlny [3], což se potvrdilo i v naší studii. Naopak u pacientů s diastolickou dysfunkcí levé komory srdeční bylo zjištěno delší trvání ejekce. Analýza pulzní vlny tedy může být nápomocna v rozlišení míry diastolické a systolické dysfunkce levé komory srdeční [5].
Závěr
U více než poloviny nemocných hospitalizovaných pro akutní dekompenzaci chronického systolického srdečního selhání jsme po stabilizaci jejich stavu nalezli snížený pulzní i augmentační tlak, taktéž jsme téměř u poloviny těchto nemocných nalezli snížený augmentační index korigovaný na tepovou frekvenci 75/min. Více než 2/3 nemocných mělo sníženou dobu trvání ejekce.
Limitace
Do naší studie byly zařazeni všichni nemocní hospitalizovaní na naší klinice pro akutní dekompenzaci chronického srdečního selhání splňující vstupní kritéria, čímž jsme se snažili omezit selekci pacientů. K určité selekci však dochází již před hospitalizací na našem pracovišti (kardiologická klinika v rámci fakultní nemocnice). Další limitací souboru je jeho velikost.
Podpořeno grantem IGA MZ ČR 10422-3/2009.
Seznam zkratek
ACE-I – inhibitor angiotenzin konvertujícího enzymu, AI – augmentační index, AP – augmentační tlak, AP CCS – angina pectoris dle Canadian Cardiac Society, ARB – blokátor receptoru 1 pro angiotenzin II, ASA – kyselina acetylosalicylová, BB – betablokátor, BMI – body mass index, BNP – B-typ natriuretického peptidu, CAA DHP – blokátor kalciového kanálu dihydropyridinového typu, CAA NDHP – blokátor kalciového kanálu non-dihydropyridinového typu, CABG – coronary artery bypass graft, CHOPN – chronická obstrukční bronchopulmonální nemoc, CHRI – chronická renální insuficience, COM – cévní onemocnění mozku, CRP – C-reaktivní protein, CRT-D – biventrikulární kardiostimulátor + ICD, CRT-P – biventrikulární kardiostimulátor, DKK – dolní končetiny, DKMP – dilatační kardiomyopatie, DKS – dočasná kardiostimulace, DM – diabetes mellitus, ED – doba trvání ejekční fáze, EF LK – ejekční frakce levé komory, EKG – elektrokardiografické vyšetření, GF – glomerulární filtrace, Hb – hemoglobin, HCTH – hydrochlorothiazid, HD/CVVH – hemodialýza/kontinuální veno-venozní hemofiltrace, HDL – high density lipoprotein, HPLP – hyperlipoproteinemie, ICD – implantabilní kardioverter defibrilátor, ICHDKK – ischemická choroba dolních končetin, ICHS – ischemická choroba srdeční, IM – infarkt myokardu, KM – kyselina močová, KTI – kardiothorakální index, LBBB – blokáda levého Tawarova raménka, LDL – low density lipoprotein, LK – levá komora, LMWH – low molecular weight heparin (nízkomolekulární heparin), NIV – neinvazivní umělá plicní ventilace, NYHA – New York Heart Association klasifikace, PCI – perkutánní koronární intervence, PM – pacemaker (kardiostimulátor), PP – pulzní tlak, PWV – rychlost pulzní vlny, RAAS – renin-angiotenzin aldosteronový systém, RBBB – blokáda pravého Tawarova raménka, RTG – rentgen, SEVR – index subendokardiální viability, SD – směrodatná odchylka, TF – tepová frekvence, TG – triglyceridy, dTK – diastolický krevní tlak, sTK – systolický krevní tlak, UPV – invazivní umělá plicní ventilace
Doručeno do redakce 17. 10. 2011
Přijato po recenzi 1. 11. 2011
MUDr. Ondřej Ludka, Ph.D.1,4
MUDr. Viktor Musil1
MUDr. Roman Štípal1
MUDr. Zbyněk Pozdíšek, Ph.D.3
RNDr. Jiří Jarkovský, Ph.D.2
doc. RNDr. Ladislav Dušek, Ph.D.2
prof. MUDr. Jindřich Špinar, CSc.1,41 Interní kardiologická klinika FN Brno a LF MU, Brno
2 Institut biostatistiky a analýz MU, Brno
3 Kardiochirurgická klinika FN Olomouc a LF UP, Olomouc
4 ICRC Brno
oludka@fnbrno.cz
Sources
1. Weber T, Auer J, Lamm G et al. Arterial stiffness, central blood pressure, and wave reflections in cardiomyopathy – implications for risk stratification. J Card Fail 2007; 13 : 353–359.
2. Rosa J, Widimský J jr. Charakteristika velkých tepen u arteriální hypertenze. Cor Vasa 2011; 53 : 418–422.
3. Voors AA, Petrie CJ, Petrie MC et al. Low pulse pressure is independently related to elevated natriuretic peptides and increased mortality in advanced chronic heart failure. Eur Heart J 2005; 26 : 1759–1764.
4. Mitchel GF, Tardif JC, Arnold JM et al. Pulsatile Hemodynamics in Congestive Heart Failure. Hypertension 2001; 38 : 1433–1439.
5. O‘Rourke MF, Pauca A, Jiang XJ. Pulse wave analysis. Br J Clin Pharmacol 2001; 51 : 507–522.
6. Zannad F, Mebazaa A, Juillière Y et al. EFICA Investigators. Clinical profile, contemporary management and one-year mortality in patients with severe acute heart failure syndromes: The EFICA study. Eur J Heart Fail 2006; 8 : 697–705.
7. Benetos A, Safar M, Rudnichi A et al. Pulse pressure: a predictor of long-term cardiovascular mortality in a French male population. Hypertension 1997; 30 : 1410–1415.
8. Fang J, Madhavan S, Cohen H et al. Measure of blood pressure and myocardial infarction in treated hypertensive patients. J Hypertens 1995; 13 : 413–419.
9. Laurent S, Boutouyrie P, Asmar R et al. Aortic stiffness is an independent predictor of all-cause and cardiovascular mortality in hypertensive patients. Hypertension 2001; 37 : 1236–1241.
10. Mattace-Raso FU, van der Cammen TJ, Hofman A et al. Arterial stiffness and risk of coronary heart disease and stroke. The Rotterdam study. Circulation 2006; 113 : 657–663.
11. Weber T, Auer J, O’Rourke MF et al. Arterial stiffness, wave reflections, and the risk of coronary artery disease. Circulation 2004; 109 : 184–189.
12. London GM, Blacher J, Pannier B et al. Arterial wave reflections and survival in end-stage renal failure. Hypertension 2001; 38 : 434–438.
13. Weber T, Auer J, O’Rourke MF et al. Increased arterial wave reflections predict severe cardiovascular events in patients undergoing percutaneous coronary interventions. Eur Heart J 2005; 26 : 2657–2663.
14. Domanski MJ, Mitchell GF, Norman JE et al. Independent prognostic information provided by sphygmomanometrically determined pulse pressure and mean arterial pressure in patients with left ventricular dysfunction. J Am Coll Cardiol 1999; 33 : 951–958.
15. Aronson D, Burger AJ. Relation between pulse pressure and survival in patients with decompensated heart failure. Am J Cardiol 2004; 93 : 785–788.
16. Tartiere JM, Logeart D, Safar ME et al. Interaction between pulse wave velocity, augmentation index, pulse pressure and left ventricular function in chronic heart failure. J Human Hypertens 2006; 20 : 213–219.
17. Shah MR, Hasselblad V, Stinnett SS et al. Hemodynamic profiles of advanced heart failure: association with clinical characteristics and long-term outcomes. J Card Fail 2001; 7 : 105–113.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2011 Issue 4-
All articles in this issue
- Nesarkomerické formy hypertrofické kardiomyopatie v dospělosti
- Peripartální kardiomyopatie
- Tachykardií indukovaná kardiomyopatie
- Není hypertrofie jako hypertrofie aneb Nezapomínejme na amyloidózu
- Kalcifikace perikardu
- Atherosclerosis of the intracranial arteries – current view, 1st part.
- Neinvazivní analýza pulzní vlny u pacientů s akutní dekompenzací chronického systolického srdečního selhání
- Ticagrelor a studie PLATO
- Mladá žena se synkopami
- Raritní příčina dysfunkce mechanické aortální chlopně
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Není hypertrofie jako hypertrofie aneb Nezapomínejme na amyloidózu
- Kalcifikace perikardu
- Nesarkomerické formy hypertrofické kardiomyopatie v dospělosti
- Peripartální kardiomyopatie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career