-
Medical journals
- Career
Terapie dyslipidemie u pacienta se svalovou dystrofií: kazuistika
Authors: Ľubica Cibičková; David Karásek
Authors‘ workplace: III. interní klinika – nefrologická, revmatologická a endokrinologická LF UP a FN Olomouc
Published in: AtheroRev 2019; 4(1): 35-37
Category:
Overview
Kazuistika popisuje případ pacienta se svalovou dystrofií a smíšenou dyslipidemií. Pacient prodělal infarkt myokardu a byl indikován k terapii dyslipidemie v sekundární prevenci, avšak pro výraznou elevací kreatinkinázy byla terapie statiny kontraindikována. Vzhledem k tomu, že ani při podávání kombinace ezetimibu a fenofibrátu nebylo dosaženo cílových hodnot LDL-cholesterol, byla zvolena terapie PCSK9-inhibitorem s výbornou snášenlivostí i potřebným poklesem hodnot LDL-cholesterolu.
Klíčová slova:
PCSK9-inhibitory – smíšená dyslipidemie – svalová dystrofie
Úvod
Kardiovaskulární onemocnění zůstávají v naší zemi stále nejčastější příčinou mortality a morbidity. Dyslipidemie je jeden z kauzálních parametrů, jehož ovlivněním můžeme kardiovaskulární (KV) riziko výrazně snížit. Volba vhodného hypolipidemika bývá v cíleném ovlivnění lipidového spektra často klíčová [1]. Není pochyb, že v první linii ovlivnění KV-rizika stojí statiny. Na druhou stranu existují faktory, které nás nutí léčbu individualizovat a postupovat mimo zvyklá schémata.
Jedním z těchto faktorů je myopatie s elevací hodnot kreatinkinázy (CK). Dle aktuálních doporučení European Atherosclerotic Society z roku 2016 je před nasazením statinů vhodné provést vyšetření CK, aby byli identifikováni pacienti, u kterých jsou tyto léky kontraindikovány [2,3]. Dle těchto guidelines není terapie statinem doporučena při elevaci CK > 4násobek horní hranice normy a má být zvážena alternativní terapie (bez uvedení bližší specifikace). Terapie inhibitorem proprotein konvertázy subtilizin/kexin typu 9 (PCSK9i) má být zvážena u pacientů netolerujících statiny [2]. Pro pacienty s dyslipidemií a kontraindikací statinů tedy nemáme jasné doporučení, která hypolipidemika bychom měli zvolit v první linii, a je nutná výše zmiňovaná individualizace postupu.
V naší kazuistice popisujeme případ pacienta se svalovou dystrofií, u kterého jsme řešili problematiku hypolipidemické terapie při kontraindikaci podání statinů.
Popis případu
48letý muž byl odeslán do lipidové ambulance s žádostí o nastavení terapie smíšené dyslipidemie. Terapie hypolipidemiky byla indikována již v sekundární prevenci. U pacienta byl dle zprávy zkoušen cholestyramin pouze s parciálním efektem a statin byl pro myopatii vysazen. Jednalo se o muže s dlouholetou anamnézou nedostatečně kompenzované arteriální hypertenze, s vertebrogenním algickým syndromem, asthma bronchiale a cholecystolitiázou. Před rokem prodělal akutní infarkt myokardu, který si vyžádal našití trojnásobného aortokoronárního by-passu. Zároveň byla zjištěna hepatopatie, myopatie a následně také diabetes mellitus 2. typu. V rodinné anamnéze se nevyskytovala předčasná manifestace kardiovaskulárních onemocnění ani dyslipidemie.
Při vstupním laboratorním vyšetření byla u pacienta zjištěna smíšená dyslipidemii s hodnotami celkového cholesterolu 7,26 mmol/l, triglyceridy 8,02 mmol/l, LDL-cholesterol 3,34 mmol/l (přímé stanovení), HDL-cholesterol 0,99 mmol/l, non-HDL 6,27 mmol/l, mírně elevované jaterní testy (ALT 3,14 µkat/l, AST 2,46 µkat/l) a výrazně zvýšená hodnota kreatinkinázy (CK 62,38 µkat/l). Hepatopatie byla standardně vyšetřena včetně ultrasonografie (USG), byly vyloučeny virové hepatitidy, hemochromatóza, autoimunitní onemocnění jater, toxonutritivní poškození a etiologicky byl stav uzavřen jako steatóza jater při metabolickém syndromu. Diferenciální diagnostiku zajistila Neurologická klinika FN Brno. Zahrnovala zobrazení svalů pletence pánevního (difuzní tuková atrofie svalové tkáně) magnetickou rezonancí (Magnetic Resonance Imaging – MRI) , elektromyografii (vyšší výskyt polyfazií v jehlové EMG, bez dalších abnormit), svalovou biopsii (nevýrazná svalová léze typu minimal change myopathy) a genetické vyšetření (identifikovány sekvenční varianty v genu ANO5). Na základě závěrů z provedených vyšetření byla stanovena diagnóza svalové dystrofie (Limb-Girdle Muscular Dystrophy – LGMD) typu 2l s autosomálně recesivní dědičností.
Naším úkolem bylo pacientovi nastavit terapii dyslipidemie. Cílovou hodnotou LDL-cholesterolu v sekundární prevenci byla u tohoto pacienta hodnota < 1,8 mmol/l, které zdaleka nedosahoval. Při našem vstupním vyšetření byl poučen o dietních a režimových opatřeních včetně omezení příjmu nasycených mastných kyselin a jednoduchých sacharidů. Statin jsme nenasazovali s respektováním aktuálních doporučení European Atherosclerotic Society z roku 2016, podle nichž není terapie statinem doporučena při elevaci CK > 4násobek horní hranice normy [2]. Farmakoterapii jsme zahájili podáváním ezetimibu především s cílem snížit LDL-cholesterol. Při režimových opatřeních a terapii ezetimibem došlo k poklesu hladiny triacylglycerolů/triglyceridů (TAG 7,7 mmol/l), avšak hladina cholesterolu zůstávala nadále vysoká (celkový cholesterol 6,3 mmol/l). S cílem dále snížit hladinu triglyceridů jsme k terapii ezetimibem přidali fenofibrát a výsledkem bylo zlepšení hodnot lipidogramu – celkový cholesterol 4,98 mmol/l, TAG 3,36 mmol/l, LDL-cholesterol 2,58 mmol/l, non-HDL cholesterol 4,1 mmol/l a apolipoprotein B 1,24 g/l. Přesto stále nebylo dosaženo cílové hodnoty LDL-cholesterolu, a proto jsme se nakonec rozhodli zažádat zdravotní pojišťovnu o schválení terapie inhibitorem PCSK9. Žádost byla schválena, a proto byl pacientovi do kombinace přidán evolokumab v dávce 140 mg jednou za dva týdny subkutánní injekcí. Za dva měsíce při této terapii (kombinace ezetimib, fenofibrát, evolokumab) poklesl celkový cholesterol na hodnotu 2,96 mmol/l, TAG 2,96 mmol/l, LDL-cholesterol 1,21 mmol/l. Po celou dobu terapie hypolipidemiky docházelo k zcela nezávislému kolísání hodnot kreatinkinázy (tab. 1). Pacient terapii toleroval subjektivně velmi dobře, zhoršení svalových potíží neudával.
Table 1. Vývoj laboratorních hodnot při terapii dyslipidemie 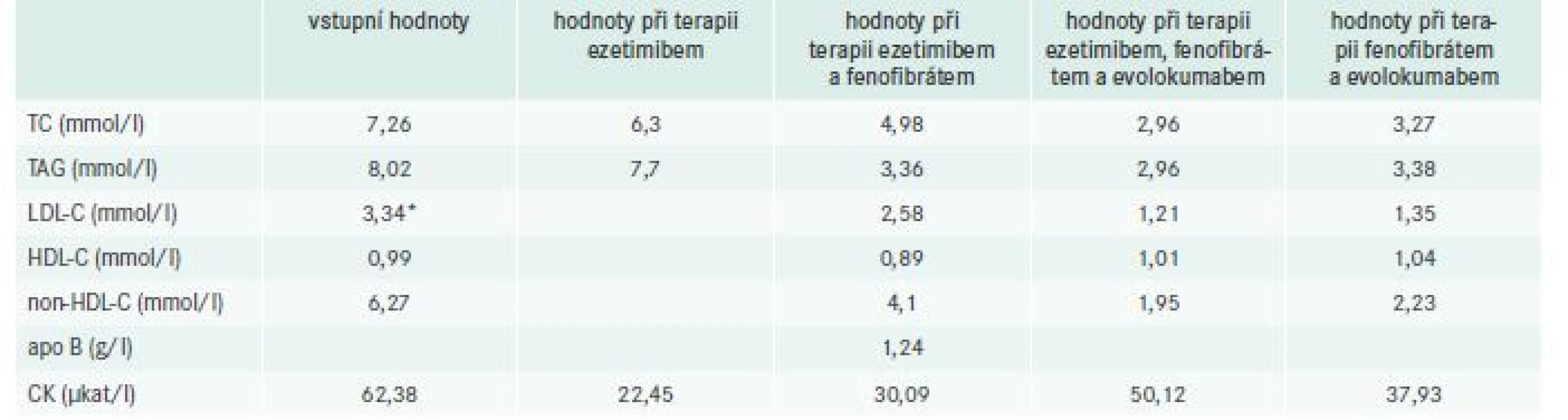
*přímé stanovení LDL-cholesterolu
apoB – apolipoprotein B CK – kreatinkináza HDL-C – HDL-cholesterol LDL-C – LDL-cholesterol TC – celkový cholesterol TAG – triacylglycerolDiskuse
Popisujeme případ mladého pacienta s myopatií a dyslipidemií, u kterého jsme řešili volbu terapie dyslipidemie v sekundární prevenci. Otázkou je, proč tak mladého pacienta (48 let) postihl infarkt myokardu. Vysvětlujeme si to tím, že došlo ke kumulaci rizikových faktorů – jednalo se o dlouholetého kuřáka se špatně kompenzovanou hypertenzí, obezitou a zvýšeným lipoproteinem Lp(a). Vypočítané SCORE bylo ještě před infarktem myokardu 5,7 % (měl tedy již vysoké KV-riziko) a v projekci na věk 60 let již 18 %.
Když se pacient dostavil do naší ambulance, byla v běhu diferenciální diagnostika přítomné myopatie. Tato je sama o sobě velmi široká a zahrnuje jak hereditární, tak získané myopatie. Při terapii statiny se nejčastěji setkáváme se získanou myopatií, a sice se svalovými symptomy asociovanými s užíváním statinů (Statin Associated Muscle Symptoms – SAMS). Nicméně získané myopatie se mohou vyskytnout také při některých endokrinopatiích a zánětlivých a systémových onemocněních. Mezi hereditární myopatie patří svalové dystrofie, myotonie a kanalopatie, kongenitální myopatie, metabolické myopatie a mitochondriální myopatie [4]. Kromě klinického vyšetření je při diagnostice myopatie důležité vyšetření svalových enzymů a myoglobinu, elektromyografie, svalové biopsie a u některých poruch významně přispívá molekulární genetika [4]. U našeho pacienta byla na Neurologické klinice FN Brno stanovena diagnóza hereditární svalové myopatie LGMD typu 2l s autosomálně recesivní dědičností. Jedná se o vzácnou pletencovou myopatii, která je způsobena mutací v genu tzv. dystrofin asociovaných glykoproteinů, konkrétně v genu pro anoctamin – ANO5 [5,6]. Začátek nemoci zpravidla nastává mezi 2. až 6. dekádou a typická je proximální pletencová svalová dystrofie a výrazná elevace CK (20násobná) [6]. Rychlost progrese je různá, od těžké formy s časnou ztrátou samostatnosti a respiračním selháním, až po lehké formy, které nezkracují život a umožňují dlouhodobě téměř normální lokomoci [5], což je zřejmě případ našeho pacienta.
Jak již bylo uvedeno, u pacientů s dyslipidemií, kteří mají zároveň myopatii a elevaci CK, nemáme jasné doporučení, která hypolipidemika bychom měli zvolit v první linii. Dle platných doporučení European Atherosclerotic Society z roku 2016 má být u pacientů s elevací CK > 4násobek horní hranice normy zvážena alternativní terapie a u pacientů netolerujících statiny terapie inhibitorem PCSK9 [2]. Vzhledem k tomu, že primárním cílem v sekundární prevenci KV-onemocnění je LDL-cholesterol, zvolili jsme nejprve terapii ezetimibem, jakožto inhibitorem vstřebávání cholesterolu, který má dle klinických studií potenciál snížit v monoterapii LDL-cholesterol o 15–22 % [2]. U našeho pacienta to bylo pouze o 13 %. Jako druhý byl do kombinace vzhledem k přetrvávající hypertriglyceridemii zvolen fenofibrát. Přestože byla role triacylglycerolů (TAG) jako rizikového faktoru KV-onemocnění opakovaně diskutována, data podporují roli na triglyceridy bohatých lipoproteinů jakožto rizikového faktoru KV-onemocnění [7]. Primárním cílem v prevenci KV-onemocnění zůstává LDL-cholesterol, jehož snížení má nepopiratelná data [2], přičemž data podporující benefity snížení TAG jsou získávána spíše ze studia subpopulací anebo post hoc analýz. KV-riziko je zvýšeno při hodnotě TAG > 1,7 mmol/l [7], avšak farmakoterapii ke snížení TAG bychom měli zvažovat u vysoce rizikových pacientů s TAG > 2,3 mmol/l, pokud toho nemůže být dosaženo změnou životního stylu [2]. Toto byl také případ našeho pacienta, u kterého bylo sice pomocí nefarmakologických opatření dosaženo jistého snížení TAG, avšak i poté přetrvávala hypertriglyceridemie indikovaná k terapii fibrátem.
Ani při kombinační terapii ezetimibem s fenofibrátem jsme nedosáhli cílové hladiny LDL-cholesterolu < 1,8 mmol/l, jak je doporučeno pro pacienty v sekundární prevenci. Zvažovali jsme proto terapii inhibitorem PCSK9, avšak pacient nesplňoval současně platná úhradová kritéria. Přestože měl v sekundární prevenci LDL-cholesterol > 3 mmol/l při maximální tolerované terapii hypolipidemiky, nemohli jsme prokázat statinovou intoleranci, protože byl k terapii statinem kontraindikován. Zažádali jsme proto zdravotní pojišťovnu a úhrada terapie inhibitorem PCSK9 byla pacientovi revizním lékařem schválena. Dle klinických studií s inhibitory PCSK9 evolokumabem a alirokumabem můžeme očekávat snížení LDL-cholesterolu v rozmezí 50–70 % nezávisle na předchozí hypolipidemické terapii [8,9]. U našeho pacienta došlo k poklesu LDL-cholesterolu o 40 % a v sekundární prevenci dosáhl cílových hodnot.
Zajímavou otázkou je, zda existuje nějaká spojitost mezi svalovou dystrofií a smíšenou dyslipidemií, které byly přítomny u našeho pacienta společně. Při zkoumání biopsií příčně pruhovaných svalů pacientů se svalovou dystrofií byla zjištěna výrazná elevace TAG ve svalové tkáni, a také změny ve složení membránových lipidů [10]. Dále bylo u těchto pacientů popsáno častější snížení ejekční frakce a abnormality na elektrokardiogramu (EKG) [11]. Avšak o tom, zda je u těchto pacientů přítomna také dyslipidemie detekovatelná v séru, jsme v literatuře zmínku nenašli. Pouze u myší byla popsána elevace non-HDL cholesterolu a endoteliální dysfunkce [12]. Přestože informací o možném propojení těchto dvou nozologických jednotek máme zatím málo, lze spekulovat, že smíšená dyslipidemie přítomná u našeho pacienta byla dána přítomností hereditární svalové dystrofie.
Podpořeno: MZ ČR – RVO (FNOL, 00098892).
MUDr. Ľubica Cibičková, Ph.D
Doručeno do redakce/Doručené do redakcie/Received 12. 12. 2018
Přijato po recenzi/Prijaté po recenzii/Accepted 14. 1. 2019
Sources
- Zlatohlávek L, Vrablík M, Češka R. Hypolipidemická terapie v rukou praktického lékaře. Med Praxi 2011; 8(7): 316–320.
- Catapano AL, Graham I, De Backer G et al. 2016 ESC/EAS Guidelines for the Management of Dyslipidaemias: The Task Force for the Management of Dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS) Developed with the special contribution of the European Assocciation for Cardiovascular Prevention & Rehabilitation (EACPR). Atherosclerosis 2016; 253 : 281–344. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosis.2016.08.018>.
- Janský P, Rosolová H, Vrablík M. 2016 ESC/EAS Guidelines for the management of Dyslipidaemias. Summary of the document prepared by the Czech Society of Cardiology. Cor et Vasa 2017; 59(4): 389–415.
- Ambler Z, Bednařík J. Myopatie – základní charakteristika, klasifikace a perspektivy. Neurol Praxi 2004; 5(3): 135–136.
- Bednařík J. Svalové dystrofie. Neurol Praxi 2004; 5(3): 137–141.
- Schneider I, Stoltenburg G, Deschauer M et al. Limb girdle muscular dystrophy type 2L presenting as necrotizing myopathy. Acta Myol 2014; 33(1): 19–21.
- Sarwar N, Sandhu MS, Ricketts SL et al. [Triglyceride Coronary Disease Genetics, Consortium and Emerging Risk Factors Collaboration]. Triglyceride-mediated pathways and coronary disease: collaborative analysis of 101 studies. Lancet 2010; 375(9726): 1634–1639. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(10)60545–4>.
- Robinson JG, Farnier M, Krempf M et al. Efficacy and safety of alirocumab in reducing lipids and cardiovascular events. N Engl J Med 2015; 372 : 1489–1499. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1501031>.
- Sabatine MS, Giugliano RP, Wiviott SD et al. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med 2015; 372 : 1500–1509. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1500858>.
- Srivastava NK, Yadav R, Mukherjee S et al. Abnormal lipid metabolism in skeletal muscle tissue of patients with muscular dystrophy: In vitro, high-resolution NMR spectroscopy based observation in early phase of the disease. Magn Reson Imaging 2017; 38 : 163–173. Dostupné z DOI: <http://dx.doi.org/10.1016/j.mri.2017.01.001>.
- Sveen ML, Thune JJ, Køber L et al. Cardiac involvement in patients with limb-girdle muscular dystrophy type 2 and Becker muscular dystrophy. Arch Neurol 2008;65(9):1196–201. Dostupné z DOI: <http://dx.doi.org/10.1001/archneur.65.9.1196>.
- Sellers SL, Milad N, White Z et al. Increased nonHDL cholesterol levels cause muscle wasting and ambulatory dysfunction in the mouse model of LGMD2B. J Lipid Res 2018; 59(2): 261–272. Dostupné z DOI: <http://dx.doi.org/10.1194/jlr.M079459>.
Labels
Angiology Diabetology Internal medicine Cardiology General practitioner for adults
Article was published inAthero Review

2019 Issue 1-
All articles in this issue
- Těžká smíšená dyslipidemie jako projev hematologického onemocnění: kazuistika
- Vliv alirokumabu na kardiovaskulární příhody: Co ukázala studie ODYSSEY OUTCOMES?
- Nutraceutika s hypolipidemickým účinkem v klinické praxi: shrnutí stanoviska Mezinárodního expertního panelu lipidologů vypracované výborem České společnosti pro aterosklerózu
- Iniciativa k ustavení aferetických center: indikace a provádění lipoproteinové aferézy v České republice
- Deficit lyzosomální kyselé lipázy v diferenciální diagnostice familiární hypercholesterolemie
- Terapie dyslipidemie u pacienta se svalovou dystrofií: kazuistika
- Psoriáza ako rizikový faktor kardiovaskulárnych príhod: kazuistika
- Intenzívny manažment dyslipidémie u veľmi vysokorizikových pacientov pomocou PCSK9-inhibítorov
- Athero Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nutraceutika s hypolipidemickým účinkem v klinické praxi: shrnutí stanoviska Mezinárodního expertního panelu lipidologů vypracované výborem České společnosti pro aterosklerózu
- Deficit lyzosomální kyselé lipázy v diferenciální diagnostice familiární hypercholesterolemie
- Terapie dyslipidemie u pacienta se svalovou dystrofií: kazuistika
- Psoriáza ako rizikový faktor kardiovaskulárnych príhod: kazuistika
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

