-
Medical journals
- Career
Tělesná teplota dítěte v průběhu anestezie
: V. Mixa; V. Kaplanová
: Klinika anesteziologie, resuscitace a intenzivní medicíny 2. LF UK a FN Motol, Praha
: Anest. intenziv. Med., 27, 2016, č. 5, s. 320-326
:
Perioperační hypotermie je závažnou komplikací anestezie a je spojena s mnoha nepříznivými důsledky, mezi něž patří oběhová nestabilita, útlum dýchání a prodloužení účinků anestetik. Největší opatrnosti si zaslouží novorozenci a malé děti, které mají větší sklon ke snížení tělesné teploty během operačního výkonu pro relativně velký tělesný povrch a tenkou vrstvu podkožního tuku. Hlavními mechanismy tepelných ztrát na operačním sále jsou odvedení a vyzařování tepla, proudění vzduchu a odpařování. Optimální tepelné homeostázy v průběhu anestezie dítěte lze dosáhnout kombinací řady postupů, např. použitím teplovzdušných matrací, voděodolného rouškování, ohřívání infuzních roztoků nebo zamezení proudění vzduchu kolem pacienta. Perioperační teplotu těla lze měřit kožním, jícnovým, rektálním či tympanálním teploměrem nebo přístrojem SpontOn pomocí vytvořeného izotermického kanálu do tělesného tepelného jádra. Spolehlivé měření tělesné teploty slouží též k prevenci arteficiálně navozené hypertermie.
Klíčová slova:
dětská anestezie – hypotermie – tepelná homeostáza – termoregulace – měření tělesné teplotyÚVOD
Udržování perioperační tepelné homeostázy a spolehlivé měření tělesné teploty operovaného dítěte patří vedle kontinuálního monitorování oxygenace, udržování přiměřené náplně cévního řečiště a dostatečné analgezie k základním podmínkám úspěšné anestezie malého dítěte. Podcenění péče o tepelnou pohodu dítěte v průběhu operace může vést k závažným komplikacím a může též významně ovlivnit pooperační průběh, zejména hojení rány. Ke správnému vedení tepelné homeostázy je třeba znát základy termoregulace dítěte, správně kombinovat jednotlivé prostředky určené k peroperačnímu udržování tělesné teploty a provádět spolehlivé měření tělesné teploty dítěte.
TERMOREGULACE
Tělesná teplota je dána výsledkem mezi příjmem, produkcí a výdejem tepla. Rovnováhu mezi těmito procesy zajišťuje termoregulace, tedy schopnost organismu trvale udržovat optimální tělesnou teplotu. Na teplotě těla závisí všechny metabolické a enzymatické pochody, ke kterým v lidském organismu dochází. Lidské tělo si lze představit jako kombinaci striktně teplokrevného (homoiotermního) tělesného jádra a periferních částí těla, které se chovají studenokrevně (poikilotermně). Tělesné jádro (označované též jako tepelné jádro) tvoří všechny orgány s vysokou látkovou přeměnou, tzn. vnitřní orgány krajiny hrudní, břišní, lebeční a proximálně nejhlouběji uložené části končetin. Jádro je hlavním producentem tepla a jeho teplota je v klidu velmi stálá. Periferní části těla, nazývané tepelná slupka, bývají různě rozsáhlé podle věku a tělesného typu. Slupku tvoří kůže, podkoží, tuková vrstva v podkoží a končetiny. Slupka má nestálou teplotu, která se mění vlivem okolí, je nižší oproti jádru a částečně přizpůsobuje svoji teplotu okolí, což v důsledku zabraňuje vysokým ztrátám tělesného tepla [1].
Průměrná tělesná teplota dítěte měřená v konečníku je 36,6–37,5 °C, u novorozence je přibližně o půl stupně vyšší. Běžně se pohybuje v rozmezí 35,5–40,0 °C. Teplo je v těle produkováno jako vedlejší efekt bazálních buněčných metabolických procesů a především zvýšeným metabolismem svalových buněk podmíněným námahou a chladovým třesem. Kolísání teploty ovlivní cirkadiánní rytmy (až o 1,5 stupně), fyzická zátěž, příjem potravy, psychický stav a závažně též teplota okolního prostředí – termoregulační mechanismy nahého dítěte se zapojují při poklesu teploty okolního prostředí pod 28 °C (!).
Centrálním orgánem, který reguluje tělesnou teplotu, je hypothalamus. Termoregulace je řízena ze dvou center: Aronsohn-Sachsova, uloženého v přední části hypothalamu, a Isenschmidt-Krohlova, které se nachází v zadní části hypothalamu. Informace přicházejí jednak z chladových a tepelných termoreceptorů v kůži, které reagují na teplotu okolního prostředí, a jednak z vnitřních termoreceptorů v hlubokých tkáních (svalech, míše, mozku i samotném termoregulačním centru) reagujících na teplotu krve. Termoregulační centrum je velmi citlivé a reaguje již na změny teploty krve řádově setiny stupňů Celsia. V hypothalamu jsou zakódovány informace o žádoucích hodnotách teploty tělesného jádra. Referenční teplota, „set-point“, na kterou je hypothalamické centrum naladěno, je 37,1 °C. Hypothalamus porovnává informace přicházející z receptorů ve vnitřním prostředí s hodnotou, na kterou je termostat nastaven. Pokud se tyto hodnoty neshodují s žádoucími hodnotami, vyšle korekční signály do tří výkonných systémů, což jsou: autonomní nervový systém (cévní reakce), endokrinní žlázy (metabolismus) a aktivace motivačních center v limbickém systému [2].
Termoregulace u novorozence
Novorozenci a malí kojenci ztrácejí více tepla než dospělí, mají méně izolačního podkožního tuku, relativně velký povrch těla vzhledem k tělesné hmotnosti, jemnou kůži a bohatou kapilární síť. Novorozenci, a zejména předčasně narození, se rodí s nedostatečně vyvinutou termoregulací. Jsou charakterizováni slabou svalovou činností, neschopností třesové termogeneze a nedostatečným krytím ztrát tepla z energetických zdrojů, které jsou pak nahrazeny netřesovou termogenezí. Novorozenec se ve chladném prostředí zahřívá metabolismem tzv. hnědé tukové tkáně, která tvoří až 5 % jeho celkové hmotnosti. Je lokalizována mezi lopatkami, v zátylku, podél velkých cév v hrudníku a břiše (obr. 1). Hnědá tuková tkáň je velmi prokrvená, buňky mají vysoký počet mitochondrií a cytochromů. Mitochondrie obsahuje ve své vnitřní membráně protein termogenin (UCP 1), který umožňuje průchod protonů z mezimembránového prostoru do matrix. Protony však neprocházejí přes ATP-syntázu, a není tedy syntetizováno ATP. Energie z tohoto přenosu je uvolněna ve formě tepla, které slouží k udržování stálé tělesné teploty novorozence. Zásoby hnědého tuku jsou menší u nedonošených dětí, protože buňky hnědého tuku se začínají diferencovat ve 26.–30. gestačním týdnu a vyvíjí se až do 5. týdne po narození. Netřesová termogeneze má velký význam od narození do 6 měsíců [3].
1. A. Umístění hnědé tukové tkáně na povrchu (vlevo) a v hloubce trupu novorozence B. Poměr mezi tvorbou tepla netřesovou a třesovou termogenezí v těle novorozence a kojence do jednoho roku života 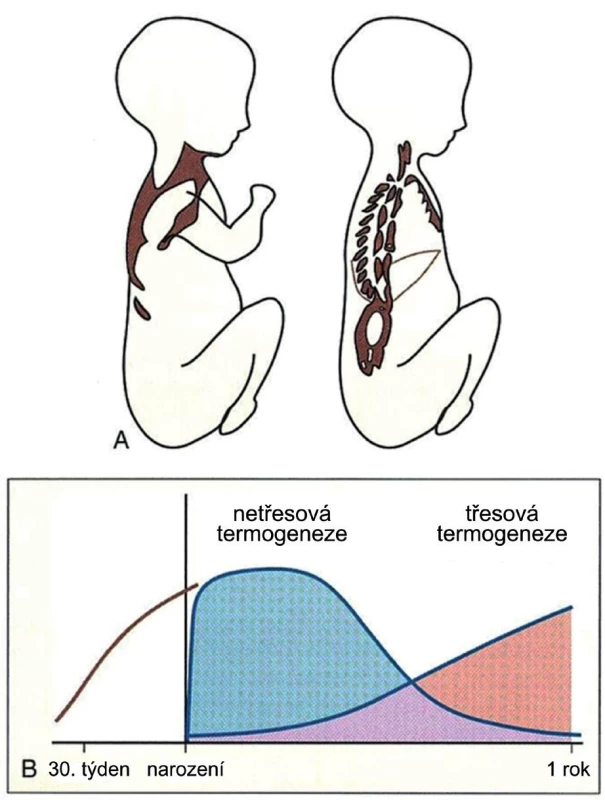
(Volně podle Luginbuehl I., Bissonnette B., Davis PJ Thermoregulation: Physiology and Periperative Disturbances. In Davis PJ, Cladis FP, Motoyama EK. Anesthesia for Infants and Children, 2011, Philadelphia, Elsevier Mosby) Ztráty tepla
Mechanismus tepelných ztrát dětského pacienta ležícího na operačním stole lze rozdělit na čtyři části (tab. 1) – kondukci, radiaci, konvekci a evaporaci (obr. 2).
1. Mechanismy tepelných ztrát malého dítěte v termoneutrálním prostředí 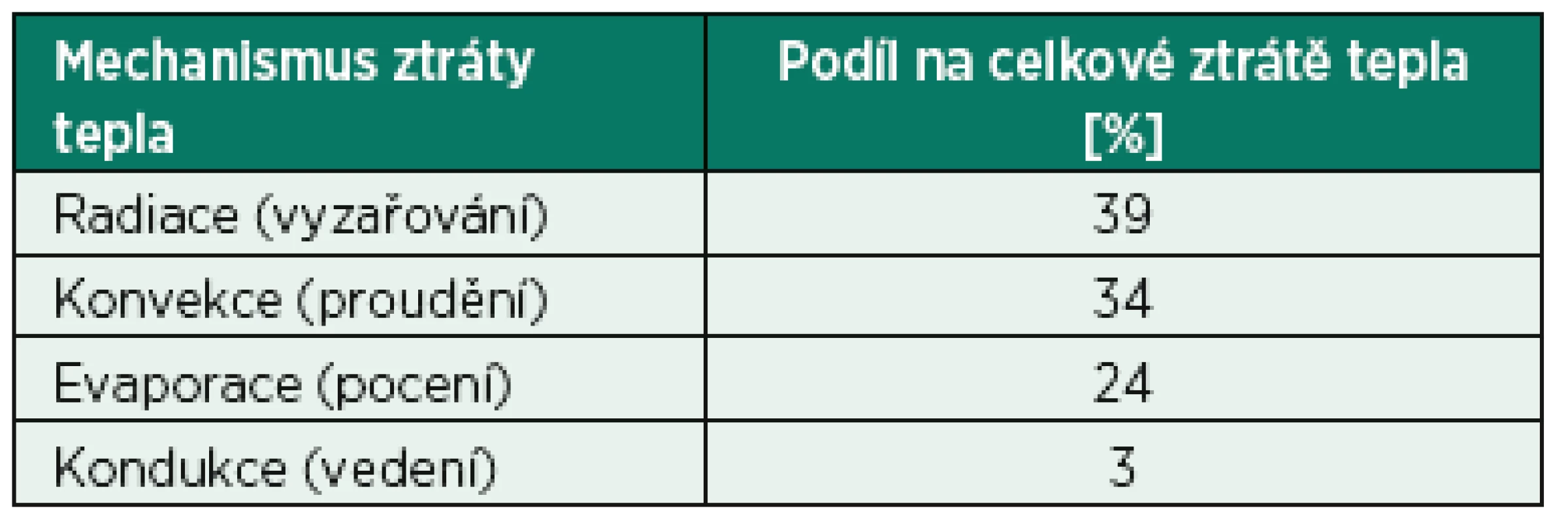
(Termoneutrální prostředí pro nedonošeného je 34 °C, pro donošeného novorozence 32,5 °C a pro čtrnáctidenního novorozence 30,0 °C). 2. Schéma čtyř způsobů ztráty tepla pacienta na operačním stole 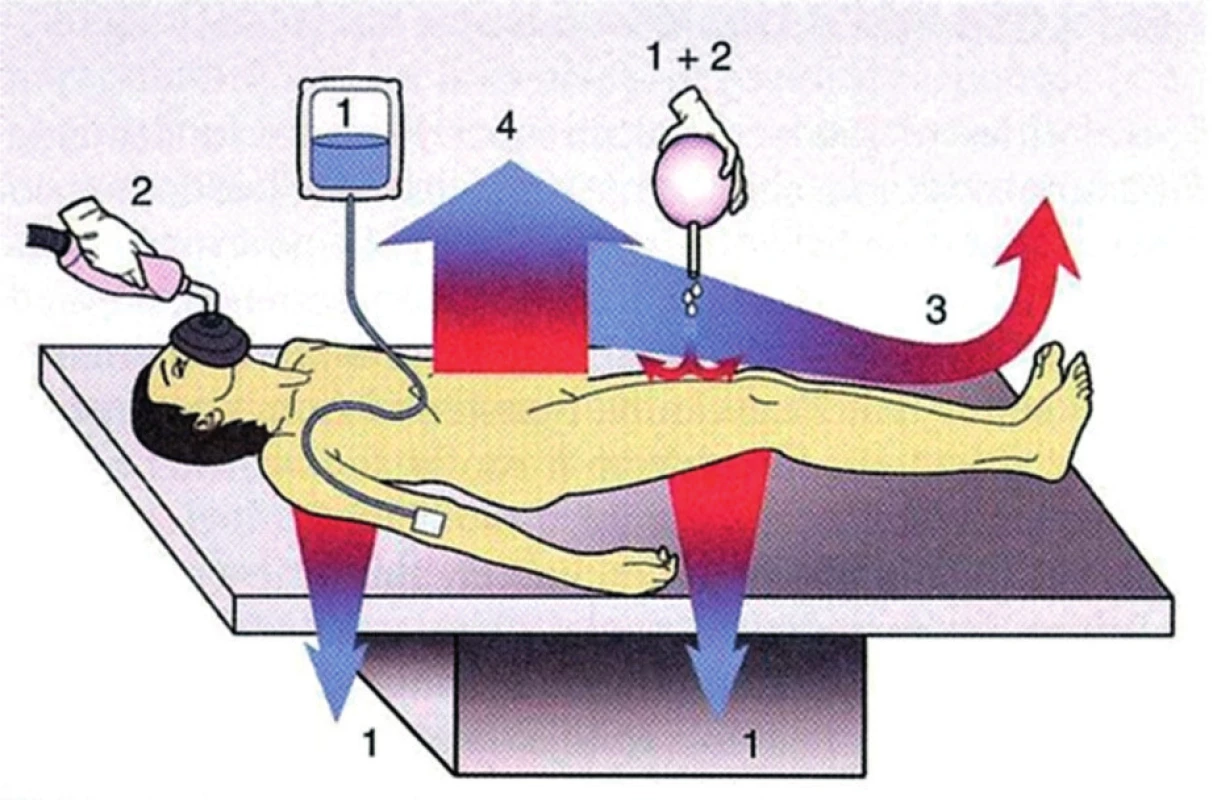
1 – kondukce, 2 – evaporace, 3 – konvekce, 4 – radiace. (Volně podle Luginbuehl I., Bissonnette B., Davis PJ Thermoregulation: Physiology and Periperative Disturbances. In Davis PJ, Cladis FP, Motoyama EK. Anesthesia for Infants and Children, 2011, Philadelphia, Elsevier Mosby) Kondukcí neboli vedením se rozumí předávání tepla mezi dvěma tělesy o nestejné teplotě přímým kontaktem. V případě operačního sálu se jedná například o ochlazování dítěte dotykem s chladnou deskou operačního stolu, infuzí chladného náhradního roztoku či vyplachováním operační rány studeným proplachem.
Radiace, vyzařování je nejvýznamnějším mechanismem tepelné ztráty. Lidský organismus, jako jakýkoliv jiný hmotný objekt, vyzařuje do svého okolí tepelné záření. Jeho intenzita je přímo ovlivňována poměrem tělesné hmotnosti a tělesného povrchu. Malé děti s velkým tělesným povrchem tudíž ztrácejí radiací více tepla než dospělí. Intenzita radiace závisí též přímo úměrně na rozdílu teploty těla a okolního prostředí.
Konvekce neboli ztráta tepla prouděním znamená předání tepla pohybujícím se molekulám okolního prostředí (v našem případě vzduchu), které je odvádí. V praxi se nejedná jen o proudění vzduchu kolem těla operovaného dítěte, ale také o tepelné ztráty způsobené výměnou dýchací směsi při ventilaci plic, zejména řízené. V běžném životě lze konvekci sledovat jako zchlazující účinek větru.
Při respiraci a evaporaci (pocení) dochází k vypařování vody. Vzhledem k velkému měrnému skupenskému teplu vypařování vody jsou to velmi významné mechanismy. Zevní vlivy ovlivňující pocení jsou především relativní vlhkost okolí, rychlost proudění vzduchu a minutová ventilace plicní. Ztráty tepla evaporací můžeme rozdělit do čtyř skupin: neznatelná evaporace, při níž se voda odpařuje pokožkou bez viditelného pocení, znatelné pocení za účasti potních žláz, energeticky velmi významné a na rozdíl od neznatelné evaporace organismem regulovatelné. Dalšími mechanismy ztráty vody a tepla evaporací jsou ztráty vody z plic při umělé plicní ventilaci a odpařování vody a tepla z otevřených tělních dutin a chirurgických ran.
HYPOTERMIE
Hypotermií je provázeno 60 % operačních výkonů v celkové anestezii. Závažné podchlazení je uváděno u 75 % výkonů s otevřením tělních dutin, zejména překračujících časový limit dvě hodiny. V perioperačním období je definována hypotermie jako pokles teploty tělesného jádra pod 36 °C (lehká 36,0–34,0 °C, střední 33,9–32,0 °C a závažná pod 32,0 °C). Jedná se o jednu z nejčastějších komplikací během chirurgického výkonu. Největší pokles tělesné teploty je 40–60 minut od začátku anestezie, neboť hypotermie se během anestezie vyvíjí charakteristickým schématem redistribuce tepla. V průběhu první hodiny se teplota jádra obvykle sníží o 1–1,5 °C v důsledku výrazného zchlazení krve cirkulující v periferních cévách dilatovaných po úvodu do anestezie. Poté následuje pomalejší, téměř lineární snížení vnitřní teploty přibližně k 35 °C po první hodině anestezie. Po nástupu termoregulační periferní vazokonstrikce a při dodržování zásad tepelné pohody teplota jádra dosáhne fáze plató na cca 35,5 °C, dále se již nesnižuje. Z uvedeného vyplývá, že je nutné měřit tělesnou teplotu už v průběhu anestezie trvající déle než 60 minut [4].
Rychlejší nástup hypotermie u pacienta v celkové anestezii je způsoben především následujícími skutečnostmi:
- poklesem metabolické aktivity organismu, a tudíž i produkcí metabolismem generovaného tepla. Úroveň metabolismu dosahuje přibližně 70 % normy;
- zvýšeným vlivem okolního prostředí na dítě na operačním stole;
- anestetiky způsobeným centrálním útlumem termoregulace;
- výše popsanou redistribucí tepla v těle;
- v případě neuroaxiální blokády vyřazením periferní vazokonstrikce, které redistribuci tepla znesnadní, a ztráty tepla se tak zvýší [5];
- únikem tepla z otevřených tělesných dutin, zejména z břišní dutiny velkou plochou střevních kliček.
Hypotermie má především vliv na metabolismus léků používaných v anestezii. Zpomalení metabolismu prodlužuje účinek mnoha léků, dávkování anestetik se stává obtížně řiditelným. Již při mírné hypotermii dochází ve srovnání s normotermickými pacienty k vyšším peroperačním krevním ztrátám. Hypotermie má totiž negativní vliv na funkci trombocytů. Je významně zvýšená pravděpodobnost rané infekce, ke které dochází snížením funkce polymorfonukleárních neutrofilních granulocytů. Pokles tělesné teploty jádra pod 36 °C vyvolá vazokonstrikci, která způsobí pokles dodávky kyslíku do tkání a narušuje se funkce fagocytujících leukocytů. Hypotermie zvyšuje riziko infekce v místě chirurgického výkonu, zejména u střevních a kolorektálních operací. Vazokonstrikce a hypoperfuze střevní stěny zvýší permeabilitu sliznice a únik toxinů může vést až k sepsi. Při hypotermii dochází ke snižování srdečního výdeje a zvyšuje se centrální venózní tlak a periferní vaskulární rezistence. Potencuje se tak dráždivost komor, snižuje se dodávka kyslíku tkáním a působí depresivně na dýchací cesty. U hypotermních pacientů dochází při opětovném ohřívání organismu k významnému vzestupu spotřeby kyslíku. U pacientů s oběhovým selháváním nebo vrozenou vývojovou srdeční vadou může dojít až ke vzniku srdečního selhání [6].
Prevence hypotermie
Úspěšného udržení tepelné homeostázy dětského pacienta v anestezii lze nejsnáze dosáhnout kombinací následujících postupů [7]:
- optimální teplota na operačním sále (v praxi ovšem nepřijatelná) je pro péči o novorozence stanovena na 27–29 °C podle zralosti dítěte (pro dospělého je nejnižší možná přijatelná teplota vzduchu na operačním sále 21 °C). Tak lze zamezit ztrátám tepla radiací. Ztráty tepla konvekcí a do značné míry i evaporací z tělních dutin lze snížit správným nasměrováním proudu vzduchu z klimatizačního zařízení;
- tepelné zářiče lze použít při přípravě dítěte k operaci před zarouškováním. Způsobují velké ztráty vody a při nedodržení bezpečné vzdálenosti mohou být příčinou popálenin;
- reflexní přikrývky a plastové fólie jsou používány vzhledem k malým rozměrům pacienta spíše výjimečně. Účelné se jeví spíše balit končetiny a především hlavičku do vaty či měkké textilie. Zásadní je rouškováním operačního pole voděodolnými rouškami, které udržují tělo dítěte v suchu a zabraňují ztrátám tepla odpařováním vody;
- nejčastěji používané jsou různé typy podušek či přikrývek předávajích teplo konvekcí nebo kondukcí. Jejich princip, konstrukce i účinnost jsou velmi rozmanité. V současné době jsou nejpoužívanější generátory proudu teplého vzduchu (Bair Hugger, Warm air, Warm touch apod.), nejúčelnější je rozvádět teplý vzduch kolem dítěte podložkou s drobnými perforacemi, které teplo rozvádějí rovnoměrně kolem dítěte. Větší pacienti (asi od deseti let věku) položení na takovou matraci ji příliš zatíží a omezí proudění vzduchu kolem celého těla. Větší děti se proto doporučuje matrací přikrývat na místech, která jsou mimo operační pole. Použití proudu teplého vzduchu bez připojené matrace hrozí hyperemií až popálením. Další možností, jak vyhřívat tělo pacienta a prostor pod rouškami, jsou vodní nebo elektrické matrace. Jejich nevýhodou je v případě malého dítěte velmi malá plocha doteku těla s matrací. Na všech výše popsaných prostředcích bývá obvykle termostatem nastavená teplota vyhřívání 36–42 °C. Moderní generace těchto přístrojů je krom termostatu opatřena ještě teploměrem a zařízením, které zpětnou vazbou reguluje teplotu vyhřívání a zamezí přehřátí pacienta [8];
- zahřívání infuzních roztoků podávaných malému dítěti během anestezie je často citovaný postup. Při podání udržovací infuze o teplotě okolního prostředí v dávce 10 ml/kg/h ztráta tepla není významná. Zásadní důležitosti nabývá až při podávání několikanásobného množství. Určit přesně míru ztráty tepla je, vzhledem k proměnné teplotě roztoku, jeho množství a hmotnosti dítěte, velmi obtížné. Znám je pouze údaj, že podání jednoho litru ledového fyziologického roztoku dospělému člověku sníží tělesnou teplotu o 1,7 °C [9]. Způsoby ohřívání infuzního roztoku jsou různé, od infuzního setu ponořeného do lahve s teplou vodou až po vysoce sofistikované elektronické průtokové ohřívače. Ideální teplota infuzního roztoku by se měla pohybovat okolo 37 °C. Při příliš dlouhé spojovací hadičce mezi ohřívačem a žilním vstupem může dojít k významné ztrátě tepla;
- ve srovnání s dospělým relativně vyšší minutový dechový objem významně zvyšuje ztráty tepla dýcháním. Endotracheální intubací je omezeno předehřívání a zvlhčování vdechovaného vzduchu v ústní dutině a ten potom významně ochlazuje dolní dýchací cesty a plicní parenchym.
Vzhledem k tomu, že v našich podmínkách obvykle nejsou v anesteziologickém okruhu vřazeny aktivní zvlhčovače dýchací směsi, je nutno spoléhat jen na porézní kondenzátory vlhkosti (umělé nosy) a částečné ohřívání směsi ve směšovací hlavě anesteziologického přístroje. Potřeba zvlhčení a nebezpečí zchlazení dítěte studenou dýchací směsí je obzvlášť naléhavá při používání jednocestného systému [10].
ZPŮSOBY MĚŘENÍ TĚLESNÉ TEPLOTY BĚHEM OPERAČNÍHO VÝKONU
V průběhu anestezie jsou tradiční lékařské teploměry nahrazeny teplotními čidly napojenými na monitory vitálních funkcí. Tato čidla, respektive způsob jejich použití, lze do jisté míry rozdělit na neinvazivní a invazivní. Za neinvazivní považujeme různá kožní čidla přikládaná do podpaží nebo na čelo a tympanální infračervené teploměry. Z invazivních způsobů jsou nejčastěji používána termistorová čidla zavedená do jícnu nebo do rekta [11]. Jícnové čidlo snímá teplotu v oblasti dolního jícnu, naměřená teplota nejvíce odpovídá teplotě krve v aortě (teplota tělesného jádra), avšak při thorakotomii malých dětí se může snadno přiblížit teplotě okolního prostředí. Použití jícnového teploměru je nevhodné u pa-cientů při vědomí, spontánně ventilujících a u nemocných se zachovaným kašlacím reflexem. Podobných výsledků lze dosáhnout čidlem, které je součástí Swanova-Ganzova katétru. Výsledky měření získané rektálním čidlem nebo čidlem, které je připojeno na močový katétr, mohou být ovlivněny velkým podchlazením nebo centralizací oběhu dítěte [12].
Zcela novou kvalitu v měření tělesné teploty pacienta nejen v anestezii či v podmínkách intenzivní péče představuje systém SpotOn firmy 3M. Jedná se o neinvazivní, kontinuální přesný způsob měření teploty tělesného jádra. Monitorovací systém SpotOn používá jednorázový samolepící senzor, který se umístí na čelo pacienta. Princip měření spočívá ve vytvoření „tunelu“ izotermického s okolní tkání, který směřuje od tohoto senzoru do nitra mozkové tkáně, tedy do tepelného jádra. Změny teploty mozkové tkáně a tedy i změny teploty izotermického tunelu jsou snímány a průběžně zobrazovány na kontrolní a ovládací jednotce. Paměťový čip umístěný v senzoru umožňuje po dobu dvou hodin nepřetržité vizuální znázornění teplotní křivky pacienta na ovládací jednotce SpotOn. Tento princip měření tělesné teploty dítěte poskytuje dosud nejpřesnější údaje o teplotě tělesného jádra zcela nezávislé na rušivých vlivech působících na teplotní čidla jiného typu [13].
Správně provedené měření tělesné teploty dítěte v anestezii nás informuje nejen o změnách teploty, ale při porovnání rozdílu kožní teploty a teploty jádra může pomoci při odhalení hypovolémie a centralizace. O tom uvažujeme, jestliže rozdíl teplot překročí více než 1 °C.
Větší děti, zejména v kojeneckém věku, mohou mít velmi dobře vyvinutou vrstvu podkožního tuku. Při příliš intenzivním zahřívání se v průběhu anestezie přehřejí a jejich tělesná teplota stoupá i po ukončení zahřívání. Produkují teplo a po zarouškování nemohou vychládat. Tachykardie z přehřátí může vést k mylné představě o nedostatečné analgezii a stoupající teplota může připomínat maligní hypertermii.
ZÁVĚR
Udržování tělesné pohody během anestezie je základním předpokladem úspěchu operace pacientů všech věkových kategorií, pro novorozence a malé kojence to platí dvojnásob. Tepelné homeostázy dětského pacienta lze dosáhnou kombinací řady aktivních opatření a kontinuální monitorací teploty moderními prostředky.
Poděkování
Autoři děkují firmě 3M Česko, spol. s r. o., za finanční podporu vydání článku.
Do redakce došlo dne 21. 6. 2016.
Do tisku přijato dne 20. 7. 2016.
Adresa pro korespondenci:
doc. MUDr. Vladimír Mixa, Ph.D.
KARIM 2. LF UK a FN Motol
V Úvalu 84
150 06 Praha 5-Motol
e-mail: vmxa@volny.cz
Sources
1. Sessler, D. I. Perioperative thermoregulation and heat balance. Lancet, 2016, Epub. ahead of print.
2. Hannenberg, A. A., Sessler, D. I. Improving Perioperative Temperature Management. Anesth. Analg., 2008, 107, 5, p. 1454–1457.
3. Duryea, E. L., Nelson, D. B., Wyckoff, M. H., Grant, E. N., Tao, W. et al. The impact of ambient operating room on neonatal and maternal hypothermia and associated morbidities: a randomized controlled trial. Am. J. Obstet. Gynecol., 2016, 214, 4, p. 505.e1-7.
4. Obare Pyszková, L., Nevtípilová, M., Žáčková, D., Fritscherová, Š., Zapletalová, J., Hrabálek, L., Adamus, M. Výskyt hypotermie v perioperačním období – unicentrická observační studie. Anest. Intenziv. Med., 2014, 25, 4, p. 267–273.
5. Shorrab, A. A., El-Sawy, M. E., Othman, M. M., Hammouda, G. E. Prevention of hypothermia in children under combinad epidural and general anesthesia: a comparison between upper - and lower - body warming. Paediatr. Anaesth., 2007, 17, 1, p. 38–43.
6. Kim, P., Taghon, T., Fetzer, M., Tobias, J. D. Perioperative hypothermia in the pediatric population: a quality improvement project. Am. J. Med. Qual., 2013, 28, 5, p. 100–106.
7. Witt, L., Dennhardt, N., Eich, C., Mader, T., Fischer, T., Bräuer, A., Sümpelmann, R. Prevention of intraoperative hypothermia in neonates and infants: results of a prospective multicenter observational study with a new forced-air warming system with increased warm air flow. Paediatr. Anaesth., 2013, 23, 6, p. 469–474.
8. Torossian, A. Thermal management during anaesthesia and thermoregulation standards for the prevention of inadvertent perioperative hypothermia. Clinical Anestesilogy, 2008, 22, 4, p. 659–668.
9. Shen, J., Wang, Q., Zhang, Y., Wang, X., Shi, P. Combination of warming blanket and prewarmed intravenous infuzion is effective for rewarming in infants with postoperative hypothermia in China. Paediatr. Anaesth., 2015, 25, 11, p. 1139–1143.
10. Torossian, A., Bräuer, A., Höcker, J., Bein, B., Wulf, H., Horn, E. P. Preventing inadvertent perioperative hypothermia. Dtsch. Arztebl. Int., 2015, 112, 10, p. 166–172.
11. Sahin, S. H., Duran, R., Sut, N., Colak, A., Acunac, B., Aksu, B. Comparison of temporal artery, nasopharyngeal, and axillary temperature measurement during anesthesia in children. J. Clin. Anesth., 2012, 24, 8, p. 647–651.
12. Drake-Brockman, T. F., Hegarty, M., Chambers, N. A., von Ungern-Sternberg, B. S. Monitoring temperature in children undergoing aneasthesia: a comparison of methods. Anaesth. Intensive Care, 2014, 42, 3, p. 315–320.
13. Iden, T., Horn, E. P., Bein, B., Böhm, R., Beese, J., Höcker, J. Intraoperative temperature monitoring with zero heat flux technology (3M SpotOn sensor) in comparison with sublingual and nasopharyngeal temperature: An observational study. Eur. J. Anaesthesiol., 2015, 32, 10, p. 747.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care Medicine
Article was published inAnaesthesiology and Intensive Care Medicine

2016 Issue 5-
All articles in this issue
- The 2016 definition of sepsis (Sepsis-3)
- Echocardiography in the acute coronary syndrome
- CPR-related injuries in out-of-hospital cardiac arrest patients
- Body temperature in the anaesthetised child
- Hypotension following induction to general anaesthesia: prevalence, significance, risk factors and preventive management options
- Aprotinin in cardiac surgery – re-evaluation of the risks?
- Selected aspects of anaesthesia for non-obstetric surgical procedures in the pregnant patient
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hypotension following induction to general anaesthesia: prevalence, significance, risk factors and preventive management options
- The 2016 definition of sepsis (Sepsis-3)
- Selected aspects of anaesthesia for non-obstetric surgical procedures in the pregnant patient
- Body temperature in the anaesthetised child
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

