-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Software LISA – virtuální resekce jater pro urychlení a usnadnění předoperačního plánování
Autoři: M. Svobodová 1,2; M. Jiřík 2,3; P. Včelák 3; V. Lukeš 3; T. Ryba 3; P. Hošek 2; K. Bajcurová 4; J. Ludvík 4; H. Mírka 2; Z. Tonar 1,2; V. Třeška 1; V. Liška 1,2
Působiště autorů: Chirurgická klinika, Lékařská fakulta v Plzni, Univerzita Karlova v Praze a Fakultní nemocnice Plzeň přednosta: prof. MUDr. V. Třeška, Dr. Sc. 1; Biomedicínské centrum, Lékařská fakulta v Plzni, Univerzita Karlova v Praze přednosta: doc. M. Štengl, Ph. D. 2; Nové technologie pro informační společnost, Fakulta aplikovaných věd, Západočeská univerzita v Plzni děkan: doc. RNDr. M. Lávička, Ph. D. 3; Klinika zobrazovacích metod, Lékařská fakulta v Plzni, Univerzita Karlova v Praze a Fakultní nemocnice Plzeň přednosta: prof. MUDr. B. Kreuzberg, CSc. 4
Vyšlo v časopise: Rozhl. Chir., 2015, roč. 94, č. 11, s. 485-490.
Kategorie: Zpráva
Chirurgie jater zaznamenává v posledních desetiletích velké pokroky, které mimo jiné odrážejí úspěchy technického vývoje a výzkumu aplikovaných v bioinženýrství, biomedicíně, lékařství. Interdisciplinární výzkum může také významně přispět k indikování většího počtu pacientů s maligními procesy v játrech k resekčnímu či ablačnímu zákroku. To je také dlouhodobý cíl spolupráce mezi Lékařskou fakultou v Plzni Univerzity Karlovy v Praze a Fakultní nemocnicí Plzeň se Západočeskou univerzitou v Plzni. Záměrem tohoto příspěvku je shrnutí nezbytných realizovaných a plánovaných kroků vedoucích k vývoji softwaru LISA (LIver Surgery Analyser). Klinicky testovaný software LISA nabídne v předoperační fázi radiologům a chirurgům tzv. virtuální resekci jater pro usnadnění rozhodnutí o možném typu a provedení kurativní léčby.
Chirurgická resekce a dále pak ablační metody jsou možnosti efektivní kurativní léčby u pacientů s nádorovým onemocněním jater. Limitujícím faktorem použití chirurgického zákroku je snížená regenerace jaterního parenchymu po resekci v důsledku cirhotického či fibrotického onemocnění nebo výskyt lézí v obou jaterních lalocích. U hraničních resekčních výkonů může být ablační léčba lézí vhodným doplněním. V případě primárně neresekovatelných nálezů může být ablace možnou metodou nahrazující chirurgický zákrok. Při plánování resekce nebo ablace je nezbytné stanovit případný zbytkový parenchym po resekci a rozhodnout o přesném vztahu nádorového ložiska k hlavním cévám a žlučovodům. Tyto parametry jsou důležité při volbě radikální léčby, pro navržení vhodné resekční linie s dodržením negativního chirurgického okraje a pro predikci regenerace jater po chirurgickém zákroku.
V předoperační fázi jaterní chirurgie se k diagnóze postižení jater pacienta používají radiologické metody. Nejčastěji se přistupuje k vyhodnocení dat z počítačové tomografie (CT) a magnetické rezonance (MRI). Výsledkem zpracování obrazových dat je rozhodnutí o výskytu lézí (velikost, poloha v jaterním parenchymu) a stanovení volumetrie jater. Současné vědecké informační technologické, kybernetické, mechanické a matematické metody mohou navíc přispět ke zdokonalení stávajících radiologických praktik a ke zkvalitnění diagnostického procesu.
Virtuální resekce jater se stala jedním z progresivních objektů vědecko-výzkumného zájmu napříč nejen Evropou. Jmenujme alespoň dvě hlavní evropská konsorcia. Virtual Liver Network (VLN), které sdružuje na sedmdesát vědeckých a klinických institucí v Německu, a dále pak IRCAD (Francie, výzkumné a vzdělávací laparoskopické centrum) ve spolupráci s INRIA (Francie, výzkumné a výpočetní centrum). Dílčím výsledkem jejich víceoborové spolupráce s dalšími vědecko-výzkumnými pracovišti jak v EU (Švýcarsko, Rakousko, Norsko atd.), tak ve světě (Japonsko, Kanada atd.) jsou volně dostupné softwary nabízející třírozměrnou (3D) rekonstrukci DICOM dat v reálném čase pro zlepšení orientace v pořízených CT a MRI datech během předoperační fáze, tj. software VR RENDER a MITK [1]. Tyto softwary dnes nabízejí uživateli poutavé grafické rozhraní a segmentaci jater nejen z DICOM dat založenou na vizualizaci velkých cév do úrovně, do které jsou CT a MRI schopné rozlišit větvící se cévní strom v jaterním parenchymu. Výpočetní centrum MEVIS, část VLN, se navíc úspěšně pokouší realizovat intraoperační navigační systém. Tento systém umožňuje využít informace z předoperačně pořízených CT a MRI dat ať už při resekci [2], tak při ablaci [3].
Během několika let interdisciplinárního výzkumu se díky 3D segmentaci a následné rekonstrukci jater a příslušného cévního řečiště ukázalo, že segmentace jater podle tzv. Coinaudových segmentů [4] není dostatečná v předoperačním plánování resekčního zákroku [8,9]. Naším cílem je podílet se na výzkumu, který povede k nalezení optimální resekční linie respektující rozdíly v segmentaci jater u každého pacienta podle anatomie cévního zásobení jater. Náš výzkum se opírá o informace nejen z makro, ale i z mikroúrovně cévního zásobení jater. Přestože se objevuje celá řada volně dostupných nebo komerčních softwarů, které nabízejí segmentaci CT a MRI dat, došli jsme k závěru, že v případě našeho mezioborového výzkumu se pokusíme o realizaci vlastního segmentačního modulu. Výhodou našeho rozhodnutí je možné využití softwaru jak pro klinické, tak experimentální účely.
Pro vlastní vědecký výzkum je nezbytné zpracování medicínských obrazových dat a jejich anonymizace. V Plzeňském kraji se během několika posledních let vyvinula fungující mezioborová spolupráce mezi Lékařskou fakultou v Plzni (LF) Univerzity Karlovy v Praze, Západočeskou univerzitou v Plzni (ZČU) a Fakultní nemocnicí Plzeň (FN). K tomu, aby mohla být CT a MRI data pacientů Fakultní nemocnice Plzeň zpracovávána pro vědecké účely, je nutné zajistit jejich bezpečný transfer na úložiště Fakulty aplikovaných věd, ZČU. Data jsou automaticky anonymizována před transferem ze zdravotnického zařízení a následně, po přenesení do výzkumného centra, jsou indexována pro další použití. V příspěvku [7] je publikovaný postup použitím autorizovaného softwaru AnonMed. Metoda rozpoznání DICOM snímků, možný výstup CT a MRI, s osobními údaji je zatím rozpracována a nebyla dosud publikována.
Největší pozornost v současném klinickém využití vyvíjených submodulů softwaru LISA byla věnována segmentaci jater z DICOM dat z CT abdominální oblasti pacientů. Na souboru 30 plně anonymizovaných DICOM dat byla testována metoda Graph-cut [8] nabízející jako jedna z mnoha segmentačních metod tzv. interaktivní segmentaci. Interaktivní segmentace, definovaná v [9], byla vyžádána experty z Kliniky zobrazovacích metod FN. Interaktivní segmentace na rozdíl od automatické segmentace se při segmentaci jater zdá výhodnější, neboť umožňuje lepší kontrolu výsledku algoritmu prostřednictvím zásahů uživatele. K tomuto faktu se přiklánějí mimo jiné i výsledky soutěže SLIVER07 [10], kde přední místa zaujímají softwary nabízející právě interaktivní segmentaci. Použití automatické segmentace při segmentaci jater z abdominální oblasti je omezené variabilitou anatomie jater mezi pacienty, mírou šumu v obrazových datech a malým rozdílem denzit mezi játry a okolními orgány (srdce, slinivka břišní, ledviny atd.). Hodnocením úspěšnosti segmentace jater z CT dat submodulem softwaru LISA se budeme dále podrobněji zabývat. Ke zpracování dat z MRI jsme zatím nepřistoupili, protože jsme v prvním klinickém testování pro validaci segmentačního submodulu měli k dispozici více dat z CT.
Zatímco pro segmentaci jater z CT dat se dle klinické praxe doporučuje venózní fáze, pro identifikaci a klasifikaci lézí je nezbytné využít jak venózní, tak arteriální fázi. Tato část softwaru LISA je zatím na úrovni vědeckého zpracování a její testování na klinických datech se připravuje. Cílem je, aby detekce lézí v jaterním parenchymu, která následuje po segmentaci jater z CT dat, byla plně automatická s případným použitím interaktivních nástrojů pro nezbytné manuální doladění výsledků. Identifikace lézí v parenchymu vychází z analýzy histogramu sestrojeného z denzit voxelů pořízeného obrazu. Analýza histogramu denzit je v podstatě úloha hledání lokálních maxim, kdy každé významné maximum je považováno za jednu ze tříd (parenchym, léze). Největší maximum je považováno za zdravou tkáň – tzv. funkční jaterní parenchym. Předpokládá se, že většina jaterního parenchymu je zdravá. Automatickou segmentací a následnou klasifikací (arteriální fáze se používá pro detekci hyperdenzních ložisek, venózní fáze se používá pro detekci hypodenzních ložisek) není možné zatím rozhodnout nad rámec zkušeného radiologického experta. Lze bezpečně rozhodnout pouze o rozdělení lézí na hypodenzní, hyperdenzní a kombinované (tzv. terčíkovité – hypodenzní centrum v hyperdenzní periferii). Současný submodul identifikace a klasifikace lézí je nastaven tak, aby falešná pozitivita převyšovala nad falešnou negativitou. Tj. pro klinickou praxi je přínosnější automaticky najít více falešných objektů než jeden skutečný ztratit.
Hlavním důvodem vývoje softwaru LISA je předoperační návrh optimálního vedení resekce s uvažováním pozitivního okraje. Stávající submoduly nabízejí resekční linii počítanou z rekonstrukce cévního stromu získaného pouze z CT dat pacienta. Tato část čeká na klinické ověření a testování. V současné době také probíhá testování zmiňovaných programových balíků VR RENDER a MITK [1]. Tyto programové balíky plánujeme využít pro návrh grafického rozhraní softwaru LISA, pokud se prokáže, že jejich intuitivní grafické rozhraní je vhodné v podmínkách naší klinické praxe. Zmiňované submoduly softwaru LISA jsou tedy ve fázi klinického testování a plánovitě je bude možné využívat pro urychlení a usnadnění stávající předoperační fáze.
Větve cévního stromu viditelné v CT datech pacienta jsou dobře rekonstruovatelné maximálně do druhého až třetího větvení portální žíly a druhého větvení jaterní žíly. Otázkou zůstává, zda počítačový model uvažující i nižší řády větvení cévního řečiště až do úrovně jaterních lalůčků může nabídnout lepší výsledek a bude možné stanovit přesnější segmentaci jater podle jejich perfuze. Naším dlouhodobým cílem je optimalizovat virtuální vedení resekční linie podle skutečné segmentace jater konkrétního pacienta a tím zvýšit počet pacientů doporučených k resekčnímu zákroku, nebo předejít zbytečným výkonům.
Za předpokladu realizace zobrazení a kvantitativního popisu cévního stromu jater od makro - k mikroúrovni [11] a jeho 3D rekonstrukci [12], které jsou také podstatným zájmem mezioborové spolupráce mezi LF UK v Plzni, ZČU a FN, je možné následně uvažovat o modelování resekční linie s ohledem na mikrostrukturu jaterního parenchymu. Jaterní parenchym protkaný složitou spletí cévního řečiště lze matematickou abstrakcí popsat jako kontinuální porézní perfuzní model. Tento model je zatím dobře shrnutý v aplikaci na srdeční tkáň [16,17]. V případě našeho pracoviště jsme schopni mikrostrukturu jaterního parenchymu popsat u prasat [15]. Přenositelnost získané informace z prasečích na lidská játra je možné diskutovat se zahraničními pracovišti, např. BioMMeda.
Zvolený matematický model zahrnující perfuzi na mikroúrovni jaterního řečiště vychází z roztřídění cévního stromu na několik tzv. kompartmentů neboli tříd podle průsvitu cévy a také podle příslušnosti k portální, jaterní žíle či jaterní tepně. U korozivního preparátu jater prasat pro kontrastní odlišení řečiště s využitím CT a mikro-CT je možné navázat na práci [16]. Zde formulovaná metodika nástřiku lidských jater nebyla u prasečích jater zatím publikována a naším zájmem je ověřit ji, potvrdit, nebo vyvrátit. V případě kladného potvrzení bude možné provést experimenty, jejichž výstupem bude soubor obrazových dat z CT a mikro-CT vhodných pro další počítačové zpracování. Za tímto účelem již dochází k vývoji tzv. „histologického analyzátoru“ vedlejšího submodulu softwaru LISA, který není určen pro přímé klinické využití, ale pro využití v experimentální chirurgii.
Vedlejším modulem softwaru LISA je tzv. histologický analyzátor, který je vyvíjen k urychlení a usnadnění 3D zpracování mikro-CT dat korozivních preparátů. Při vývoji tohoto submodulu se přihlíží ke kvantitativnímu popisu mikrostruktury korozivních preparátů prasat uvedenému v [11]. Na rozdíl od uvedené práce, kde autoři přistoupili k manuálnímu vyhodnocení vzorků, histologický analyzátor nabízí automatické vyhodnocení a tím podstatně zkracuje čas zpracování z několika let na minuty. Nabízí vyhodnocení délkové a objemové hustoty cév, objemový podíl cév, povrchovou hustotu cév, měření křivosti (tortuozity) úseků cév mezi bifurkacemi a stanovení výskytu počtu bifurkací ve vzorku. Histologický analyzátor je důležitým mezikrokem od pracného pořízení korozivního preparátu jater k matematickému a počítačovému modelování perfuze jater s uvažováním mikrostruktury cévního řečiště. Segmentace cév z mikro-CT dat vzorku korozivního preparátu je provedena metodou narůstání oblastí patřící do skupiny metod označených „region growing“. Dále probíhá skeletonizace cév (pro zjednodušení modelu) – reprezentace cév jejich střednicí, která převede 3D model na zjednodušený jednodimenzionální (1D) model. Stejně jako v případě ostatních submodulů softwaru LISA i zde probíhají morfologické operace pro odstranění šumu pořízeného obrazového signálu – vyhlazení. V současnosti je výstup „histologického analyzátoru“ porovnáván s výstupem uvedeným v [11]. Dalším plánovaným krokem je využití stereologického přístupu k možnému morfologickému určení 3D propustnosti, tj. poréznosti jaterního parenchymu. Tento přístup je jedním z dalších vhodných postupů vedle mechanického modelu diskutovaného pro parenchym lidských jater v [17]. Diskuze výhod mechanického a morfologického modelu pro matematické a počítačové modelování poréznosti biologických tkání je shrnuta v [18].
Během klinického testování segmentačního submodulu softwaru LISA [19] bylo navrženo zjednodušené interaktivní uživatelské prostředí podle testovacích potřeb expertů Kliniky zobrazovacích metod a Chirurgické kliniky FN Plzeň. Komplikované oblasti při segmentaci (srdeční tkáň atd.) naléhající u některých testovacích dat na jaterní parenchym byly manuálně odstraněny za použití konvexních ploch. V současnosti se hledají jiné možnosti odstranění nežádoucích oblastí v obrazových datech založené na automatickém odstranění všech orgánů v hrudním koši, tzv. změně intenzity obrazového signálu příslušných voxelů. Tato úloha spočívá v segmentaci bránice, která odděluje abdominální a hrudní oblast až na některé výjimky, které by se musely vždy řešit manuálním odstraněním.
Segmentační submodul byl úspěšně validován podle soutěžních kritérii SLIVER07 [10]. Jediným rozdílem oproti referenčním datům ze soutěže bylo nezahrnutí velkých cév a dobře identifikovatelných lézí. Z pohledu našich expertů je v klinické praxi užitečnější počítat volumetrii funkčního parenchymu, která do výpočtu tyto struktury neuvažuje.
Testování segmentačního submodulu softwaru LISA neskončilo pouze u soutěžních dat. Ve FN Plzeň byla připravena sada 30 dat pacientů, která po úplné anonymizaci byla manuálně (Syngo Volume software, Siemens, Erlangen, Německo) a také interaktivně (software LISA) proměřena. Byla testována citlivost použití softwaru LISA při instalaci v operačním systému Windows, Mac OS a Linux. Vzhledem k tomu, že segmentační submodul nabízí interaktivní segmentaci, byla testována také citlivost na uživatele (zkušený radiolog (ZKR) Kliniky zobrazovacích metod (KZM), začínající radiolog (ZAR) Kliniky zobrazovacích metod a studentka medicíny (ST) Lékařské fakulty UK v Plzni). V případě manuální volumetrie jsme jako referenční sadu zvolili výsledky získané zkušeným radiologem KZM. Rozdíl v manuální volumetrii jsme schopni shrnout jen v číselném vyjádření objemu, viz Tab. 1.
Tab. 1. Číselné srovnání manuální volumetrie 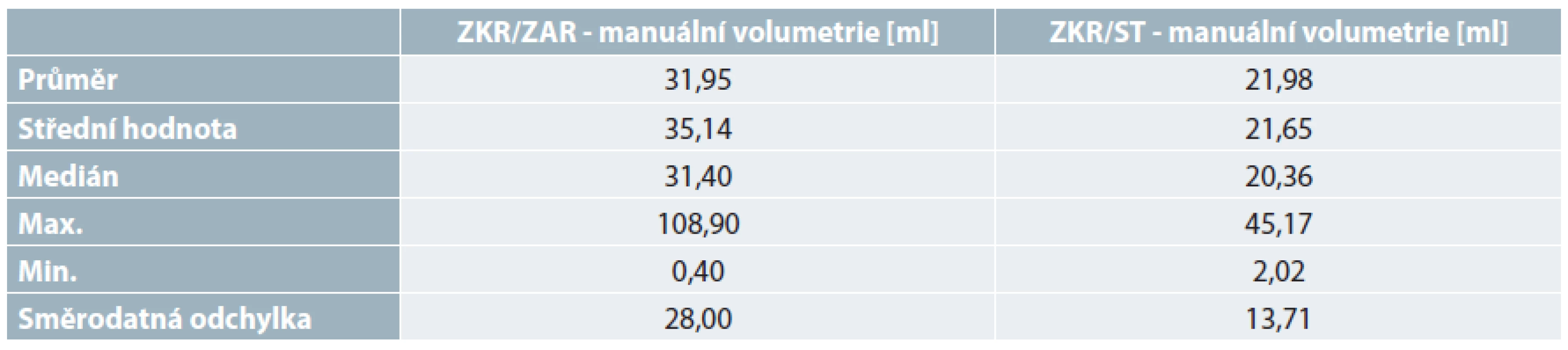
Poznámka: Číselné srovnání absolutní chyby manuálních volumetrií jater u 30 dat z CT abdominální oblasti. ZKR (zkušený radiolog Kliniky zobrazovacích metod Fakultní nemocnice Plzeň), ZAR (začínající radiolog Kliniky zobrazovacích metod Fakultní nemocnice Plzeň), ST (studentka medicíny Lékařské fakulty v Plzni Univerzity Karlovy v Praze). Interaktivní volumetrii jsme měřili jak pro řezy pořízených obrazových dat s šířkou řezu do 1 mm, tak pro řezy s šířkou řezu 5 mm. Interaktivní volumetrie je přesnější v případě zpracování obrazového záznamu s šířkou řezů do 1 mm, viz Tab. 2. Ve stejném případě ale dochází k selhání softwaru LISA instalovaného v operačním systému Windows z důvodu velkého nárůstu dat nutných pro zpracování. V dalším testování proto budeme pokračovat s operačními systémy Linux a Mac Os.
Tab. 2. Číselné srovnání manuální a interaktivní volumetrie 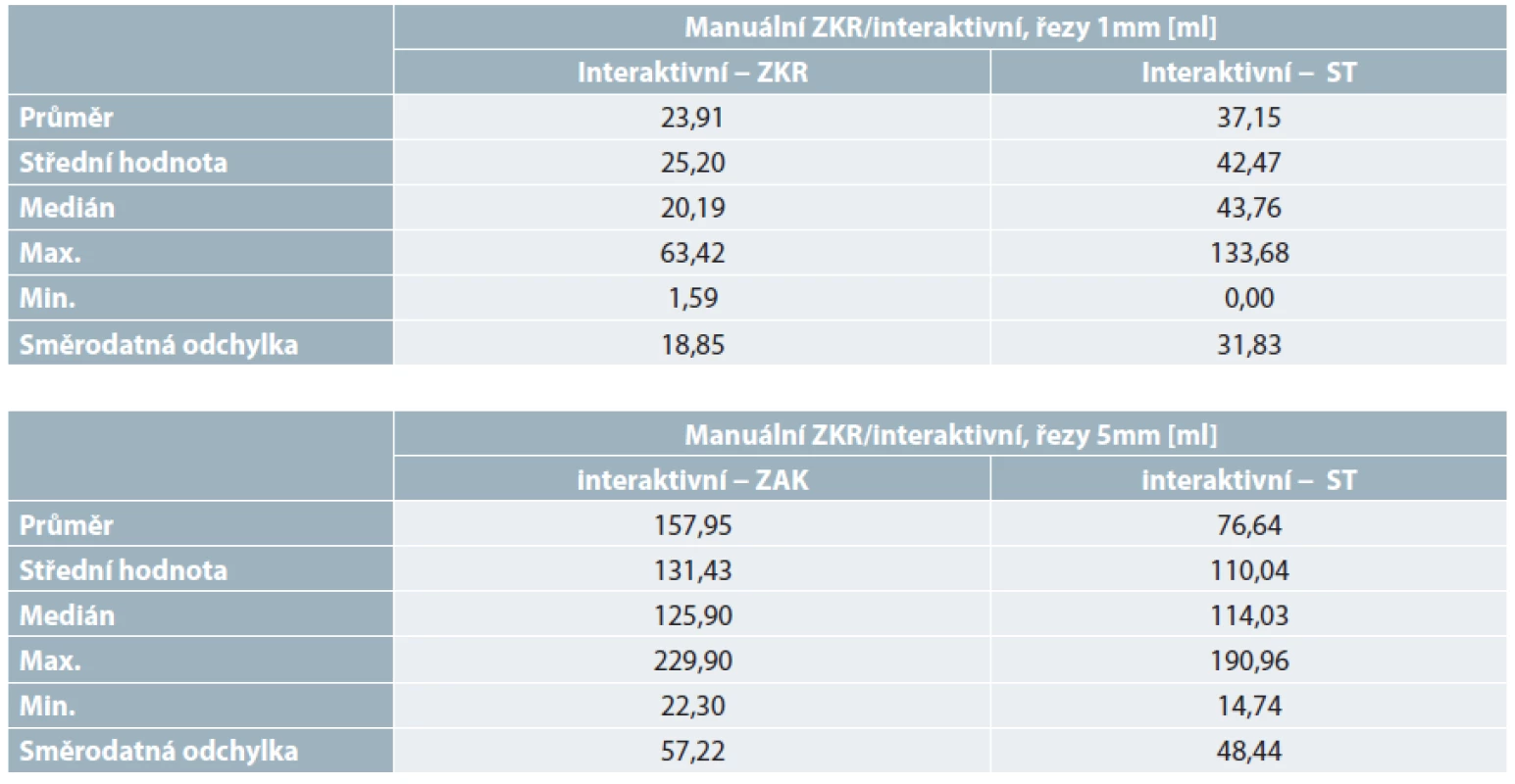
Poznámka: Srovnání (absolutní chyba) referenční manuální (ZKR) a interaktivní volumetrie (ZKR, ZAR, ST) jater u 30 dat z CT abdominální oblasti. Interaktivní volumetrie byla získaná z dat o šířce řezů do 1mm a 5mm. Začínající radiolog (ZAR) měl k dispozici software LISA instalovaný v operačním systému Windows. Zkušený radiolog (ZKR) a studentka medicíny (ST) měli k dispozici software LISA instalovaný v operačním systému Mac OS. Interaktivní volumetrii můžeme vzájemně srovnat i vizuálně. Na základě výsledků manuální a interaktivní (pro řezy do 1 mm) volumetrie zkušeného radiologa KZM jsme jako novou referenční volumetrii zvolili interaktivní volumetrii (pro řezy do 1 mm) získanou z měření ZKR softwarem LISA instalovaným v operačním systému Mac OS.
Při vizuálním srovnání volumetrií se ukázala chyba, ke které může dojít pouhým číselným srovnáním. Číselně vyjádřená volumetrie není dostatečný parametr pro srovnání kvality získané volumetrie. Tento fakt uvádí i celkové shrnutí výsledků ze soutěže SLIVER07 [9]. Číselně vyjádřená volumetrie se počítá z voxelů zahrnutých do segmentace jater. Dvě odlišné segmentace tedy mohou dát číselně stejný výsledek. Zjednodušeně řečeno, stejný počet voxelů zahrnutých v jednom řezu a nezahrnutých v jiném řezu u jednoho odborníka a naopak u druhého odborníka vede ke stejnému číselnému výsledku. Vizuální srovnání naproti tomu ukazuje skutečnou kvalitu volumetrie. Pokud chceme volumetrie srovnávat číselně, musíme přistoupit k jiné metrice – např. maximální rozdíl mezi okraji referenční a srovnávané segmentace atd. Metrik je několik a je možné je také kombinovat, viz článek shrnující výsledky soutěže SLIVER07 [9]. V dalším připravovaném testování segmentačního submodulu softwaru LISA budeme tedy muset přistoupit ke srovnání výsledků použitím jiné metriky nebo jejich kombinací. Přesto na základě dosažených výsledků můžeme přejít k rozšíření segmentačního submodulu i pro data z MRI. Segmentace jater z CT a MRI je důležitým krokem v předoperačním plánování resekce. Na segmentaci celého orgánu navazuje identifikace lézí v segmentované oblasti, segmentace cévního řečiště a další kroky vedoucí k virtuálnímu návrhu resekční linie. Naším cílem je vyvinout segmentační submodul, který bude spolehlivý a důsledně testovaný přímo na klinických datech. Obdobný zodpovědný přístup zvolili i jiní při vývoji softwarů zpracovávajících medicínská obrazová data, např. MEVISlab [4] nebo MiaLite [20]. Naším záměrem je rozšířit software LISA i pro experimentální chirurgii, proto se nemůžeme spoléhat jen na volně či komerčně dostupné softwary.
Virtuální resekce jater je komplexní úloha. Stejně jako k vlastní chirurgii jater vzhledem k chirurgii ostatních orgánů bylo přistoupeno o mnoho let později z důvodu komplikovaného cévního řečiště [6], tak v případě matematického a počítačového modelování se přistupuje také se značným zpožděním. Vše je dáno dlouhodobým vývojem vhodných metod, které lze v případě jaterního parenchymu použít [16,17]. Na druhé straně, díky tomu, že jednotlivé metody byly v minulosti používány i pro např. ložiskovou geologii v ropném průmyslu, jsou metody dnes dobře popsané, i když nejsou běžně aplikovány na živé materiály [18]. Proto očekáváme úspěšné řešení virtuální resekce jater zohledňující mikrostrukturu cévního řečiště. Mikrostrukturu cévního řečiště lidských jater lze popsat, viz [17], jen u omezeného počtu vzorků. Proto je statistický soubor malý a zobecnění vyplývající ze statistické analýzy nemusejí být důvěryhodná. My máme možnost pracovat s velkým souborem prasečích jater. Výsledky z naší statistické analýzy mohou být důvěryhodné. V našem případě vyvstává otázka přenositelnosti poznatků z mikrostruktury prasečích jater na lidská. Jsme teprve na začátku tohoto vědeckého poznání, a proto je nezbytná otevřená diskuze s ostatními vědeckými týmy, kterou úspěšně navazujeme.
V Plzeňském kraji byla navázána úspěšná spolupráce mezi fakultami dvou univerzit, která je především orientována na klinickou i experimentální chirurgii jater. Během několika let došlo k výraznému pokročení v počítačovém a matematickém modelování s cílem zefektivnit předoperační fázi resekce jater. Některé dílčí kroky jsou stále jen součástí vědeckého výzkumu, což je dáno komplikovaností jaterního cévního systému a také řadou nejasností fyziologické i patologické funkce jater. Přesto se podařilo přistoupit i ke klinickému testování, které nabízí důležitou zpětnou vazbu správné volby technického postupu při aplikaci v medicíně.
Zkratky
BioMMeda – vědecko-výzkumné výpočetní centrum zaměřené na aplikace v medicíně, Univerzita Gent, Gent, Belgie. Dostupné na www: http://www.biommeda.ugent.be/
CT – počítačová tomografie (Computed Tomography) – radiologická vyšetřovací metoda
DICOM − Digital Imaging and Communications in Medicine – je standard pro pořízení, skladování, distribuci aj. medicínských dat pořízených z CT, MRI a jiných radiologických vyšetřovacích metod
EU – státy Evropské unie
FN – Fakultní nemocnice Plzeň
INRIA − Inventeurs du monde numérique – výzkumné a výpočetní centrum ve Francii. Dostupné na www:http://www.inria.fr
IRCAD − Research Institute against Digestive Cancer – výzkumné a vzdělávací laparoskopické centrum, dostupné na www:http://www.ircad.fr
KZM – Klinika zobrazovacích metod, Fakultní nemocnice Plzeň
LF – Lékařská fakulta v Plzni Univerzity Karlovy v Praze
LISA – název vyvíjeného softwaru určeného k virtuální resekci jater. LISA jsou první písmena slov celého názvu „LIver Surgery Analyser“. Mezioborová spolupráce klinik Fakultní nemocnice Plzeň, ústavů Lékařské fakulty v Plzni Univerzity Karlovy v Praze a kateder Západočeské univerzity v Plzni
Mac OS – operační systém pro počítače Macintosh firmy Apple
MEVIS – výpočetní a výzkumné centrum zabývající se vývojem a servisem softwarů zpracovávajících medicínská data. Dostupný na www: http://www.mevis.de/
MITK − The Medical Imaging Interaction Toolkit – volně dostupný software zpracovávající medicínská data. Vznikl v rámci VLN ve spolupráci s German Cancer Research Center, Division of Medical and Biological Informatics, Heidelberg. Dostupný na www: http://mitk.org/wiki/MITK
MRI – magnetická rezonance (Magnetic Resonance Imaging) – radiologická vyšetřovací metoda
SLIVER07 – Segmentation of the LIVER 2007 – neustále otevřená soutěž, která vznikla v rámci sympozia „3D Segmentation in the Clinic: A Grand Challenge“ konference MICCAI pořádaná v roce 2007. SLIVER07 dostupná na http://sliver07.org
ST – studentka medicíny Lékařské fakulty v Plzni Univerzity Karlovy v Praze
VLN – Virtual Liver Network – konsorcium vědecko-výzkumných a klinických institucí v Německu zaměřené na výzkum funkce jater, virtuální plánování vhodné léčby jaterních onemocnění. Dostupné na www:http://www.virtual-liver.de
VR RENDER – software zobrazující medicínská data pořízená z CT, MRI. Je výstupem výpočetního centra IRCAD. Dostupný na www:http://www.websurg.com/softwares/vr-render/
ZAR – začínající radiolog Kliniky zobrazovacích metod Fakultní nemocnice Plzeň
ZČU – Západočeská univerzita v Plzni
ZKR – zkušený radiolog Kliniky zobrazovacích metod Fakultní nemocnice Plzeň
Poděkování
Práce vznikla za podpory z projektu IGA MZ CR NS 13326 a CZ.1.05/2.1.00/03.0076 spolufinancovaného z prostředků Evropské unie. Publikace je spolufinancována Evropským sociálním fondem a státním rozpočtem České republiky, název projektu „Zvýšení kapacity vědecko-výzkumných týmů Univerzity Karlovy prostřednictvím nových pozic pro absolventy doktorandských studií“, registrační číslo projektu: CZ.1.07/2.3.00/30.0061. Vytvořený software z veřejných zdrojů bude bezplatně k dispozici zájemcům na http://mjirik.github.io/lisa.
MUDr. Václav Liška, Ph.D.
Chotíkov 426
330 17 Chotíkov
e-mail: vena.liska@gmail.com
Zdroje
1. Valeri G, Mazza FA, Maggi S, et al. Open source software in a practical approach for post processing of radiologic images, La radiologia medica 2015;120 : 309−23.
2. Peterhans M, vom Berg A, Dagon B, et al. A navigation system for open liver surgery: design, workflow and first clinical applications. Int J Med Robot 2011;7 : 7−16.
3. Banz VM, Baechtold M, Weber S, et al. Computer planned, image-guided combined resection and ablation for bilobar colorectal liver metastases, World J Gastroenterol 2014;20 : 14992−6.
4. Couinaud C. Surgical anatomy of the liver revisited. Paris, 15 reu Spontini 75116, 1989.
5. Fasel JHD, Majno PE, Peitgen HO. Liver segments: An anatomical rationale for explaining inconsistencies with Couinaud’s eight-segment concept. Surg Radiol Anat 2010;32 : 761−5.
6. Fasel JHD, Schenk A. Concepts for liver segment classification: neither old ones nor new ones, but a comprehensive one. J Clin Imaging Sci 2013;3 : 48−54.
7. Včelák P, Klečková J. Automatic real-patient medical data de-identification for research purposes. Int J Eng Sci Technol of World Acad Sci Eng Technol 2011;52 : 506−10.
8. Boykov Y, Funka-Lea G. Graph cuts and efficient N-D image segmentation. Int J Comput Vis 2006;70 : 109–31.
9. Ginneken B, Heimann T, Styner M. 3D Segmentation in the clinic: A grand challenge. In: MICCAI Workshop Proceedings 2007 : 7−15.
10. Segmentation of the Liver Competition, 3D Segmentation in the clinic: A grand challenge [on line]. SLIVER07 dostupná na www: http://sliver07.org.
11. Králíčková A, Eberlová L, Kalusová K, et al. Quantification of liver microcirculation using X-ray microtomography of vascular corrosion casts, Key Eng Mater 2014;592-3 : 505−8.
12. Lukeš V, Jiřík M, Jonášová A, et al. Numerical simulation of liver perfusion: from CT scans to FE model. Proc. of the 7th Eur conf. on python in science 2014. Dostupný na www:arXiv preprint arXiv 1412.6412.
13. Michler C, Cookson AN, Chabiniok R, et al. A computationally efficient framework for the simulation of cardiac perfusion using a multi-compartment Darcy porous-media flow model, Int J Numer Meth Biomed Engng 2013;29 : 217–32.
14. Hyde ER, Cookson AN, Lee J, et al. Multi scale parametrization of a myocardial perfusion model using whole organ arterial networks, Ann of Biomed Eng 2014;42 : 797–811.
15. Brůha J, Vyčítal O, Tonar Z, et al. Monoclonal antibody against transforming growth factor beta 1 does not influence liver regeneration after resection in large animal experiments. In Vivo 2015;29 : 327−40.
16. Debbaut Ch, Segers P, Cornillie P, et al. Analyzing the human liver vascular architecture by combining vascular corrosion casting and micro-CT scanning: a feasibility study. J Anat 2014;224 : 509−17.
17. Debbaut Ch, Vierendeels J, Casteleyn C, et al. Perfusion characteristics of the human hepatic microcirculation based on three-dimensional reconstructions and computational fluid dynamic analysis. J Biomech Eng 2012;134 : 10 pages.
18. Moreno R, Borga M, Smedby O. Techniques for computing fabric tensors: A review. In: Visualization and processing of tensors and higher order descriptors for multi-valued data. Berlin/Heidelberg, Springer, Mathematics and Visualization 2014 : 271−92.
19. Liver Surgery Analyser LISA [on line]. Dostupný na www: http://mjirik.github.io/lisa.
20. Wang Ch, Frimmel H, Smedby O. Fast level-set based image segmentation using coherent propagation. Medical Physics 2014;41 : 073501.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek Data pro chirurgii
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2015 Číslo 11- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Hojení análních fisur urychlí čípky a gel
-
Všechny články tohoto čísla
- Data pro chirurgii
- Hepatální pseudoléze v blízkosti falciformního ligamenta
- Léčba infekce v třísle po tepenné rekonstrukci pomocí podtlakové terapie
- Naše zkušenosti s měřením transkutánní tenze kyslíku pro hodnocení prokrvení periferie dolních končetin u pacientů s chronickou ischemickou chorobou dolních končetin
- K životnímu jubileu primáře Herberta Jaroška
- Stanovení exprese CEA, EGFR a hTERT v peritoneální laváži u pacientů s adenokarcinomem pankreatu metodou RT-PCR
- Resekabilní karcinom pankreatu − 5leté přežití
- Perigraft serom jako vzácná angiochirurgická komplikace
- Dialyzační cévní přístup transponovanou vena femoralis superficialis
- Software LISA – virtuální resekce jater pro urychlení a usnadnění předoperačního plánování
- 41. sjezd českých a slovenských chirurgů
- Gerontochirurgie a její problémy
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hepatální pseudoléze v blízkosti falciformního ligamenta
- Naše zkušenosti s měřením transkutánní tenze kyslíku pro hodnocení prokrvení periferie dolních končetin u pacientů s chronickou ischemickou chorobou dolních končetin
- Resekabilní karcinom pankreatu − 5leté přežití
- Léčba infekce v třísle po tepenné rekonstrukci pomocí podtlakové terapie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



